Clear Sky Science · ja
小型(〈100 kDa)GPCRのクライオEM構造研究に向けた戦略的進展
なぜ小さな細胞のスイッチが医学で重要なのか
現代医学の多くは、細胞膜に存在する小さなスイッチ、Gタンパク質共役受容体(GPCR)をそっと調整することで機能します。これらのスイッチはホルモンや匂い、薬物を感知し、承認薬のおよそ3分の1が標的としています。より安全で賢い薬を設計するには、特に薬が標的にする「オフ」状態、つまり不活性形のこれら受容体の詳細な3次元像が必要です。本記事は、分子をほぼ自然な状態で凍結して観察できる強力なイメージング法であるクライオ電子顕微鏡(クライオ‑EM)を用いて、最も小さなGPCRのいくつかを可視化する研究がどのように進んでいるかを解説します。
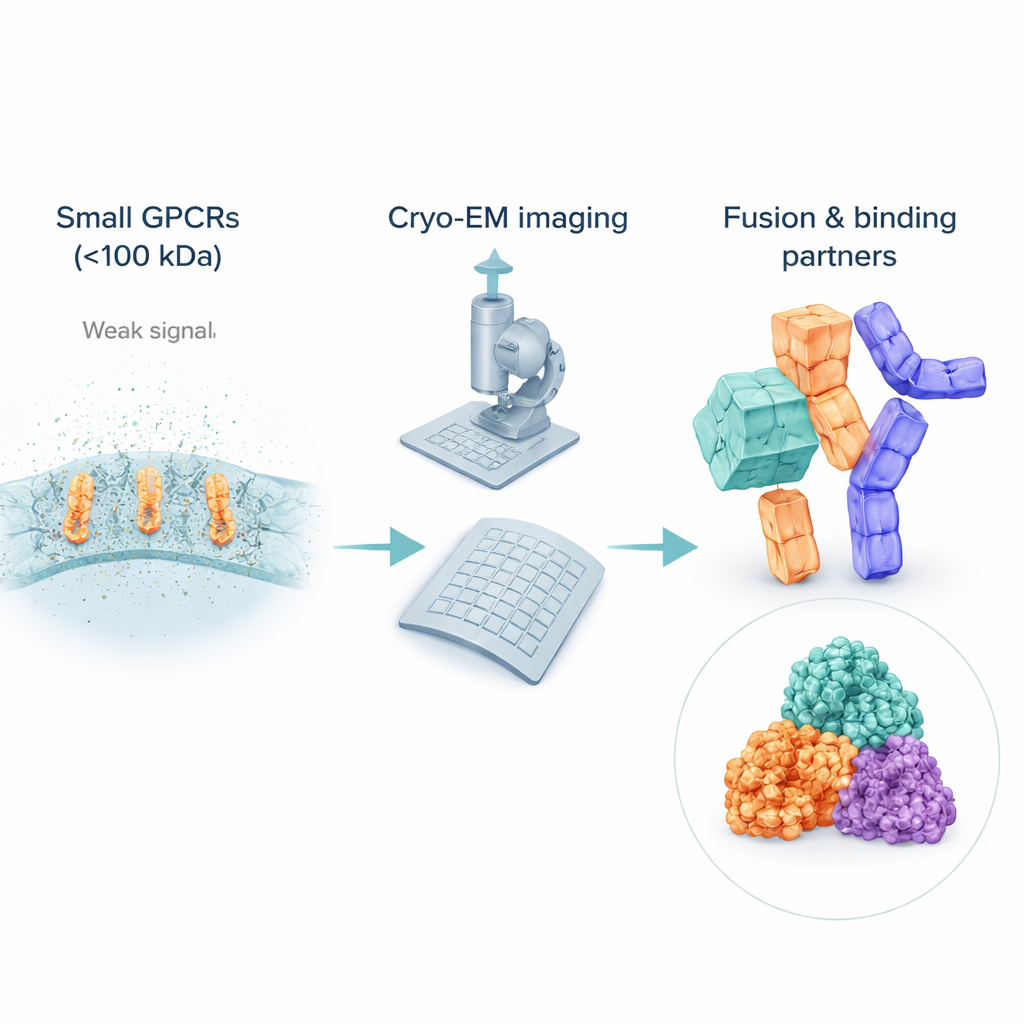
非常に小さな受容体を観る際の課題
クライオ‑EMは構造生物学に革命をもたらしましたが、それでも小さく柔軟な分子の扱いには限界があります。多くの不活性GPCRは100キロダルトン未満であり、ノイズの多い画像で検出・整列するのが難しいです。可溶化のためにこれら受容体を界面活性剤の泡や脂質模倣体で包むと、電子線には受容体自身より「大きく」見え、目的タンパク質の信号が埋もれてしまうことがあります。Gタンパク質のような大きな相手と結合した活性型受容体とは異なり、不活性GPCRは外側に目立つ突起がないことが多く、そのため多数の画像を平均化して鮮明な3次元像を得るのがコンピュータにとって難しくなります。その結果、不活性GPCRの構造の多くは依然として古典的なX線法から得られており、薬が作用する重要な領域でクライオ‑EMのカバレッジに穴が残っています。
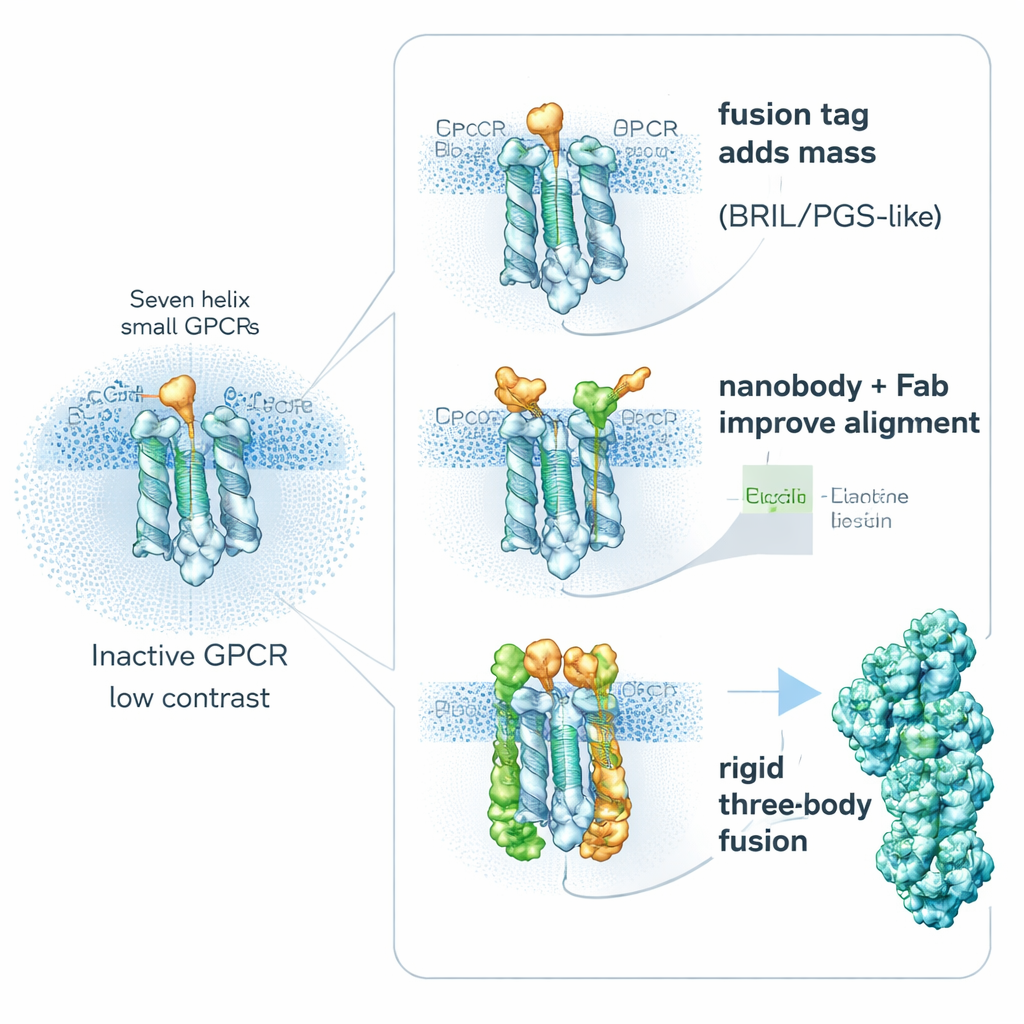
受容体を内蔵ヘルパーで「大型化」する
一つの重要な戦略は意外に単純で、受容体を意図的に「重くする」ことです。研究者は遺伝子融合により、小さく安定したヘルパータンパク質をGPCRの柔軟な領域に付加してサイズと剛性を高め、薬結合領域を阻害しないようにします。広く使われるヘルパーには、4本のヘリックス束であるBRIL、耐熱性酵素断片のPGS、より大きなクランプ様タンパク質であるカルシニューリンなどがあります。これらの融合パートナーは、多くの場合、二つのヘリックスをつなぐ可動な内側ループに挿入されます。この領域を硬くすることで分子運動によるブレを減らし、コンピュータが粒子を整列させるための認識しやすい形状を提供します。研究は、融合ピースの正確な位置と配向が成功を左右することを示しており、ある受容体ではPGSタグの配置を変えることで解像度がぼやけた6オングストロームから明瞭な3.7オングストロームに改善した例があります。
抗体や設計された結合体をハンドルとして借用する
第二のアプローチは受容体に大きな融合体を組み込む代わりに、外側から高親和性の「ハンドル」を付ける方法です。ナノボディと呼ばれる小さな抗体断片やそれに類する結合体は、不活性GPCRを認識して可動な内側ループに結合するよう作られます。代表的な例がNanobody‑6で、最初はあるオピオイド受容体のセンサーとして作られ、その後わずかな修正で複数の他のGPCRの不活性形を安定化するために再利用されました。オフセンターで結合するため、各粒子に明確な配向手がかりを与え、画像平均化の信頼性を高めます。研究者はこれをさらに拡張し、ナノボディ自体を認識する通常の抗体断片を追加して、より大きく剛性の高い複合体を作り、クライオ‑EMで鮮明に映るようにすることが多いです。DARPinsなどの他の設計結合体は、モジュラーなスペーサーやより大きなタンパク質ケージへの連結子として用いることで、非常に小さな標的からの信号をさらに増強できます。
賢いサンプル設計とAIで強化された画像処理
ヘルパーの融合や結合体の追加は物語の一部にすぎません。レビューは、良好な構造は慎重に設計された受容体コンストラクトから始まると強調します:だらしない末端領域の切除、安定化変異の導入、問題を引き起こしやすい部分を特定するための現代的な構造予測ツールの利用などです。イメージング面では、微弱な粒子のコントラストを高める位相板のような古い手法が、人工知能ツールによって補完あるいは置き換えられつつあります。ディープラーニングプログラムはノイズの多いマイクログラフの中から微小な粒子を見つけ出し、新しいアルゴリズムは受容体が多様なコンフォメーションをとる場合に画像を異なる形状に分類できます。これらの進展はフィデュシャルヘルパーと組み合わさって、かつては小さすぎるか動的すぎると見なされた膜タンパク質をクライオ‑EMで確実に解像する方向へと推し進めます。
将来の医薬品にとっての意義
この記事は、すべての受容体に効く単一の「魔法の」ヘルパーは存在しないが、融合パートナー、抗体様結合体、AI駆動の手法という道具箱が拡大しており、不活性GPCRの領域をクライオ‑EMで徐々に明らかにしている、と結んでいます。専門外の読者への要点は、小さな受容体を顕微鏡にとってより大きく秩序立って見えるようにすることで、科学者たちは多くの薬が好んで結合する正確な形状の詳細なスナップショットをついに得られるようになったということです。これらの構造的ブループリントは、これらの細胞スイッチをより正確にオフにする、あるいは活動を微調整する薬を、より少ない副作用で設計することを加速するはずです。
引用: Singh, S.K., Agrawal, M., Pattanayak, A. et al. Strategic advances for cryo-EM structural studies of small (<100 kDa) GPCRs. Commun Biol 9, 237 (2026). https://doi.org/10.1038/s42003-026-09516-y
キーワード: Gタンパク質共役受容体, クライオ電子顕微鏡, 創薬, 構造生物学, ナノボディ足場