Clear Sky Science · ja
分子張力と細胞牽引力を結びつける:焦点接着力学へのマルチスケールアプローチ
細胞が周囲を感じ、引く仕組み
細胞が移動したり分裂したり組織の形を変えたりするたびに、周囲にそっと力をかけています。こうした小さな機械的な引っ張りは創傷治癒、がんの転移、臓器の発生に重要ですが、直接見ることは難しく、測定もさらに難しい。本研究では、細胞がやわらかい基材に対して全体としてどれだけ引いているかと、細胞内の接着部位にある個々の「分子ばね」がどれだけの力を担っているか、という二つの視点を同時に観察する新しい方法を示します。これらの視点を結びつけることで、細胞が剛性を感知し周囲への把持を調節する仕組みの解明に貢献します。
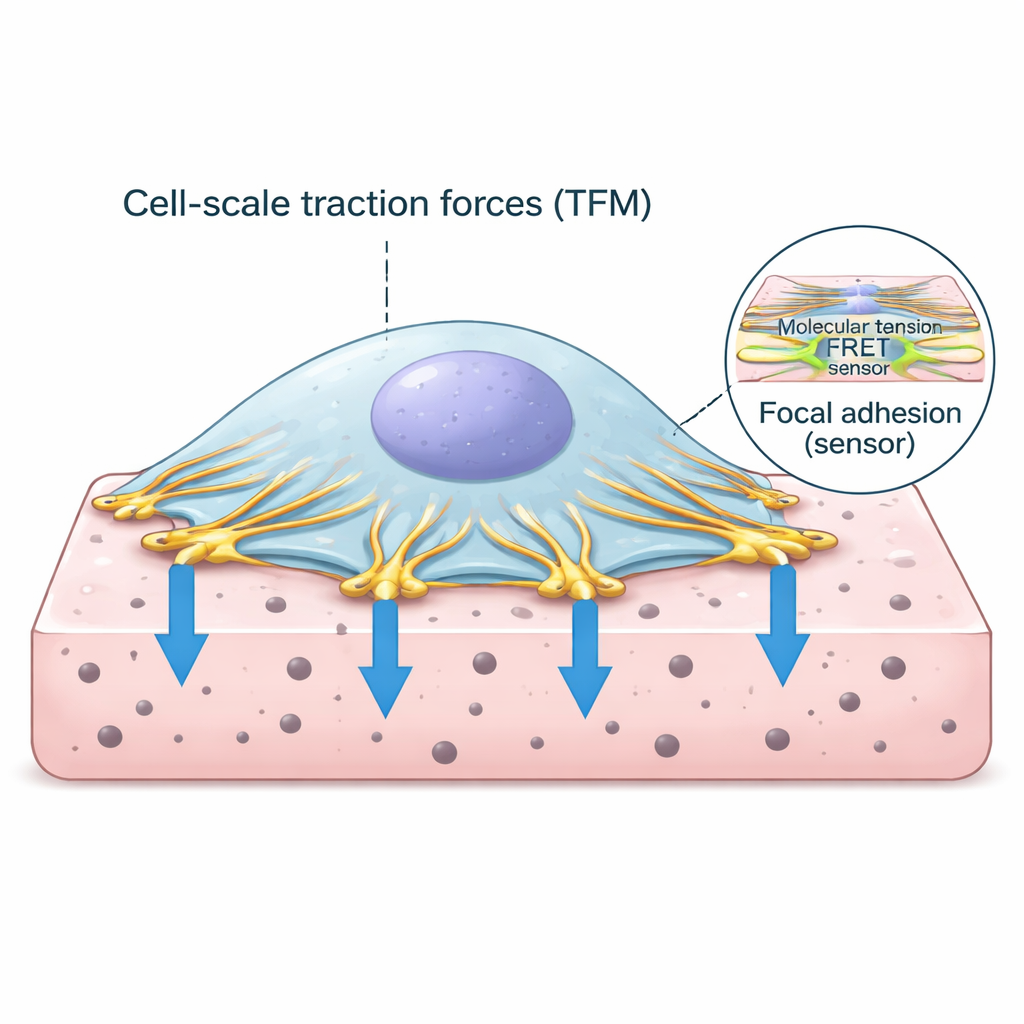
細胞が外界に作る把持点
細胞は組織中をただ浮いているのではなく、焦点接着と呼ばれる特殊な接触点を通じて基質に固定しています。これらの場所では、細胞内のアクチン繊維骨格が細胞膜を貫通するタンパク質に接続し、周囲の基質に取り付いています。アンカリング複合体の重要なタンパク質の一つがビンキュリンで、力に反応するリンクのように振る舞います。細胞の収縮機構がアクチンを引くと、ビンキュリンが負荷を感知して結合を強化します。これらのリンクを通してどれだけの力が伝わるか、そしてそれが細胞全体の引きとどう関連するかを理解することは、組織が健康であるか病的になるかを解読するうえで中心的です。
細胞力を見る二つの窓
研究者たちは二つの強力な手法を一つのワークフローに統合しました。まず、牽引力顕微鏡法は、基質中の微小蛍光ビーズの動きを追跡することで、細胞が柔らかいゲル状基材をどれだけ変形させるかを測定します。これらのビーズの動きから、細胞の下での押し引きの力の分布を算出できます。次に、特別に設計されたビンキュリンには伸張時に光信号が変わる蛍光張力センサーが組み込まれています。進んだ寿命イメージングを用いて、この光信号をビンキュリン上の分子張力の読み出しに変換しました。高解像度で撮像できる薄い平坦なハイドロゲルを設計し、両データセットを個々の接着部位まで整列、セグメント化、解析するためのカスタムソフトウェアを作成しました。
剛性が細胞の努力をどう変えるか
細胞をやわらかいゲルとより剛いゲルで培養したとき、全体的な振る舞いには明確な違いが出ました。剛い基材上では細胞はより広がり、基材表面に対して強い牽引力を発揮しました。同時に、ビンキュリンセンサーの蛍光読み出しは焦点接着内で高い分子張力を示しました。興味深いことに、接着の基本的な構造的特徴―数や平均サイズなど―はやわらかいゲルと剛いゲルで大きく変わりませんでした。それよりも、力の組織化のしかたが変わっていました。放射状に大きな接着でビンキュリンが多いものはより高い牽引力を担う傾向があり、接着部位のジオメトリと分子構成が細胞の引く強さを決める助けになっていることが示唆されます。
局所力と分子力の複雑な関係
個々の接着部位を詳しく見ると、局所的な牽引とビンキュリン張力の関係は一様ではないことが明らかになりました。ある細胞では、高い牽引を生む接着は高いビンキュリン張力も示し、荷重がかかった接触は分子レベルでも直接的に力を共有していることを示唆しました。別の細胞では逆のパターンが現れ、強い牽引領域は低いビンキュリン張力に結びつき、他の接着が分子負荷を多く担って外向きの大きな引きを生み出さない場合もありました。多くの細胞では明確なパターンが見られませんでした。これらの異なる振る舞いは、活発な広がり、安定した接着、収縮などの細胞状態の違いを反映している可能性が高く、細胞が接着ネットワーク全体で力を多様な方法で再配分できることを示唆します。
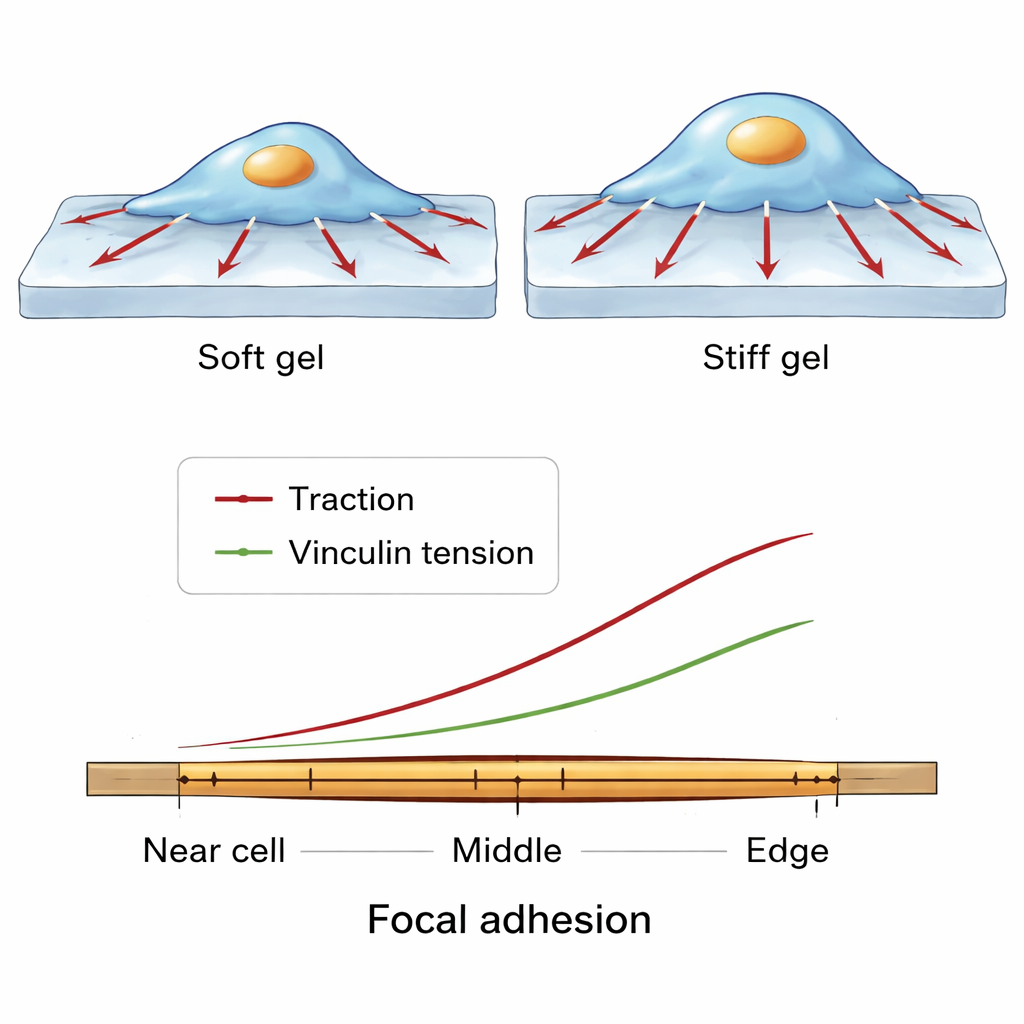
単一の把持点に沿った微細な力のパターン
研究チームはさらに詳細に踏み込み、単一の焦点接着の長さに沿って、細胞中心側から細胞の周辺に近い端まで力がどのように変化するかを調べました。多くの細胞と条件を横断して、一貫したパターンが現れました。ビンキュリン分子は接着の中央寄りに最も密に詰まっていました。しかし、基質にかかる牽引とビンキュリン上の分子張力はいずれも外側のより末端側へ向かって上昇しました。これはバランスの取り合いを示唆します:中央領域では多くのビンキュリン分子が荷重を分担するため各分子の張力は小さく、外側端では少ない分子が比較的大きな力を担って強い局所的な引きを支えつつ接着を保っているのです。
健康と病のための示唆
全細胞の牽引マップとタンパク質レベルの張力測定を統合することで、本研究は細胞が機械的な把持をどのように管理しているかのマルチスケールな像を提示します。環境が剛くなると細胞はより強く引き、ビンキュリンのリンクにより大きな負荷をかける一方で、外向きの力と分子張力との詳細な関係は接着ごと、細胞ごとに異なることが示されました。同時に、個々の接着内での力の空間分布に関する頑健なパターンは保存されているようです。専門外の方への主要なメッセージは、細胞はどこでどう引くかを精密に調節し、多くの小さな分子“ばね”に力を再配分して異なる機械的環境に適応している、ということであり、これは組織発生、線維化、がん侵襲といった多様な過程の基盤となる原理かもしれません。
引用: Aytekin, S., Kimps, L., Coucke, Q. et al. Linking molecular tension and cellular tractions: a multiscale approach to focal adhesion mechanics. Commun Biol 9, 236 (2026). https://doi.org/10.1038/s42003-026-09514-0
キーワード: 細胞力学, 焦点接着, ビンキュリン, 牽引力顕微鏡法, 機械的シグナル伝達