Clear Sky Science · ja
ヒト細胞におけるLbuCas13aによる二次的RNA切断の時間動態
細菌の防御機構を精密な細胞キラーに変える
研究者たちは、細菌の免疫タンパク質をヒト細胞の高度に選択的な「自己破壊」スイッチに変える方法を発見しました。LbuCas13aと呼ばれるCRISPR酵素を利用することで、細胞内の特定のRNAメッセージを認識し、それに続いてほぼすべての他のRNAを断片化できます。一般向けに言えば、RNAメッセージは細胞がどのタンパク質を作るかを決めるため、それらを任意に消去できることは、がん治療や抗ウイルス戦略、新たな研究ツールへの道を開く興味深い発見です。
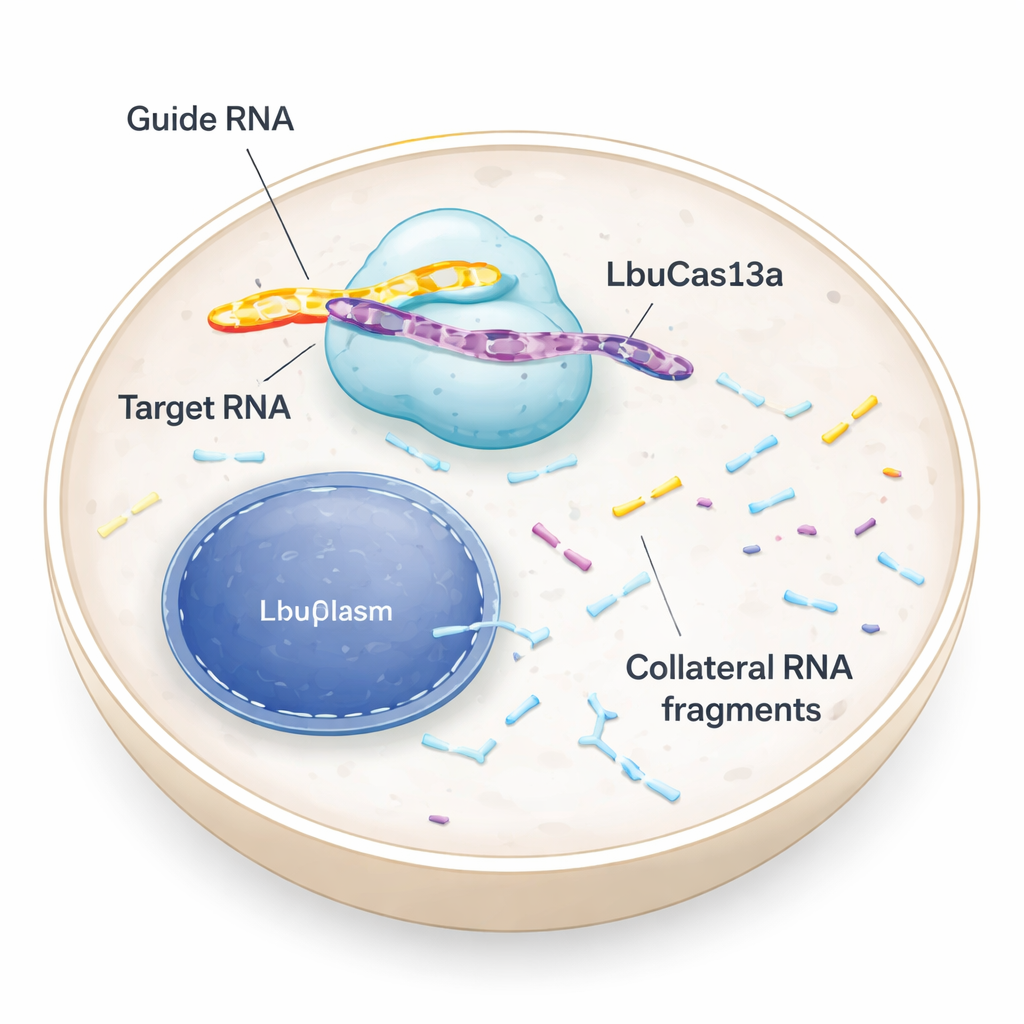
DNAでなくRNAを狙う分子はさみ
多くの人がDNAを切断して遺伝コードを書き換えるCRISPRツールについて聞いたことがあるでしょう。LbuCas13aは異なります:これはDNAではなくRNA、すなわちDNAからタンパク質合成装置へ指示を運ぶ一時的なメッセージを認識して切断します。細菌ではCas13酵素は抗ウイルス防御の一部であり、ウイルスRNAを検出するとその侵入者を切断するだけでなく周囲の多くのRNAも切り刻みます。このいわゆる「コラテラル(副次的)」活性は、感染した細胞を休眠や死へと導き、細菌集団を保護します。動物やヒト細胞での初期の試験では、Cas13のコラテラル切断は弱いか欠如していると考えられていたため、酵素は主に精密なRNAの「オフスイッチ」として使われてきました。新しい研究はその仮定を再検討し、適切な条件下ではヒト細胞でもコラテラル活性が強く有用になり得ることを示しています。
ヒト細胞でコラテラル切断を解き放つ
研究チームは複数のCas13バリアントを比較し、LbuCas13aが特に強力であることを発見しました。彼らは精製したLbuCas13aタンパク質を短いガイドRNAとあらかじめ複合化した状態で、リボヌクレオプロテイン(RNP)として直接ヒト細胞に導入しました。ガイドが蛍光マーカー遺伝子やGAPDHや18SリボソームRNAのような豊富な天然メッセージなどターゲットRNAと一致すると、酵素はまずそのターゲットを切断し、続いて多くの他のRNAを切り刻み始めました。約50分以内に細胞の全体的なRNAプロファイルは劇的に変化し、特徴的な切断断片が現れました。このコラテラル効果は異なる導入方法や複数の細胞種で観察され、一つの細胞株や人工的なターゲットの特異的な現象ではないことを示しています。
RNAの粉砕から細胞死と選択へ
RNAメッセージが突如として消えた細胞には何が起きるのでしょうか。ライブセルイメージングで、研究者たちはターゲットRNAを発現する細胞が徐々にアポトーシス、すなわち細胞が秩序立って分解されるプログラム細胞死に入る様子を観察しました。この過程は、細胞が崩壊する前に現れる特徴的な「早期警告」シグナルを伴います。重要なのは、ターゲットRNAを発現していない隣接細胞はほとんど影響を受けなかったことで、自己破壊が特異的であることを示しています。グループはこの特性を選択ツールとしても活用しました。ターゲットを持つ細胞を正常な細胞と混合してLbuCas13aを活性化すると、ターゲットを持つ細胞は数日で選択的に枯渇しました。処理を繰り返すことでその割合はさらに低下します。彼らはこれが遺伝子編集に成功した細胞を濃縮するのに使えること、またCDK4のような癌遺伝子を過剰発現する癌細胞を攻撃し、関連するがRNA量の少ない細胞を温存するように調整できることを示しました。
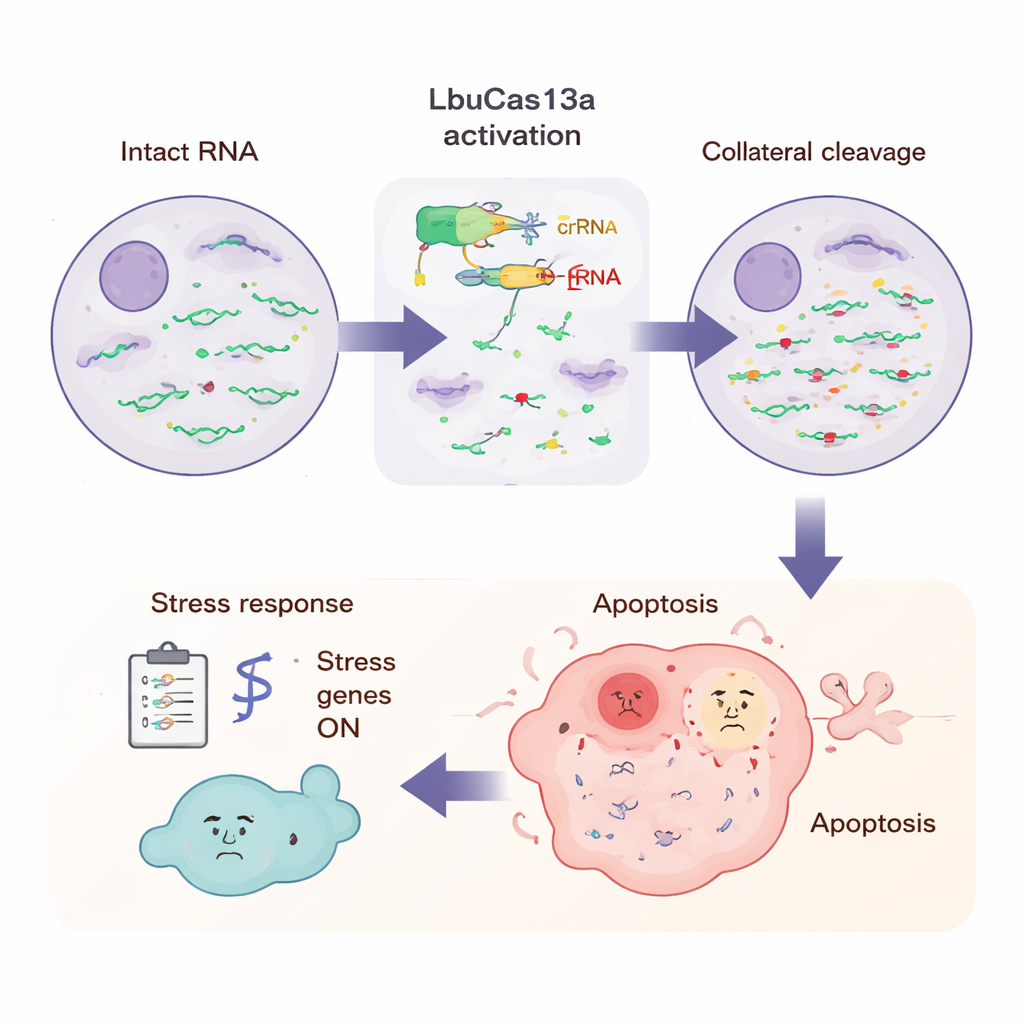
攻撃中に細胞が経験すること
全体像を把握するため、科学者たちはLbuCas13a活性化後のいくつかの時点で細胞内の全RNAを測定しました。既知のRNA標準をスパイクインすることで、細胞質にあるほとんどのタンパク質コードRNAが数時間以内に半分以上減少した一方で、ミトコンドリア由来のメッセージや一部の核内非コードRNAは大部分が保たれていることが分かりました。ロングリードシーケンシングは、切断が繰り返し現れる特定の塩基位置で起きていることを明らかにし、多くはウラシルに富む柔軟なループ領域での切断であり、試験管実験で見られたパターンと一致しました。後期の時点では、多くのストレス応答や自然免疫関連遺伝子がオンになり、炎症性シグナルや抗ウイルス防御に関わる遺伝子群が含まれていました。このパターンは、細胞が壊れたRNA末端の急増をウイルス感染のように感知し、警報プログラムを起動して最終的にアポトーシスに至ることを示唆しています。
なぜ重要か、そして今後の展望
簡潔に言えば、本研究はLbuCas13aをRNA誘導型の「殺傷スイッチ」に変えられることを示しています:ある細胞が特定のRNAを過剰に作る場合、そのRNAを標的にLbuCas13aを活性化すると事実上全体のRNAが失われ、免疫様の警報が鳴り、制御された細胞死に至ります。この過程は標的RNAの豊富さに強く依存するため、ある種のがん細胞のように有害な遺伝子を過剰発現する細胞を除去したり、研究や細胞療法の製造過程で混在する不要な細胞を除去したりするために利用できる可能性があります。一方で、本研究は注意を促す教訓でもあります:RNAを標的とするCRISPRツールは強力な副作用を持ちうるため、慎重な管理が必要です。コラテラルRNA切断がいつどのように起きるかを理解することは、医療やバイオテクノロジーでCas13技術を安全に使うために不可欠です。
引用: Bot, J.F., Zhao, Z., Li, M. et al. Temporal dynamics of collateral RNA cleavage by LbuCas13a in human cells. Commun Biol 9, 233 (2026). https://doi.org/10.1038/s42003-026-09511-3
キーワード: CRISPR-Cas13, RNA切断, 細胞死, がん標的化, 遺伝子編集ツール