Clear Sky Science · ja
プラズマ膜脂質によるヒトクラスB1 GPCRの調節
細胞の受信機を微調整する脂肪分子
細胞は受容体と呼ばれる小さなタンパク質アンテナに依存してホルモンや神経伝達物質を感知します。多くの主要な医薬品はこれらの受容体を標的にしています。本研究は、細胞外層に存在する一般的な脂質が単なる受動的な背景を作る以上の役割を果たし、重要な受容体群全体に直接結合して形を変え、シグナルのオン/オフを微妙に制御していることを明らかにしました。この隠れた制御層を理解することで、副作用の少ないより賢い薬の設計につながる可能性があります。
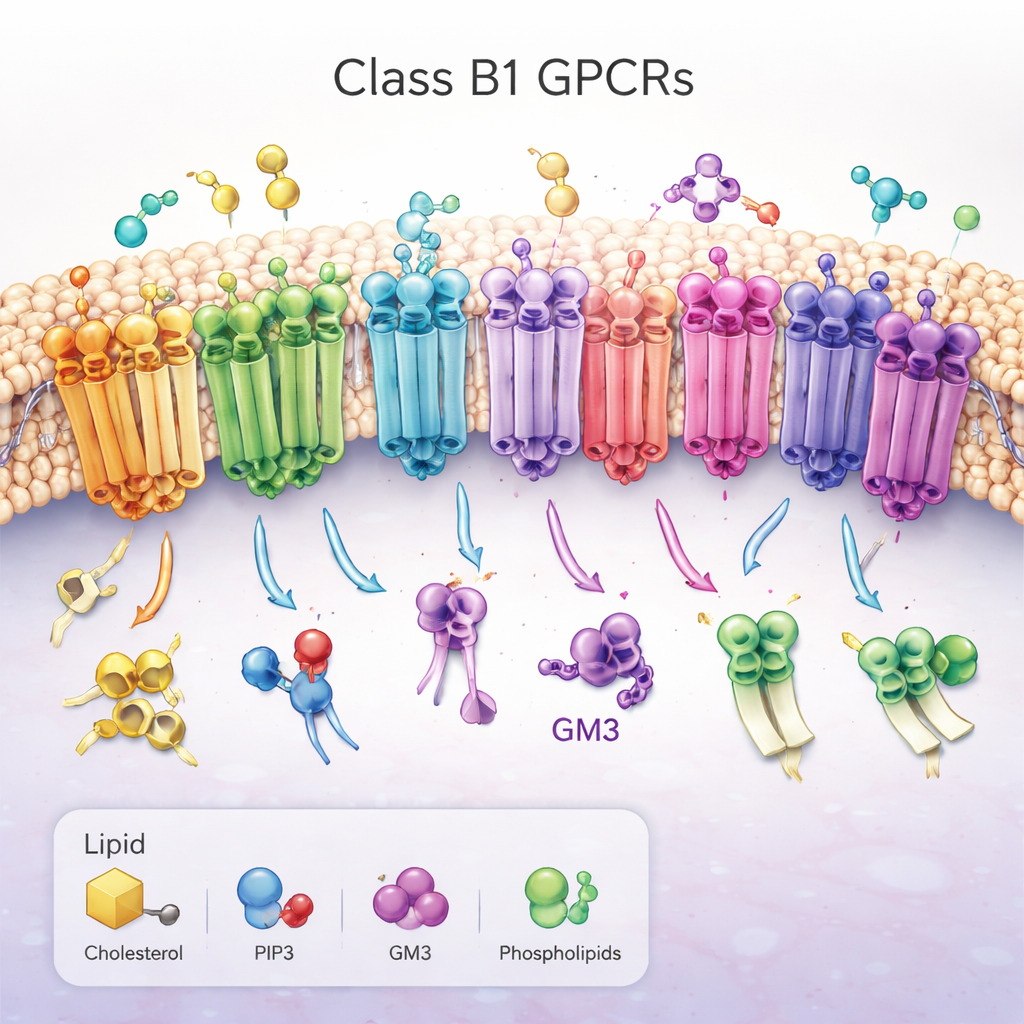
重要な分子アンテナのファミリー
本研究はクラスB1のGタンパク質共役受容体(GPCR)に焦点を当てています。これは血糖、代謝、成長、ストレス応答の制御に関与する15個の密接に関連した受容体群です。これらは脂質膜を貫いて配置され、細胞外側にホルモン様分子をつかむ大きな「頭部」を持ち、膜を通す7本のヘリックスの束を備えます。活性化されると、受容体は細胞内側で形を変え、パートナータンパク質を引き寄せる溝を開いてシグナル伝達を引き起こします。糖尿病や肥満などの疾患における中心的役割から、クラスB1 GPCRは重要な薬物標的ですが、それらを取り巻く膜脂質がどのように調節しているかはこれまで不明瞭でした。
自然な環境を模した受容体のシミュレーション
研究者らは受容体を人工的な界面活性剤バブルで調べる代わりに、15種すべてのヒトクラスB1 GPCRを実細胞の脂質組成を模したコンピュータ生成膜に配置しました。粗視化分子動力学と呼ばれる手法を使い、各受容体の活性型と不活性型の両方で複数の長時間シミュレーションを実行し、合計で約ミリ秒単位のシミュレーション時間を得ました。コレステロール、シグナル脂質PIP2、糖鎖を持つ脂質GM3という三つの「調節的」脂質が各受容体の異なる領域にどのように近づき、結合し、離れるかを追跡しました。大規模なデータセットを他者が再現・拡張できるよう、セットアップと解析の全工程をオープンワークフローツールaiida-gromacsで記録し、物理ベースの結果をタンパク質と小分子の結合を推測する新しいAIモデル(Chai‑1)の予測とも比較しました。
隠れたポケットと保存された脂質のつかみ
シミュレーションは受容体ファミリー全体にわたる再現性のある結合パターンを明らかにしました。食事の話題でよく知られるコレステロールは、既知のヘリックス上の部位だけでなく、ヘリックス間の「深い膜内」ポケットにも入り込み、極性頭部が膜内に異例に深く埋まる様子が観察されました。特にセクレチン受容体では、活性型と不活性型でそれぞれ異なるポケットに長時間結合する例が見られ、コレステロールがそのシグナル伝達を強く偏らせる可能性が示唆されます。PIP2は顕著に保存された挙動を示しました。PIP2は受容体の内側面、2本のヘリックスと短い尾部(TM6、TM7およびH8)の接合部付近に集まり、特に受容体が活性状態にあるときに顕著でした。この部位では、正に帯電したアミノ酸群が負に帯電したPIP2の頭部をつかむネットワークを形成しており、この脂質が活性形を安定化したり、細胞内側でパートナータンパク質を呼び寄せたりする仕組みを示唆します。
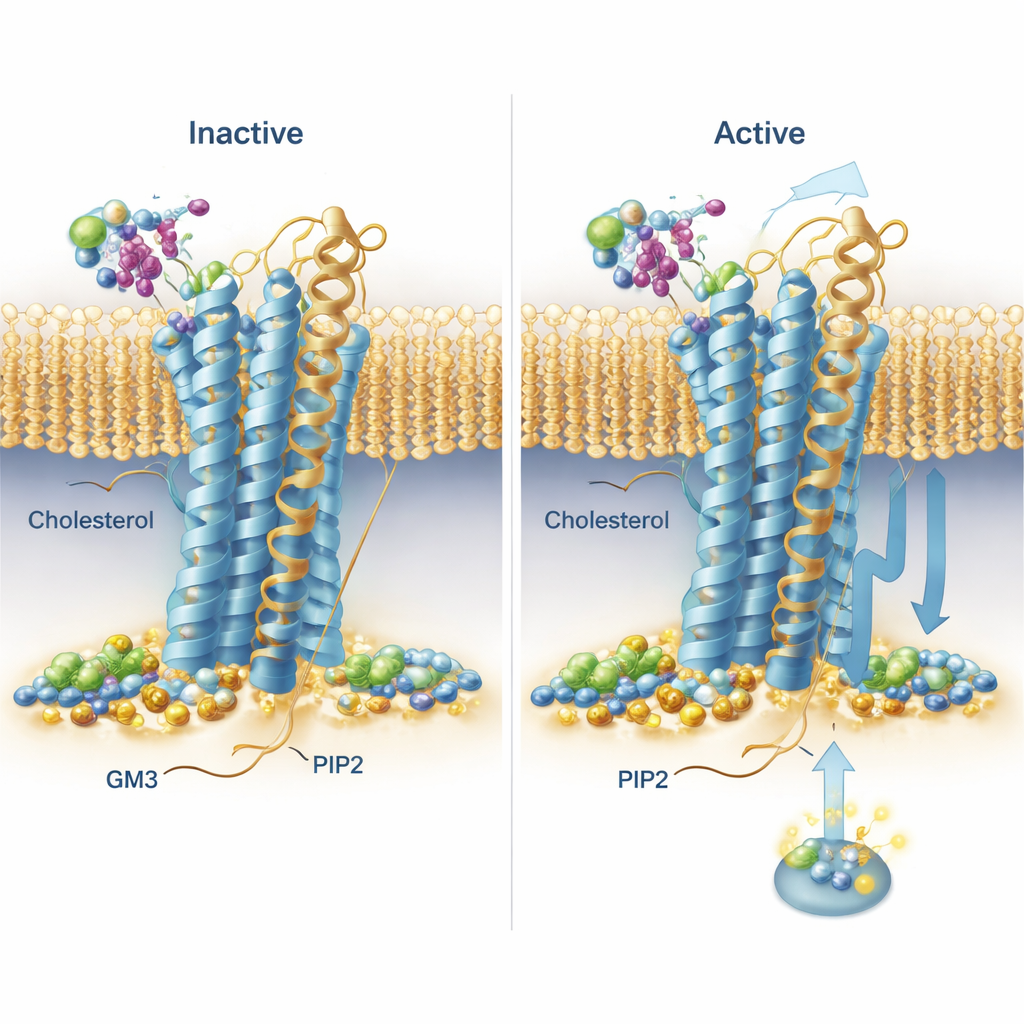
受容体の動きを促す糖被覆脂質
糖頭部をもつ複合脂質GM3は主に受容体の大きな外側頭部と相互作用しました。研究チームは、ある受容体では外側ドメインが膜に対して大きく振れ曲がるのに対し、他はより制約されていることに気付きました。薬理学的に重要な二つの受容体、GLP‑1RとGIPRについてはGM3の役割を詳しく調べました。GM3が存在するシミュレーションでは、GM3が外側ドメインとリガンド結合ポケットの基部に寄り添う(GLP‑1R)か、外側ドメインの先端に付着する(GIPR)かのいずれかで、いずれの場合もこれらドメインの動きの自由度に影響を与えました。これらの予測を生細胞で検証するため、研究者らは標識した受容体の頭部が膜にどれだけ近いかを報告する蛍光時間差法(TR‑FRET)という光ベースの手法を用いました。小分子阻害剤でGM3レベルを低下させると、刺激に応じた受容体頭部の変化に測定可能な変化が見られ、GM3が受容体や状態に依存して受容体の柔軟性を調節するという考えを概ね支持しました。
なぜこれらの脂質–受容体の結びつきが重要か
本研究はクラスB1 GPCRを単なるホルモンスイッチとしてではなく、周囲の脂質と緊密に調和したダンスの一部として描き出しています。コレステロールは隠れたポケットに入り込み特定のシグナル結果を微妙に優位にすることがあり、PIP2は受容体を活性形に固定してパートナータンパク質を導く可能性のある保存された内側の「取っ手」を形成し、GM3は受容体の外側領域の動きやリガンドとの出会い方を調整します。専門外の読者にとっての要点は、膜が能動的な調節層であるということです:脂質組成の小さな違いが同じ受容体の振る舞いを組織や疾患状態によって変える可能性があります。これらの相互作用を詳細にマップし、基礎となるシミュレーションデータを共有することで、本研究は特定の脂質接触を利用したり回避したりする新たな薬剤設計の基盤を築き、治療をより選択的かつ効果的にする道を開きます。
引用: Chao, K.W., Wong, L., Oqua, A.I. et al. Human class B1 GPCR modulation by plasma membrane lipids. Commun Biol 9, 317 (2026). https://doi.org/10.1038/s42003-025-09445-2
キーワード: Gタンパク質共役受容体, 膜脂質, コレステロール, PIP2, GM3