Clear Sky Science · ja
マルチモーダルAIによるERS–CAF免疫制御軸の解読とその汎がん予後・治療予測価値
メスを使わずに腫瘍をのぞく
がん治療に携わる医師たちは、腫瘍を取り巻く環境が腫瘍本体と同じくらい重要になり得ることをますます認識しています。しかし、この隠れた「近隣」を生検で繰り返し採取するのは侵襲的で、多くの場合実行しにくいのが現状です。本研究は、日常的な医療画像や顕微鏡画像を人工知能(AI)が読み解くことで、腫瘍内部の測りにくい免疫反応や瘢痕様過程を推定できることを示しており、日常の画像検査を異なるがん種にわたって機能する「デジタル生検」のように変え得る可能性を示唆します。
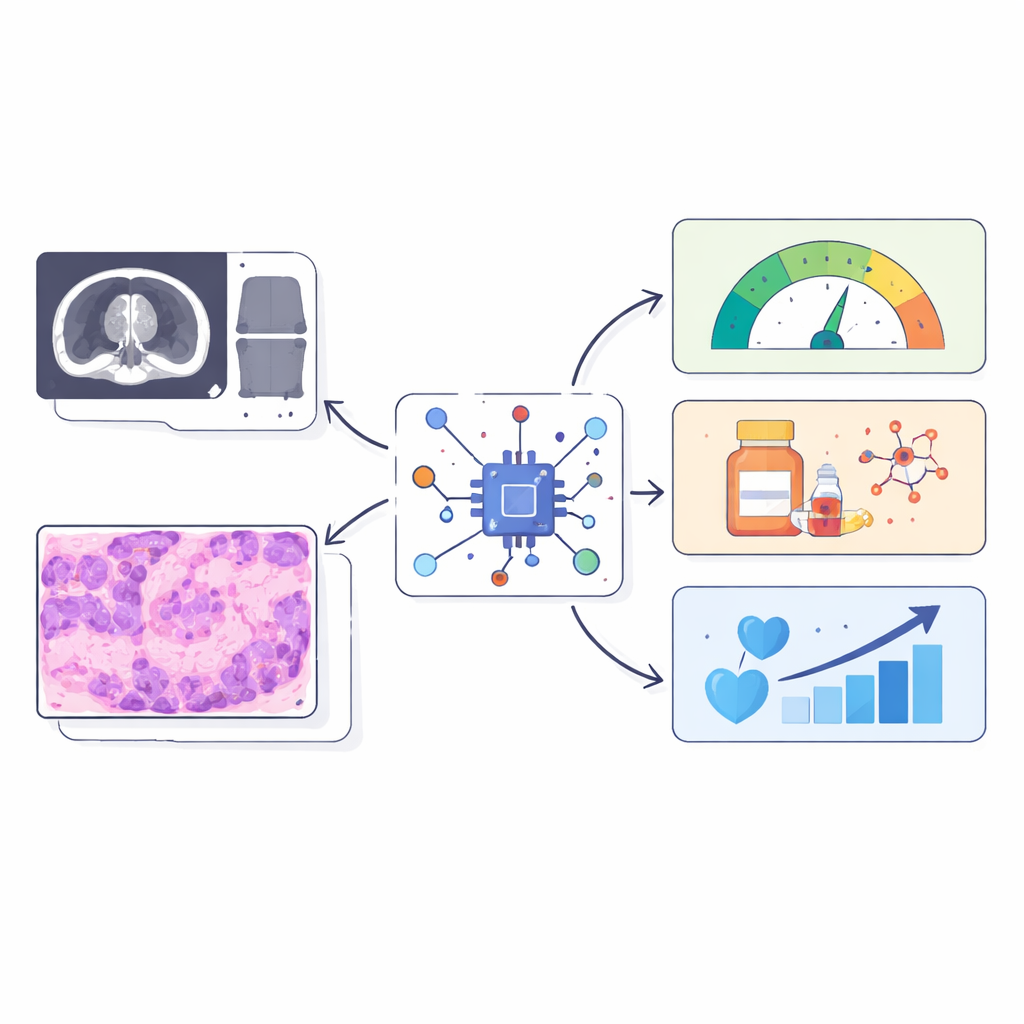
がん形成を形作る隠れた支持細胞
多くの実質性腫瘍は、線維芽細胞と呼ばれる特殊な支持細胞によって作られた頑丈な線維性の被膜に包まれています。これらの細胞が小胞体(細胞のタンパク質合成工場)でストレスを受けると、攻撃的でがんを助長する状態へと変化します。希少な骨腫瘍であるコルドーマ(chordoma)では、こうしたストレスを受けた線維芽細胞が濃密なマトリックスを形成して免疫細胞の浸入を阻み、治療効果を低下させます。膵臓がんや大腸がんなど他のがんでも同様の線維化・免疫乏しい環境が見られ、この生物学が一つの病気に固有のものではないことを示唆します。問題は、現在のストレス線維芽細胞やそれらの免疫遮断挙動を測定する方法が組織サンプルや複雑な分子検査に依存しており、反復が困難で腫瘍の重要な領域を見落としがちだという点です。
目に見えない生物学をAIに教える
研究者らは、術前の標準的なMRI画像や日常的なH&E病理スライドに、このストレス線維芽細胞による免疫バリアに関する視覚的手がかりがすでに含まれているかを検証しました。腫瘍のRNAシーケンシングから三つの数値的「参照スコア」を作成しました:線維芽細胞のストレスプログラムの活性度を表すもの、これらの細胞が免疫細胞にどれだけシグナルを送っているかを要約するもの、そして周囲の免疫および支持細胞集団の多様性を記述するものです。何千もの遺伝子を予測する代わりに、AIは画像のみからこれら三つの生物学的に意味あるスコアを予測するよう訓練されました。そのためにチームは二つの枝を組み合わせました:一つはMRIのテクスチャーや形状特徴を解析する枝、もう一つはデジタルスライド上の数千の小領域を走査し、線維化や免疫乏しい組織の専門家の記述に一致する領域に注目するための言語誘導型アテンション機構を用いる枝です。
画像とスライドを融合して信号を強化する
MRI、病理スライド、RNAデータ、経過観察が揃った126例のコルドーマ患者において、融合型AIモデルはMRIのみやスライドのみのモデルを上回りました。三つの分子スコアの予測はRNA由来の測定値と密接に一致し、病院やスキャナが異なっても良好に較正されたままでした。病理医が独立して線維化や免疫排除領域をマーキングしたとき、AIの「ホットスポット」はおおむね同じ領域に反応し、単に腫瘍サイズを追っているだけでなく実際の生物学を捉えていることを示唆しました。モデルは予後情報も捉えており、予測されたストレス線維芽細胞スコアおよびシグナルスコアが高いと生存率が低下し、周囲微小環境の多様性が高いと部分的に保護される関連が見られました。臨床の通常の因子にこれらAI由来のスコアを追加すると、時間経過に伴う高リスク・低リスク患者の識別能が向上しました。
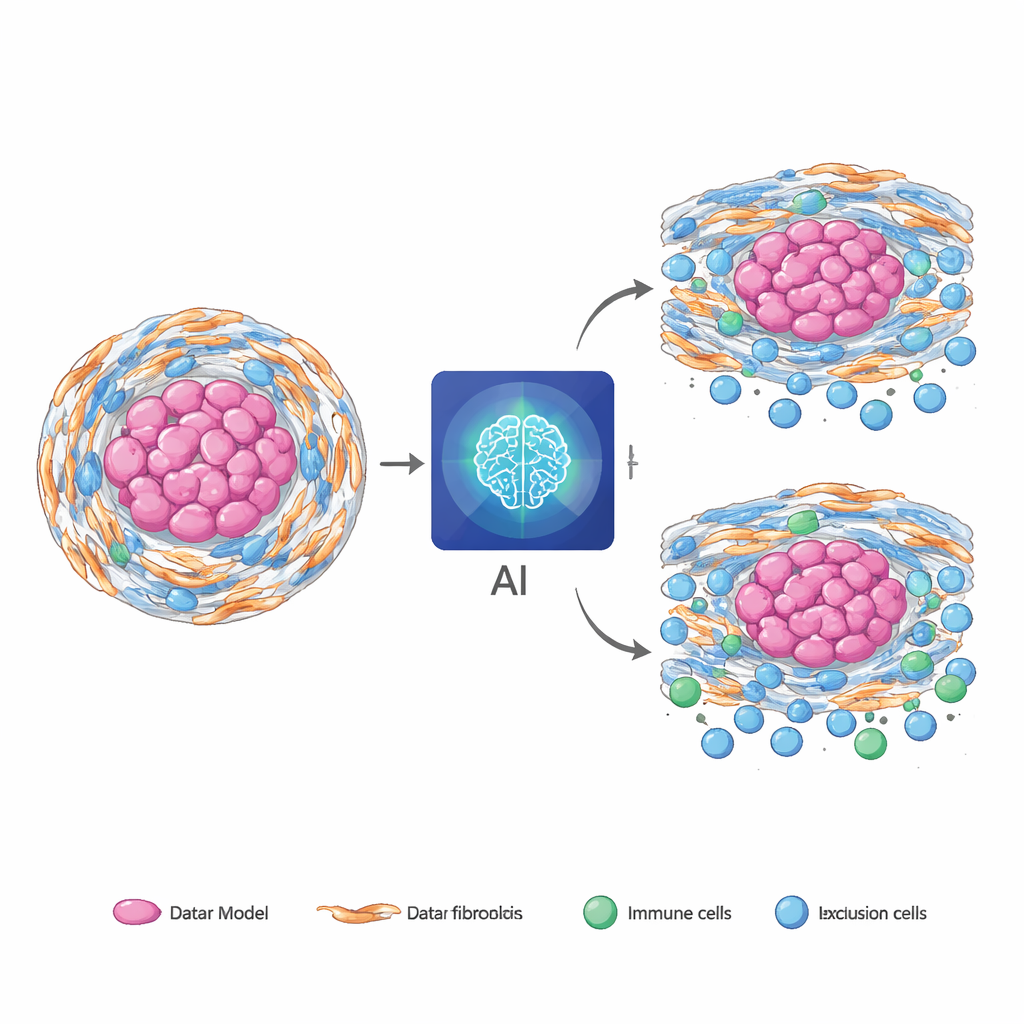
稀な腫瘍から一般的ながんへ
重要な試験は、コルドーマで完全に訓練されたモデルが他のより一般的ながんに対して「そのまま」使えるかどうかでした。再訓練せずに膵臓がん、胃がん、大腸がんの大規模公開データセットに適用したところ、スライドのみのモデルであっても画像ベースの予測と新たに算出したRNAベースのスコアとの間に意義ある整合性が示されました。これらのがんの一部では、AIスコアが標準的な臨床情報を超えて患者生存の予測を改善し、どの患者が化学療法の恩恵を受けやすいかの識別にも役立ちました。デジタル病理の整備が限られる場所でも導入しやすくするために、チームはフルのマルチモーダルモデルをMRIのみのバージョンへ蒸留し、多くの予測能力を保ちながら高速で計算資源を節約するモデルを作りました。
患者にとっての意義
まとめると、結果は日常的な医療画像が、通常は高価な分子検査を必要とするようなストレスを受けた支持細胞、免疫排除、微小環境の多様性に関する情報を静かに符号化しているという考えを支持します。現時点の研究は遡及的解析であり前向き検証が必要ですが、標準的なスキャンとスライドから侵襲を伴わずに敵対的な線維化免疫バリアを有する腫瘍を示唆し、追加検査や個別化治療の候補を案内し、多くのがん種に跨って患者に余分な負担をかけずに役立てられる未来への道筋を示しています。
引用: Zheng, BW., Xia, C., Tang, M. et al. Decoding the ERS–CAF immunoregulatory axis via multimodal AI and its pan-cancer prognostic and therapeutic predictive value. npj Digit. Med. 9, 199 (2026). https://doi.org/10.1038/s41746-026-02388-w
キーワード: 腫瘍微小環境, がん画像診断, 人工知能, 線維芽細胞, 免疫療法