Clear Sky Science · ja
知識強化型がん痛管理のためのLLM駆動協調フレームワーク
なぜ賢い疼痛ケアが重要なのか
がん性疼痛は単なる不快な副作用ではなく、患者の最期の数か月や数年を支配してしまい、睡眠や動作、さらには会話さえ困難にします。強力な鎮痛薬は存在しますが、安全かつ効果的に使うのは難しく、患者ごとにがんの種類や併存疾患、服用薬が異なるためです。本稿では、電子記録を精査し、最新のガイドラインに沿いながら、がん患者に対してより安全で個別化された疼痛管理プランの設計を支援することを目的とした、大規模言語モデル(LLM)ベースの新しい人工知能フレームワーク「OncoPainBot」について述べます。
日常的ながん医療における難問
がん性疼痛の原因は多岐にわたります。腫瘍による骨や神経の圧迫、手術、化学療法、放射線治療などです。進行がんの患者の最大70%が有意な疼痛を抱えていますが、十分な緩和はしばしば得られていません。医師はオピオイドや非オピオイド薬、補助療法を組み合わせつつ、特に肝機能や腎機能が脆弱な患者での有害事象に注意を払わなければなりません。現行の疼痛評価ツールは短いスケールや自由記述ノートに大きく依存しており、臨床者や施設ごとに差が出やすい。その結果、治療方針にばらつきが生じ、快適さを向上させる機会が見逃されることがあります。
医療テキストを実行可能な知見へ変える
ChatGPTやClaudeのようなLLMは、長く乱れた文書を読み要約する力があり、医療業務に魅力的です。しかし、一般的な「チャットボット」は詳細を作り出したり、薬剤の相互作用を見落としたり、最新ガイドラインを無視したりするため、がん性疼痛には安全ではありません。OncoPainBotは、主要ながん関連団体の疼痛ガイドラインから作成したキュレーション済みの知識ベースとLLMを組み合わせ、実臨床の役割を模した4つの協調する「エージェント」に作業を分割することで、これらの問題に対処します。1つのエージェントが電子記録から疼痛に関する主要事実を抽出し、別のエージェントが疼痛のタイプを推論し、3つ目が治療プランを作成し、4つ目が薬物相互作用や臓器機能、モニタリングの必要性に焦点を当てた安全性チェックを行います。
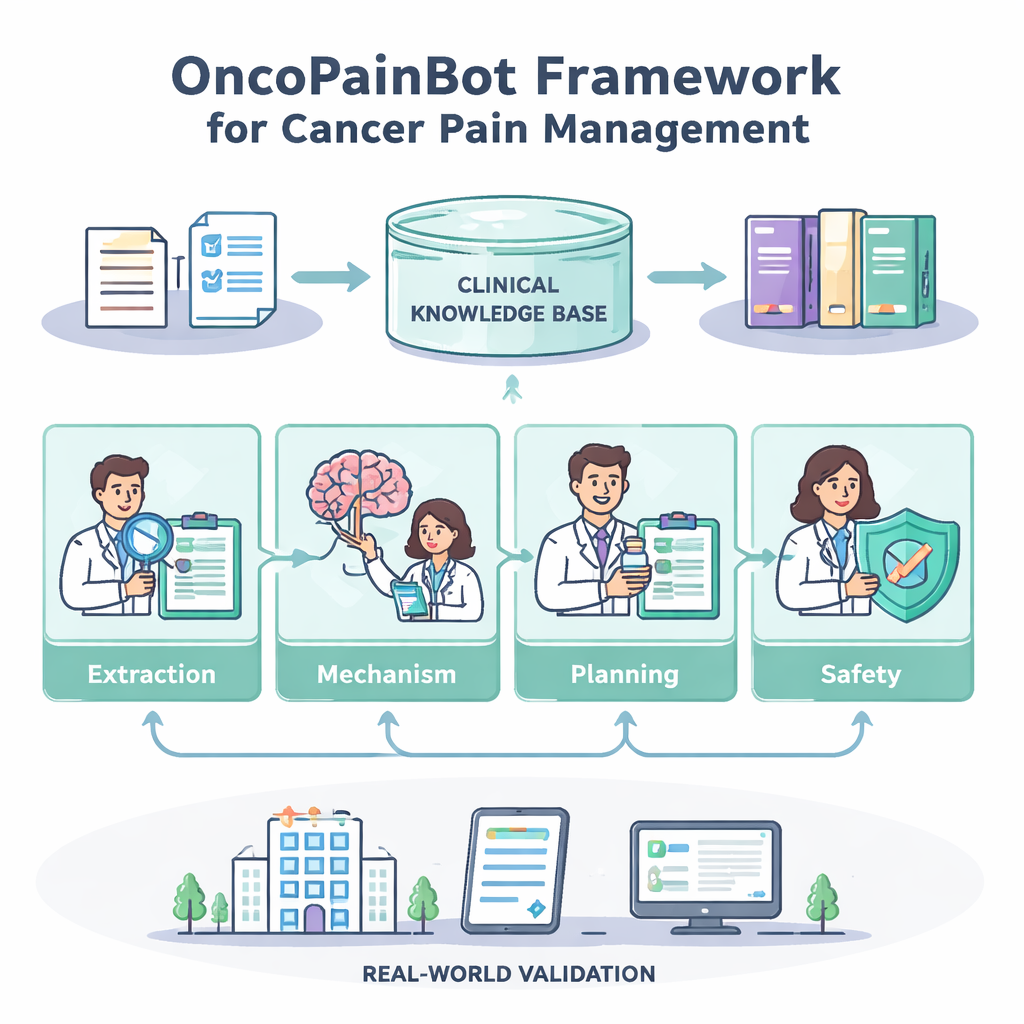
4つのエージェントチームの仕組み
Pain-Extractionエージェントは自由記述のノートを読み取り、疼痛の部位、痛みの強さ、何が悪化・緩和するか、既に試された薬剤などを構造化された情報に変換します。Pain-Mechanism Reasoningエージェントはその情報を用いて、疼痛が主に組織損傷によるものか、神経障害性か、あるいは両者の混合かを推定します。これは適切な薬剤選択の重要な手がかりです。次にTreatment-Planningエージェントが、retrieval-augmented generation(検索強化生成)と呼ばれる手法を使ってガイドラインベースの知識ベースを参照し、モデルが単なる記憶に頼るのではなく特定で最新の記述を取り込めるようにします。通常は世界保健機関(WHO)の「疼痛ステップ法(pain ladder)」を基軸とした段階的プランを提案し、開始用量、調整方法、突発的な痛みのためのレスキュードーズを含めます。最後にSafety-Checkエージェントが慎重な薬剤師のように振る舞い、投与量の問題や危険な併用、欠落している検査情報をスキャンし、データが不十分で確固たる推奨を裏付けられないケースを警告します。
システムの検証
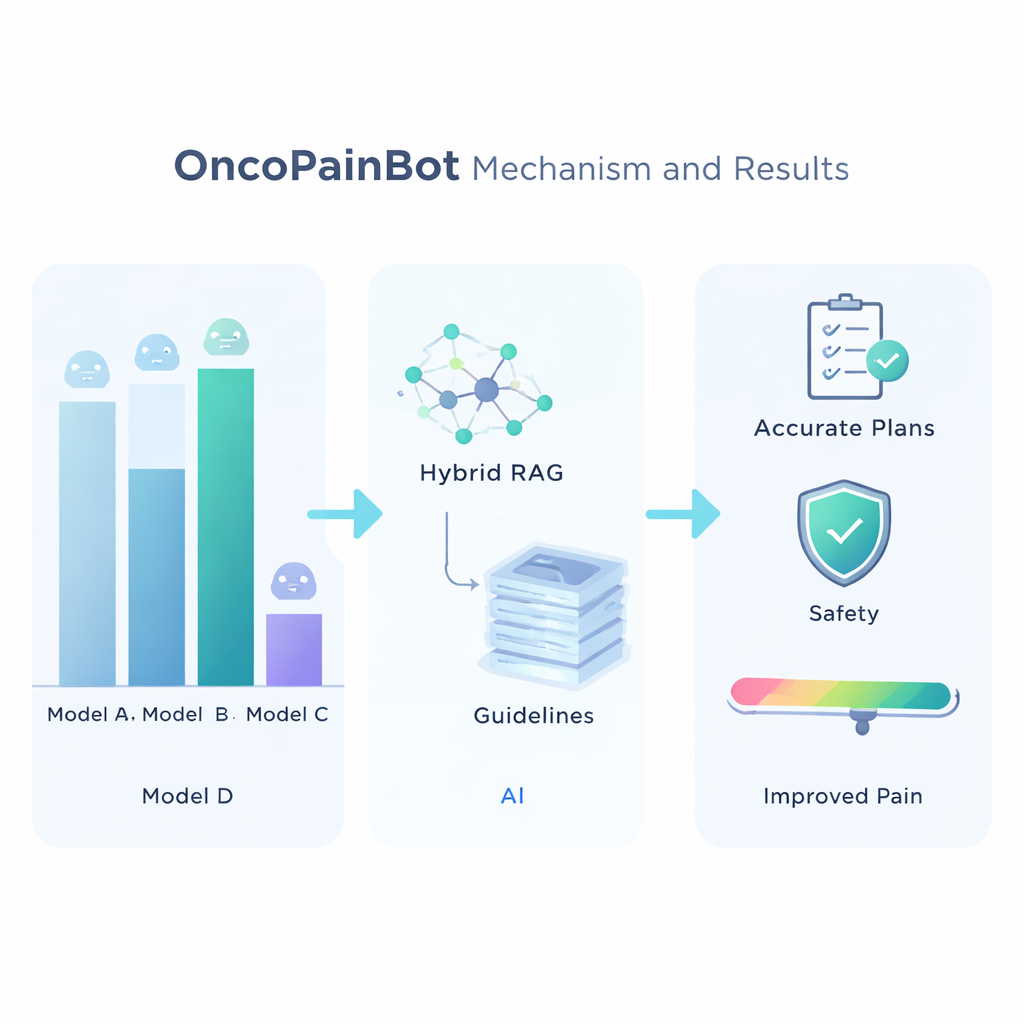
基盤となる言語モデルを選ぶために、研究者らは複数の医療系質問応答テストで7つの主要モデルを比較しました。Claude 4は最も正確である一方、最速ではなく、したがってOncoPainBotの「頭脳」として選ばれました。次にこの頭脳をガイドラインライブラリに接続するさまざまな方法を評価し、キーワード一致と深い意味検索を併用する「ハイブリッド」検索戦略が最も信頼できる回答をもたらすことが分かりました。この構成で、チームは中国の大規模病院から得た516件の実際のがん性疼痛記録にOncoPainBotを適用しました。システムの生成した報告は言語と内容の両面で臨床医の記録とよく一致し、疼痛治療の提案は実際の処方と約84%の割合で一致しました。重要なのは、不一致の多くは文書化されていないオピオイド耐性や複雑な臓器不全などの微妙で患者特有のニュアンスに起因しており、明らかに間違った薬剤選択によるものではなかった点です。
患者にとっての意義
がんとともに生きる患者にとって、OncoPainBotの約束は機械が治療を引き継ぐことではなく、ケアチームにより鋭く一貫したセカンドオピニオンを提供することです。本フレームワークは「クリニシャン・イン・ザ・ループ」ツールとして設計されており、ノート内に埋もれがちな疼痛特徴を浮かび上がらせ、ガイドラインに沿った選択肢を示し、安全性の懸念に注意を促しつつ、最終的な意思決定は医師に委ねます。著者らは本研究がまだ初期の後ろ向き解析段階にあり、単一施設でのみ検証されたことを強調しており、複数病院でのリアルタイム試験が依然として必要です。それでも、確かなエビデンスと透明な推論に基づいた慎重に設計されたAIは、がん性疼痛ケアの標準化、危険な投与ミスの減少、そして何よりも患者が苦しむ時間を減らし生活する時間を増やす可能性があることを示唆しています。
引用: Liu, H., Hu, Y., Li, D. et al. LLM-driven collaborative framework for knowledge-enhanced cancer pain assessment and management. npj Digit. Med. 9, 180 (2026). https://doi.org/10.1038/s41746-026-02362-6
キーワード: がん性疼痛管理, 臨床意思決定支援, 大規模言語モデル, オピオイド療法, 検索強化生成(RAG)