Clear Sky Science · ja
マルチオミクスと機械学習の統合により、MASLDからMASHへ進行する過程での細胞異質性と線維化制御ネットワークを体系的に解読
この肝疾患研究が重要な理由
肥満や2型糖尿病に関連する脂肪性肝疾患は、現在世界で最も一般的な肝疾患の一つになっています。多くの人では症状は軽度のままですが、かなりの割合で静かに悪化し、炎症や瘢痕化を伴う攻撃的な形態に進行し、肝硬変や肝がんにつながることがあります。医師は誰が進行するかを予測するのに苦労しており、生検なしでこの危険な段階を早期に見つけることは難しいのが現状です。本研究は最先端の“マルチオミクス”ツールと人工知能を用いて個々の肝細胞を詳細に解析し、新たに認識された免疫細胞タイプとシグナル経路を明らかにしており、これらが有害な瘢痕化を駆動している可能性を示すとともに、将来的に侵襲を伴わずに高リスク患者を示唆する血中マーカーを提案しています。

単純な脂肪沈着から危険な肝障害へ
研究者たちは、代謝異常関連の脂肪肝(MASLD、一般に脂肪肝と呼ばれる)から、より重篤な仲間である代謝異常関連の非アルコール性脂肪性肝炎(MASH)への移行に焦点を当てました。MASLDは非常に一般的で、特に肥満や糖尿病のある成人のうち3分の1以上に影響します。多くのMASLD患者は肝臓に脂肪がたまっているだけで大きな障害はありません。しかしMASHでは肝細胞が損傷を受け、炎症が高まり、瘢痕組織が形成されます。MASHの患者の約5人に1人から3人に1人が最終的に肝硬変や肝がんを発症します。現在の血液検査や画像検査では臓器内部でどのような微視的な細胞変化が進行しているかを正確に把握できないため、早期介入の機会を逃すことがよくあります。
肝臓を一細胞ずつ観察する
この問題に取り組むため、チームは公開データから複数の強力なデータタイプを組み合わせました。個々の肝細胞を対象とした50万以上のシングルセルRNAシーケンシングデータ、細胞の組織内位置を保持する空間トランスクリプトミクス、全生検からのバルク遺伝子発現プロファイル、そしてどのDNA領域が開いて活性化されているかを示すクロマチンアクセス性マップを収集しました。高度なソフトウェアを用いて細胞を肝細胞、免疫細胞、肝星細胞と呼ばれる支持細胞を含む7つの大きなタイプに分類しました。その後、健常肝、MASLD、初期および進行したMASHを比較し、疾患が悪化するにつれて細胞の構成やそれらのコミュニケーションネットワークがどのように変化するかをマップしました。
瘢痕を駆動する免疫細胞と支持細胞の協働
顕著なパターンが浮かび上がりました。単球やマクロファージとして知られる免疫細胞と肝星細胞が、初期段階よりもMASHで著しく増加し、病変組織の同じ領域に集積する傾向があったのです。さらに詳しく調べると、星細胞は休止状態から完全に活性化し平滑筋様になるものまで5つのサブタイプに細分されました。肝臓がMASLDからMASHに移行するにつれて、静かな星細胞は減少し、瘢痕を作る活性化星細胞が増加して、休止状態から線維化状態への明確な軌跡が描かれました。空間解析では、これらの活性化星細胞が濃縮したマクロファージの近くに位置しており、肝の瘢痕形成における密接な協力関係を示唆していました。
新たに注目されたマクロファージ型と線維化シグナル軸
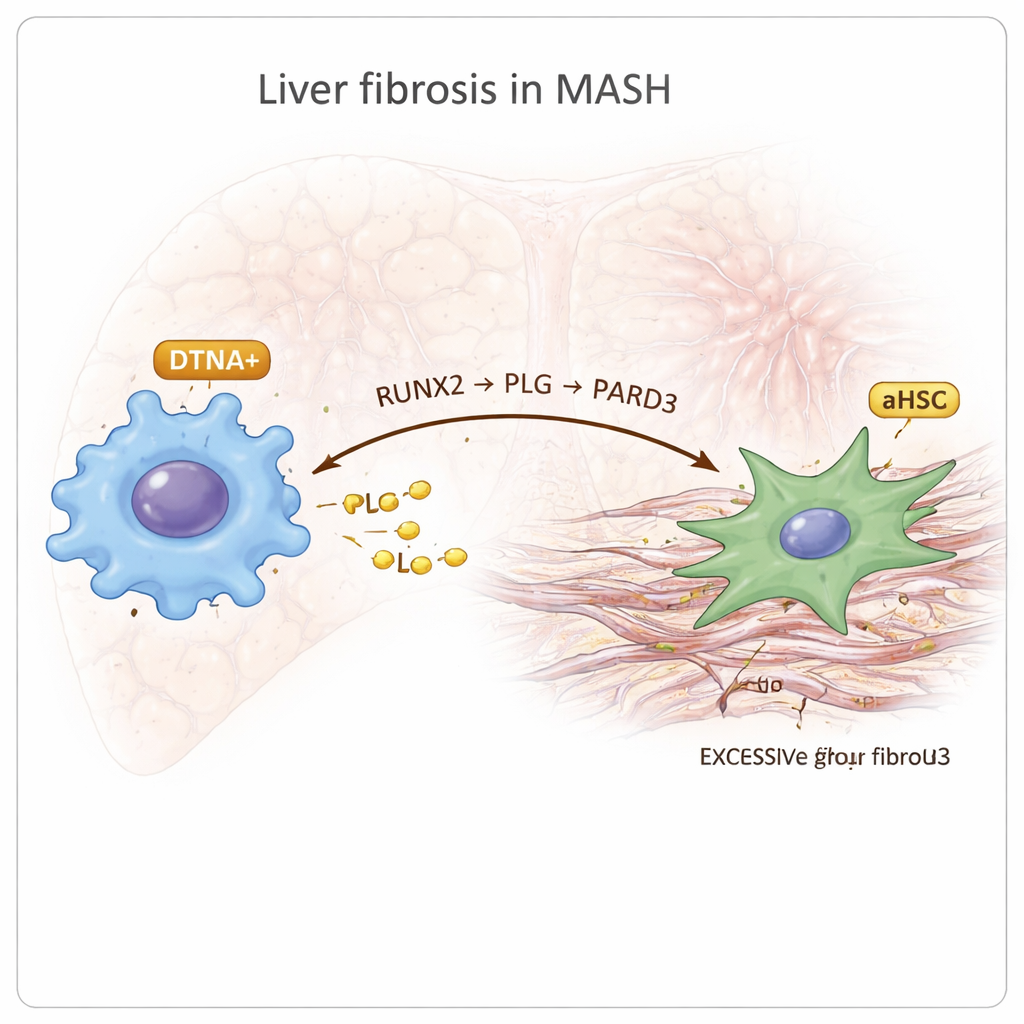
免疫細胞の中で、研究者たちはDTNAという遺伝子で特徴づけられる明確なマクロファージのサブグループを発見し、これは特にMASHで濃縮していました。これらのDTNA陽性マクロファージは、慢性的な炎症や組織再構築と関連することが多い所謂M2偏倚の特徴を示すとともに、低酸素および強い炎症シグナルの兆候を伴っていました。発生の“軌跡”を再構築することで、これらの細胞は肝内の在来クッパー細胞から生じると推定されました。制御ネットワーク解析は、これらのマクロファージにおけるマスター・スイッチとしてRUNX2という転写因子を示しました。さらに細胞間コミュニケーションのマッピングにより、DTNA陽性マクロファージが活性化星細胞とRUNX2–PLG–PARD3軸と呼ばれる連鎖を介して対話していることが示唆されました:RUNX2はマクロファージでタンパク質PLGの産生を高め、PLGはPARD3を発現する星細胞にシグナルを送り、この相互作用がより強い線維化と変化した血液凝固活性に結びついているのです。
細胞マップから考えられる検査と治療へ
これらの発見が患者に役立つかを確かめるため、研究チームはMASLDまたはMASHの患者から得られた大規模なバルク遺伝子発現データセットを用いて、113種類の機械学習モデルを訓練・検証しました。Elastic Netモデルが最も良好に機能し、複数の独立コホートにわたって一つの遺伝子が最も強い予測因子として浮かび上がりました:DTNAです。DTNAおよびその協調遺伝子(RUNX2を含む)の高い活性は、一貫して単純な脂肪肝よりもMASHの患者を特徴づけました。著者らは既存の薬剤データベースもスクリーニングし、新たに記述されたRUNX2–PLG–PARD3経路に作用する可能性のある複数の薬剤を見出しました。これらはリポジショニングの可能性を示唆しますが、実験室および臨床での検証がまだ必要です。
脂肪性肝疾患の患者にとっての意義
実務的には、本研究は肝臓の免疫細胞や支持細胞が一様ではなく、特定のマクロファージサブタイプと瘢痕形成を担う星細胞の協働が脂肪性肝を危険な瘢痕化へと駆動する主要な原動力である可能性を示しています。DTNAのようなマーカーを血中や組織で測定することが、将来的に侵襲的な生検に頼ることなく脂肪性肝患者のうち誰がMASHへ進行するリスクが高いかを医師が特定する手助けになるかもしれません。また、RUNX2–PLG–PARD3軸という特定のシグナル経路を、肝線維化を遅らせたり逆転させたりする薬剤の有望な標的として浮かび上がらせます。これらの知見はまだ研究段階でありさらに検証が必要ですが、複雑な細胞データを早期診断や標的治療の実用的なツールへとつなげるためのより明確な道筋を示しています。
引用: Wen, W., Liu, Z., Tan, W. et al. Integrating multi-omics and machine learning systematically deciphers cellular heterogeneity and fibrotic regulatory networks in the progression from MASLD to MASH. npj Digit. Med. 9, 167 (2026). https://doi.org/10.1038/s41746-026-02352-8
キーワード: 脂肪性肝疾患, MASH, マクロファージ, 肝線維症, マルチオミクス