Clear Sky Science · ja
WHO 2021 膠芽腫サブタイプ分類のための病理と放射線基盤モデルのマルチモーダル融合
脳腫瘍の二つの視点を結びつける
脳腫瘍と診断されたとき、医師は単に腫瘍があることを知るだけでなく、その正確な種類を把握する必要があります。腫瘍タイプによって手術、放射線、薬物治療への反応は大きく異なります。現在、この詳細な「サブタイピング」は遺伝学的検査が必要であり、時間がかかり費用が高く、どこでも利用できるわけではありません。本研究は、脳の画像(MRI)と腫瘍組織の顕微鏡画像の両方を解析する賢いコンピュータシステムが、これらのサブタイプを信頼性を持って推定できるかを探り、精密治療へのアクセスを迅速化・拡大する可能性を検討します。
腫瘍の種類が重要な理由
成人のびまん性膠腫は最も致命的な脳腫瘍の一つですが、標準的な画像や顕微鏡検査ではしばしば似た外見を示します。現行のガイドラインは、病勢や患者の生存期間に大きな差がある三つの遺伝学的サブタイプに分類しています。これらを区別する現在のゴールドスタンダードは腫瘍DNAの分子検査であり、追加の組織、専門的な検査設備、数日から数週間の待ち時間を要します。著者らは、日常的に取得されるMRIとデジタル病理スライドを組み合わせることで、遺伝学的検査の一部を代替しうる十分な情報を抽出できるかを問います。
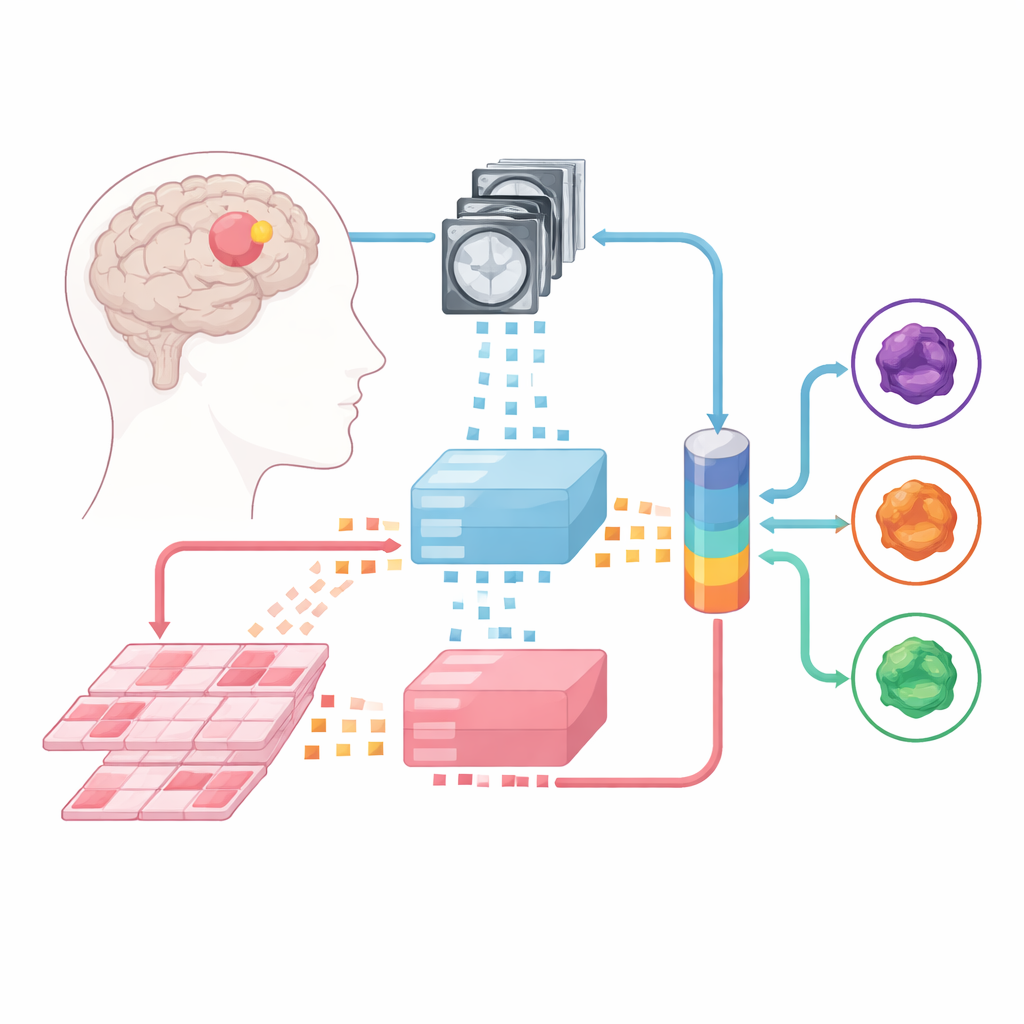
機械にスキャンとスライドの読み取りを教える
研究チームは、大規模「ファウンデーションモデル」—事前に膨大な医用画像で訓練された強力な画像解析器—を基盤に構築しました。一方は多様なパラメトリックMRIを処理し、もう一方は腫瘍組織から作成された高解像度の病理スライドを扱います。各症例は小さな画像パッチに分割され、ファウンデーションモデルがそれらを数値的な指紋へ変換します。これらの固定された“専門家”の上で、研究者らはMRIと病理の情報を組み合わせる方法を学ぶ三種類の融合モデルを訓練しました:レイトフュージョン(後融合)、アーリーフュージョン(前融合)、そして各情報源への依存度を動的に決定できる柔軟なミクスチャー・オブ・エキスパーツ(専門家混合)アーキテクチャです。
患者のマッチングがなくてもモダリティを混ぜる
こうしたマルチモーダル手法の現実的な障壁は、病院において全ての患者についてMRIと病理画像がきれいに対になった大規模データセットが稀であることです。著者らは完全に一致するデータに依存する代わりに、別々のコレクションを集めました:複数センターからの数百例のMRI、別のリソースからの数百例の病理、そして両方を持つ公的ながんプロジェクト由来の171名の小さなセット。訓練中、腫瘍が同じサブタイプであれば、ある人のMRIと別の人の病理スライドを組み合わせることが頻繁に行われました。驚くべきことに、そのような「アンペアード(非対)」データで訓練したモデルは、真の患者対で訓練したモデルと同等に機能し、単純に二つの単一モダリティモデルを平均した場合よりも明らかに優れていました。
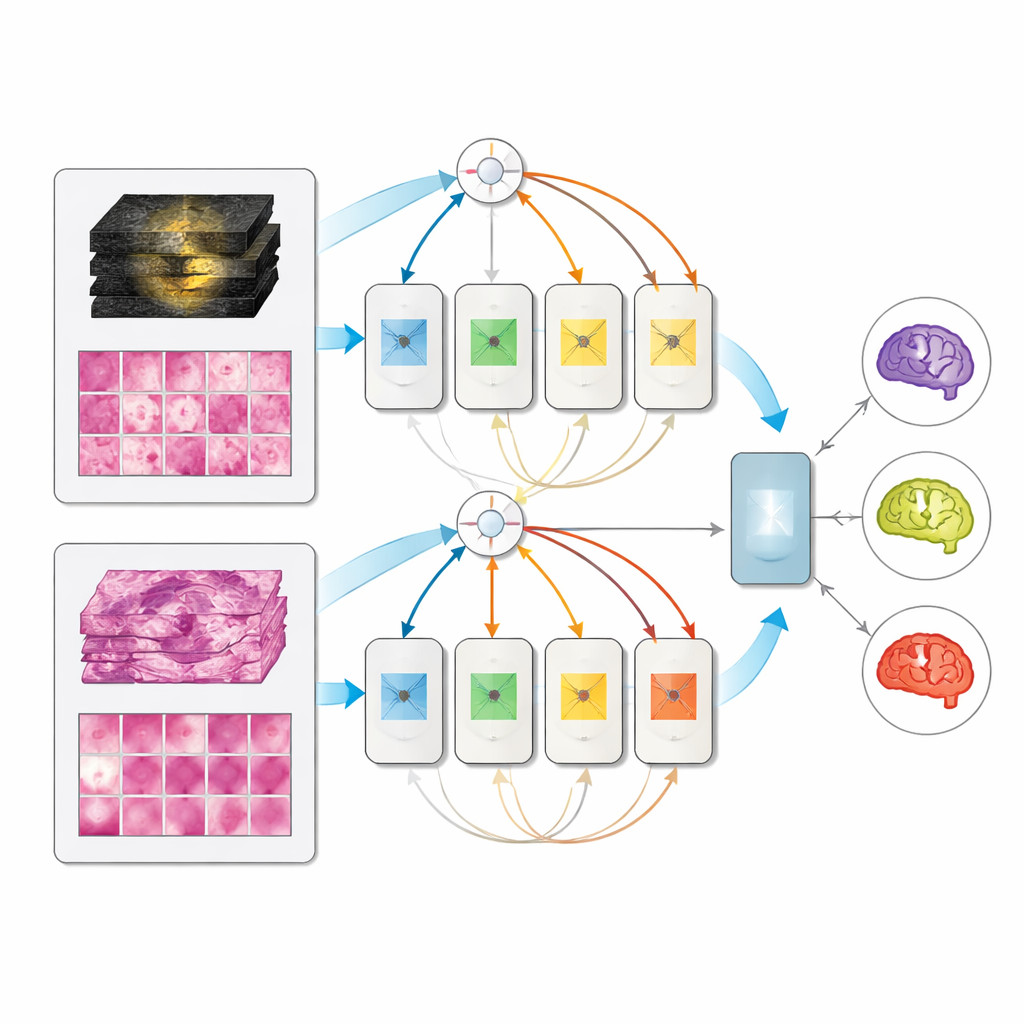
利用可能な情報に適応する単一モデル
完全に特徴付けられた171名の保持セットに対して、すべてのマルチモーダルモデルは単一入力モデルを上回り、ミクスチャー・オブ・エキスパーツ設計が最良の性能を示し、三つのサブタイプを区別する際に非常に高いスコアに達しました。注目すべきは、テスト時にMRIのみ、あるいは病理のみが提供された場合でも、マルチモーダルモデルは崩壊せず、専用の単一モダリティモデルとほぼ同等の性能を示した点です。これは、診療現場が状況に応じて—術前のスキャンのみ、術後の組織のみ、または両方—利用可能な情報を使う一つの統一システムを導入でき、各ケースごとに別個のツールを維持する必要がないことを意味します。
モデルが何を見ているかを可視化する
システムの決定に対する信頼を構築するため、研究者らはモデルが「どこを見るか」およびどの画像特徴が重要かを調べました。アテンションマップは、結合モデルがMRIと病理スライドの両方において腫瘍と周辺領域に幅広く焦点を分散させることを示し、より拡散した注目は正しい予測と一致する傾向がありました。学習された特徴の詳細解析は、既知の医学的手がかりと一致するパターンを明らかにしました。例えば、造影増強する腫瘍コアや歪んだ液体空間を強調するMRI特徴はより悪性の腫瘍を分離するのに寄与し、古典的な細胞形態やテクスチャを捉える病理特徴は特定の膠腫サブタイプの認識を助けました。一方で興味深いギャップも見られ、モデルは最も悪性の腫瘍の教科書的な兆候を強く符号化していないことがあり、その群を明確な有利なサブタイプの証拠がない限り“デフォルト”として扱うことが多いことを支持する結果も示されました。
患者にとっての意義
簡潔に言えば、本研究は脳スキャンと顕微鏡画像を組み合わせるAIシステムが、単一タイプの画像のみを見るシステムよりも脳腫瘍を正確に分類できること、そして両画像が同一患者から得られていない場合でも訓練可能であることを示しています。より大規模で多様な集団で追加検証されれば、こうしたツールは遺伝子検査が制限される環境でも、医師が早期かつ広範に腫瘍サブタイプを推定するのを助ける可能性があります。分子検査の代替ではないにせよ、迅速で低コストのガイドとして、外科医や腫瘍医に最も可能性の高い診断や適切な治療方針を示す手がかりを提供し得ます。
引用: Saueressig, C., Scholz, D., Raffler, P. et al. Multimodal fusion of pathology and radiology foundation models for WHO 2021 glioma subtyping. npj Precis. Onc. 10, 118 (2026). https://doi.org/10.1038/s41698-026-01366-5
キーワード: 膠腫サブタイピング, マルチモーダルイメージング, 人工知能, MRI と病理, 脳腫瘍診断