Clear Sky Science · ja
バルプロ酸はマクロファージに富む神経膠腫におけるマクロファージ介在性テモゾロミド耐性を逆転させる
体の“援助者”を脳腫瘍に対して利用する
神経膠腫と呼ばれる脳腫瘍は治療が非常に難しく、主な化学療法薬であるテモゾロミドに反応しなくなることが多いことが一因です。本研究は意外な味方を探ります:長年使われてきた抗けいれん薬、バルプロ酸です。腫瘍内外の特定の免疫細胞に寄り添わせることで、バルプロ酸はマクロファージに味方を変えさせ、マクロファージに富む腫瘍の患者で化学療法の効果を高める可能性があります。
標準治療がしばしば不十分な理由
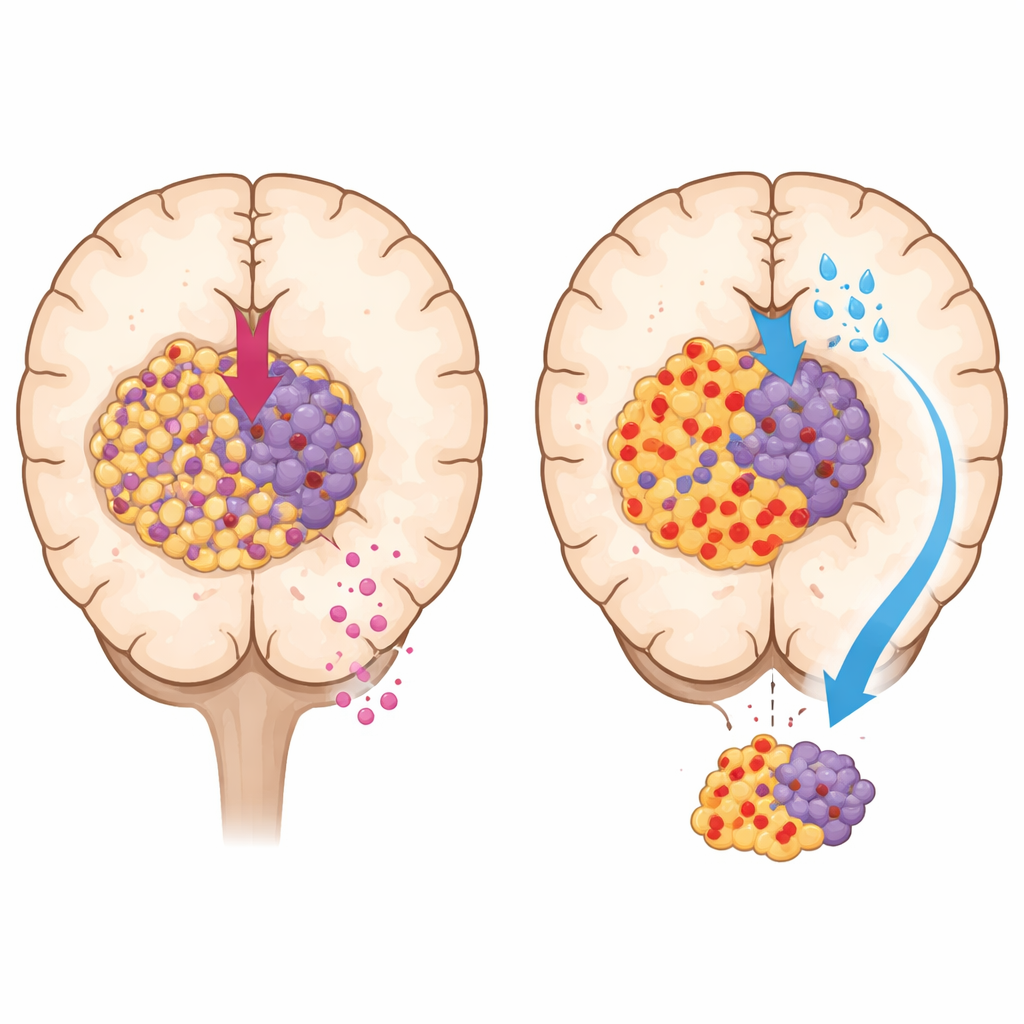
特に膠芽腫などの悪性度の高い神経膠腫では、手術と放射線療法の後に通常テモゾロミドが使われます。それでも多くの腫瘍は初めから薬に耐性だったり、時間とともに耐性を獲得したりします。これまでの研究は主にがん細胞内部、たとえばDNA損傷の修復のような変化を原因として挙げてきました。しかし、患者の腫瘍はがん細胞だけでなく、免疫細胞や支持細胞が入り組んだ複雑な周辺環境に置かれています。その中で最も多い細胞の一つがマクロファージで、これは本来腫瘍を攻撃することもあれば、状況によっては腫瘍の成長を静かに助けることもあります。
腫瘍の“ご近所”が治療を妨げるとき
研究者らは、複数の神経膠腫細胞株がシャーレ内とマウス体内でテモゾロミドにどう反応するかを比較しました。シャーレでは非常に感受性が高く見えた細胞株の一部が、腫瘍として成長すると頑固に薬に耐えるようになりました。重要な違いはがん細胞自身の遺伝的要因ではなく、周囲の環境でした。動物で治療に抵抗した腫瘍はマクロファージが大量に浸潤しており、特に炎症を和らげ腫瘍を保護しがちな“修復”型マクロファージが目立ちました。患者データと組織サンプルの解析でも、これらのマクロファージに富む神経膠腫は治療後に再発しやすく、予後不良と関連していることが示されました。
二つの抗けいれん薬、異なる免疫への影響
多くの神経膠腫患者はレビチラセタムやバルプロ酸といった抗けいれん薬を投与されます。両薬ともテモゾロミドの補助として提案されてきましたが、腫瘍の免疫環境に対する影響は十分に検証されていませんでした。本研究では、ヒト由来マクロファージを神経膠腫細胞由来のシグナルにさらし、その後レビチラセタムまたはバルプロ酸で処理しました。バルプロ酸は一貫してマクロファージをより攻撃的で腫瘍と戦う状態へと傾け、攻撃的なメッセンジャー分子の産生を高めました。一方、レビチラセタムはむしろマクロファージを保護的で腫瘍を支援する方向へ押しやる傾向がありました。
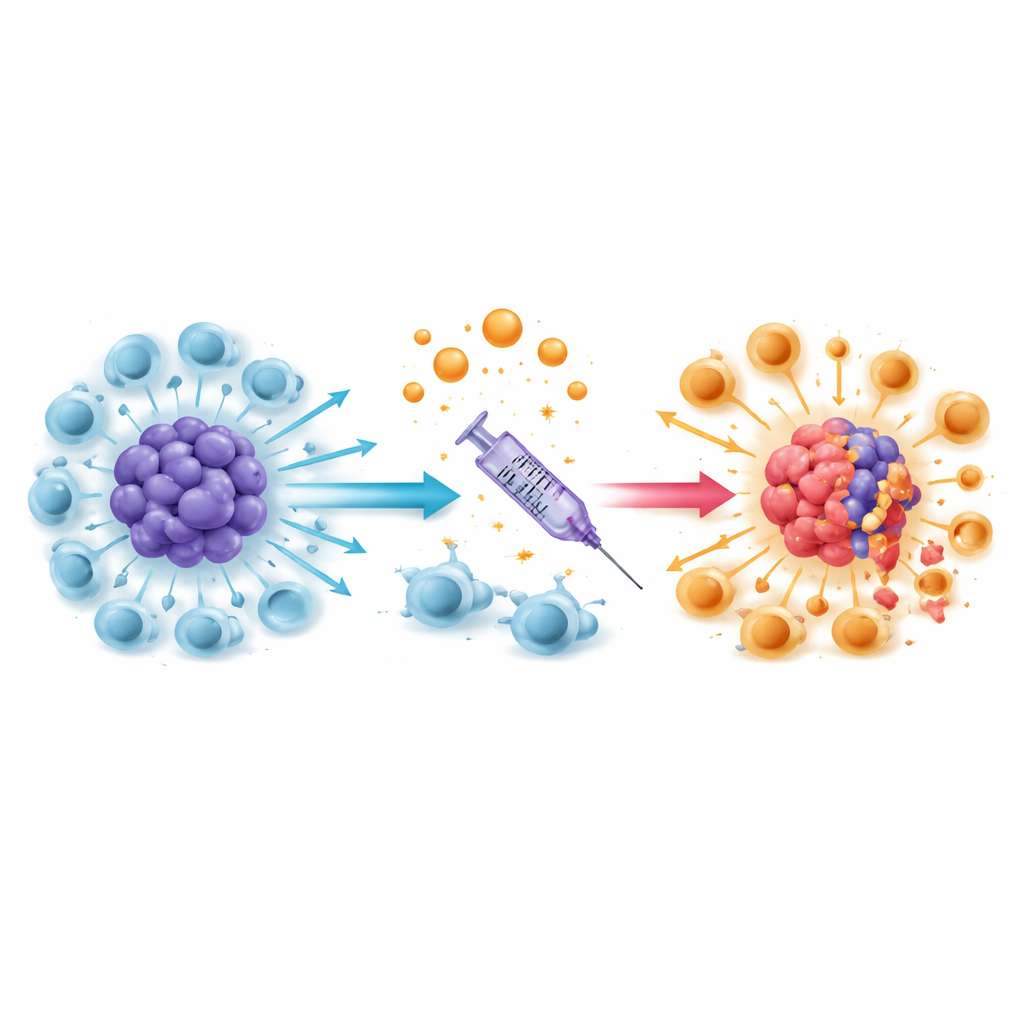
マクロファージを書き換えて薬剤感受性を回復する
次に研究者らは、これらの免疫変化が実際に腫瘍の化学療法反応を変えるかどうかを検討しました。神経膠腫細胞をマクロファージやマクロファージ由来の培養上清とともに培養すると、テモゾロミドの効果は低下し、動物や患者で見られる耐性を模倣しました。しかし、マクロファージが事前にバルプロ酸で処理されている場合は逆の結果となり、その分泌物は神経膠腫細胞をテモゾロミドに対してより脆弱にし、いくつかの耐性関連因子の産生を減らしました。マクロファージに富む神経膠腫のマウスモデルでは、バルプロ酸とテモゾロミドを併用すると、テモゾロミド単独やテモゾロミド+レビチラセタムよりも腫瘍成長が遅くなり生存が延びました。バルプロ酸処置マウスの腫瘍には、攻撃的なマクロファージが増え、保護的なタイプは減っていました。
より個別化された治療選択に向けて
総じて、この結果は、マクロファージに占められた神経膠腫に対してバルプロ酸が二重の役割を果たしうることを示唆します:けいれんを抑えるだけでなく、腫瘍を取り巻く免疫細胞を再武装して化学療法が本来の効果を発揮できるようにするのです。レビチラセタムは、耐性が腫瘍の内部のDNA修復経路によって主に駆動されるケースでは依然として有用である可能性があります。本研究は標準治療を直ちに変えるものではありませんが、将来の臨床試験に向けた明確で検証可能なアイデアを提供します:腫瘍の生物学に応じて抗けいれん薬を選び、マクロファージが優勢な場合にはバルプロ酸を用いて、腫瘍の“かつての援助者”をその破壊の味方に変えるという考えです。
引用: Ni, X., Chen, W., Xu, P. et al. Valproic acid reverses macrophage-mediated temozolomide resistance in macrophage-rich gliomas. npj Precis. Onc. 10, 120 (2026). https://doi.org/10.1038/s41698-026-01325-0
キーワード: 膠芽腫, テモゾロミド耐性, 腫瘍微小環境, マクロファージ, バルプロ酸