Clear Sky Science · ja
次の層:構造を保持し注意機構に導かれた学習で局所パッチから大域文脈認識へ基盤モデルを強化する計算病理学
がんスライドを「読む」ようにコンピュータを教える
病理医が顕微鏡でがん生検を観察する際、彼らは個々の細胞だけでなく、パターンや近傍、腫瘍・免疫細胞・正常組織の配置の仕方を見ている。現在のデジタル病理向けAIシステムは小さな画像パッチのディテールを見つけるのが得意だが、このより大きな文脈を見落としがちだ。本研究はEAGLE-Netを紹介する。これは、局所の詳細とスライド上の組織全体の配置の両方に注意を払うことで、コンピュータが病理専門家のようにがんスライドを把握できるようにする新しいAIアプローチである。

腫瘍組織の配置が重要な理由
腫瘍はがん細胞の塊以上の存在だ。血管や免疫細胞、結合組織、瘢痕や細胞死の領域に囲まれた賑やかな近傍に存在する。これらの要素の配置――距離や境界、混合の仕方――は、がんの侵襲性や患者の治療反応を示す手がかりになる。従来の病理AIは通常、全スライド画像を何千もの小タイルに切り分け、それらをほぼ孤立に解析する。次に全タイルの情報をプーリングして診断や予後を推定するが、この戦略はタイル同士が空間的にどのように関連しているかを無視しがちで、予測精度が落ちたり、AIのヒートマップが散在して解釈しにくくなったりする。
大局を捉える新しい方法
EAGLE-Netは、局所の詳細と大域的な構造の間のギャップを埋めるよう設計されている。まず、小さなスライドパッチから豊富な視覚特徴を抽出することを既に学んでいる強力な「基盤モデル」を出発点とする。その上に、各パッチがスライド上のどこから来たかを符号化する新しいモジュールを追加し、組織の真の幾何学を歪んだグリッドに押し込めるのではなく保持する。マルチスケールフィルタを用いて、EAGLE-Netは細胞レベルの微細な変化から腫瘍境界や周囲の間質のようなより広い組織構造に跨るパターンを学習する。次に注意機構、すなわち重要度スコアを割り当てる仕組みを使って、診断や生存予測に最も関連するパッチや近傍に注目する。
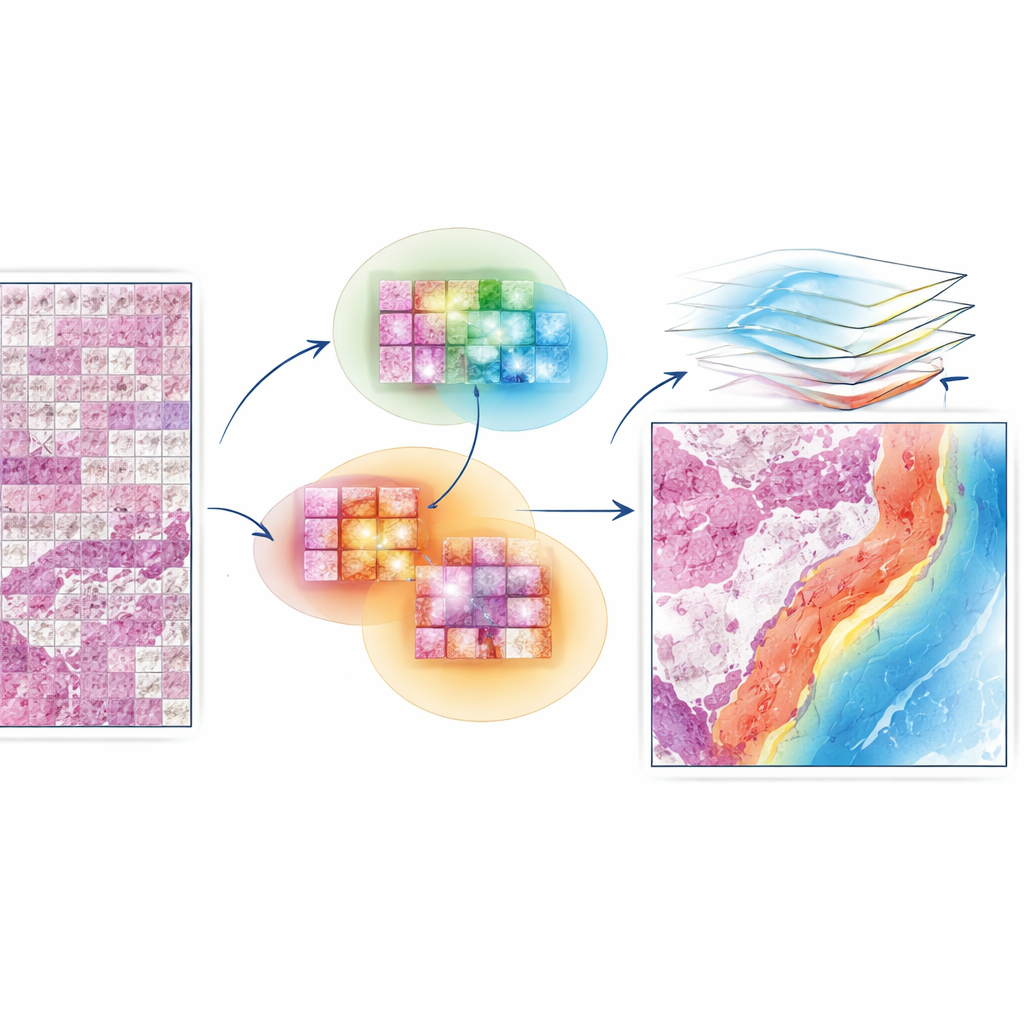
点ではなく近傍から学ばせる
EAGLE-Netの重要な革新は、ネットワークに最も重要なタイルだけでなくその近傍も重視させる学習法にある。訓練中、この手法はモデルが最も有益と判断したタイルを繰り返し特定し、さらに小さな半径内の周辺タイルを同じ意味のある領域の一部として考慮するよう促す。この「近傍認識」学習は、モデルが病理医が見るような腫瘍前線、免疫クラスター、その他の微小環境に沿った滑らかで連続した注意領域を形成するよう促す。同時に、訓練過程の追加項は背景や空白領域を無視するようモデルを積極的に押し、散在するアーティファクトや余白に誤って強調が入るリスクを低減する。
多くのがん種でその有用性を実証
研究者らは、肺、腎、胃、子宮、甲状腺、大腸、前立腺腫瘍を含む10種類のがんにわたる約15,000枚の全スライド画像でEAGLE-Netをテストした。評価対象は主に生存期間の予測と腫瘍の種類やグレードの分類の2つのタスクである。ほとんどのがんコホートでEAGLE-Netは複数の主要な注意ベース手法と同等かそれ以上の性能を示し、生存予測スコアや分類精度を数ポイント向上させることが多く、集団規模では意味のある改善であった。また、3種類の異なる基盤モデルと組み合わせても強い性能を示し、その設計が単一の特徴抽出器に依存しない柔軟性を持つことを示した。
モデルの判断の中身を可視化する
単なる精度以上に、チームはEAGLE-Netがスライド上のどこを「見ている」かを詳しく解析した。他の手法と比較して、その注意マップは腫瘍境界に沿ってより滑らかで一貫した領域を形成し、浸潤縁、壊死のポケット、免疫細胞のクラスターを捉えていた。専門家が描いた腫瘍マスクとの定量的比較では、EAGLE-Netの強調領域は真の腫瘍との重なりがより大きく、正常組織への誤検出が少なく、複雑な腫瘍形状をより忠実に再現した。また、モデルは腫瘍、壊死、免疫区画に注意を多く割き、正常肺組織や血管にはあまり割かない傾向を示し、予後評価時に病理医が優先する点を反映していた。
将来のがん医療にとっての意義
実務的には、EAGLE-Netは既存の病理AIの上に空間認識と近傍推論を追加することで、性能と解釈可能性の両方を改善できることを示している。スライドを切り離されたタイルの集合として扱う代わりに、この手法は患者転帰に関わる生物学的に意味のあるニッチ――腫瘍境界、免疫に富む領域、侵襲パターン――を認識することを学ぶ。多様な基盤モデルで動作し、ピクセル単位の手作業ラベルを必要としないため、EAGLE-Netは大規模なデジタルスライドのアーカイブへ広く適用できる可能性がある。さらなる検証と臨床ワークフローへの統合が進めば、この種のシステムは病理医による患者層別化をより精密に支援し、新たな組織ベースのバイオマーカーを発見し、最終的にはより個別化されたがん治療の指針となることが期待される。
引用: Waqas, M., Bandyopadhyay, R., Showkatian, E. et al. The next layer: augmenting foundation models with structure-preserving and attention-guided learning for local patches to global context awareness in computational pathology. npj Precis. Onc. 10, 109 (2026). https://doi.org/10.1038/s41698-026-01312-5
キーワード: 計算病理学, がん予後, デジタル病理AI, 腫瘍微小環境, EAGLE-Net