Clear Sky Science · ja
複数のがん種にまたがる組織病理学全スライド画像における自動腫瘍セグメンテーションの一般化
がん医療にとってなぜ重要か
がんの診断は依然として、染色した組織標本をガラススライドで顕微鏡観察する専門家の手作業に頼っています。症例数の増加と病理医不足によってこの作業は時間を要するものになっています。本研究は単純だが強力な疑問を投げかけます:多くの異なる腫瘍タイプに対して、個別にツールを作るのではなく、1つの人工知能システムがデジタル顕微鏡画像上で腫瘍領域を確実に見つけられるか。もし可能なら、診療負荷の軽減、診断の迅速化、そしてデータが乏しい希少ながんに対しても高度な解析を拡張できる可能性があります。
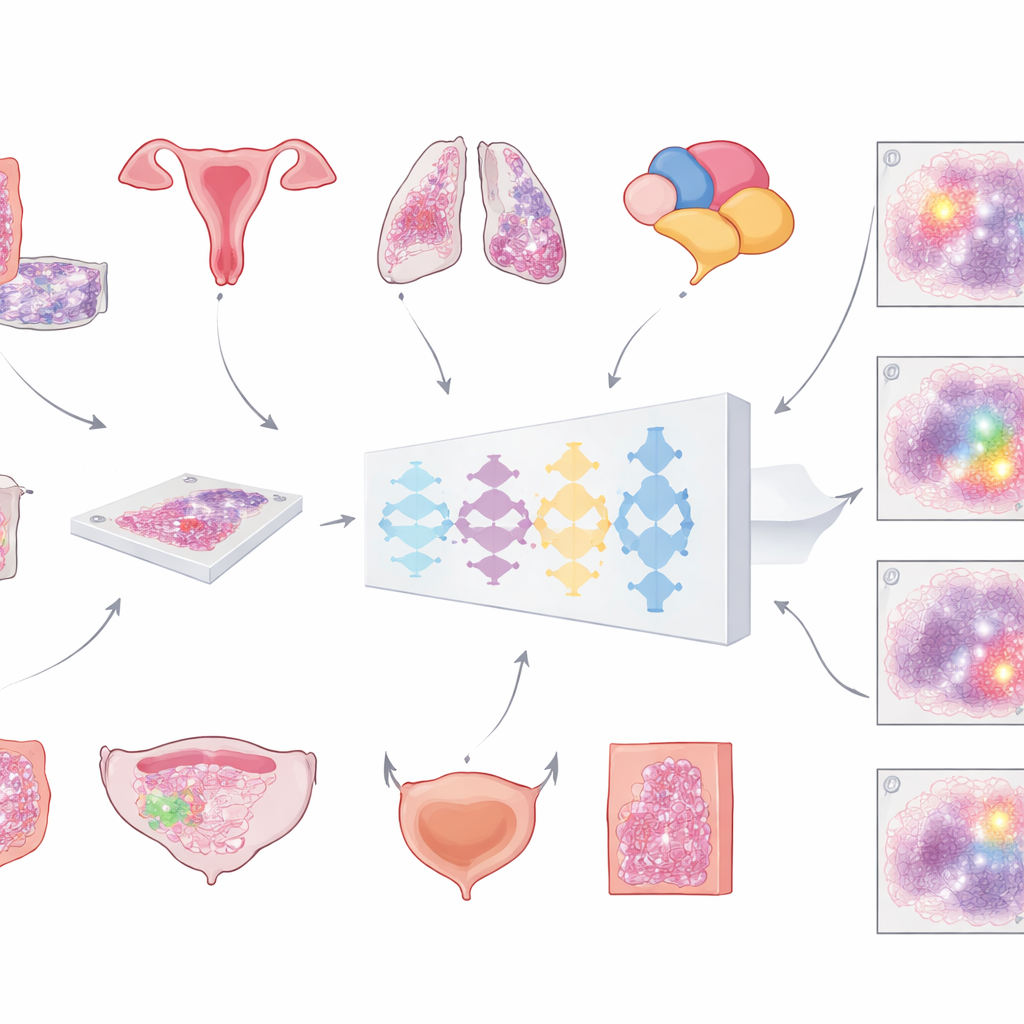
ガラススライドからデジタル支援へ
現代の病院では、顕微鏡スライドをスキャンして腫瘍の巨大で高詳細な「全スライド画像」を作成する流れが進んでいます。コンピュータ解析の最初の重要なステップは、腫瘍組織を正常細胞、脂肪、空白ガラス、アーチファクトなどのそれ以外のものから分離することです。これまでのほとんどの自動化ツールは単一のがん種で訓練されており、適用範囲が限られていました。本研究チームは、日常的に用いられるヘマトキシリン・エオシン(H&E)染色スライド上で、複数の一般的ながんにまたがって腫瘍領域を検出できる単一の汎用モデルを構築することを目指しました。彼らのビジョンは、毎回設計をやり直すことなく多様な診断ワークフローに組み込める汎用ツールを作ることでした。
一つのモデルで多くのがんを見る
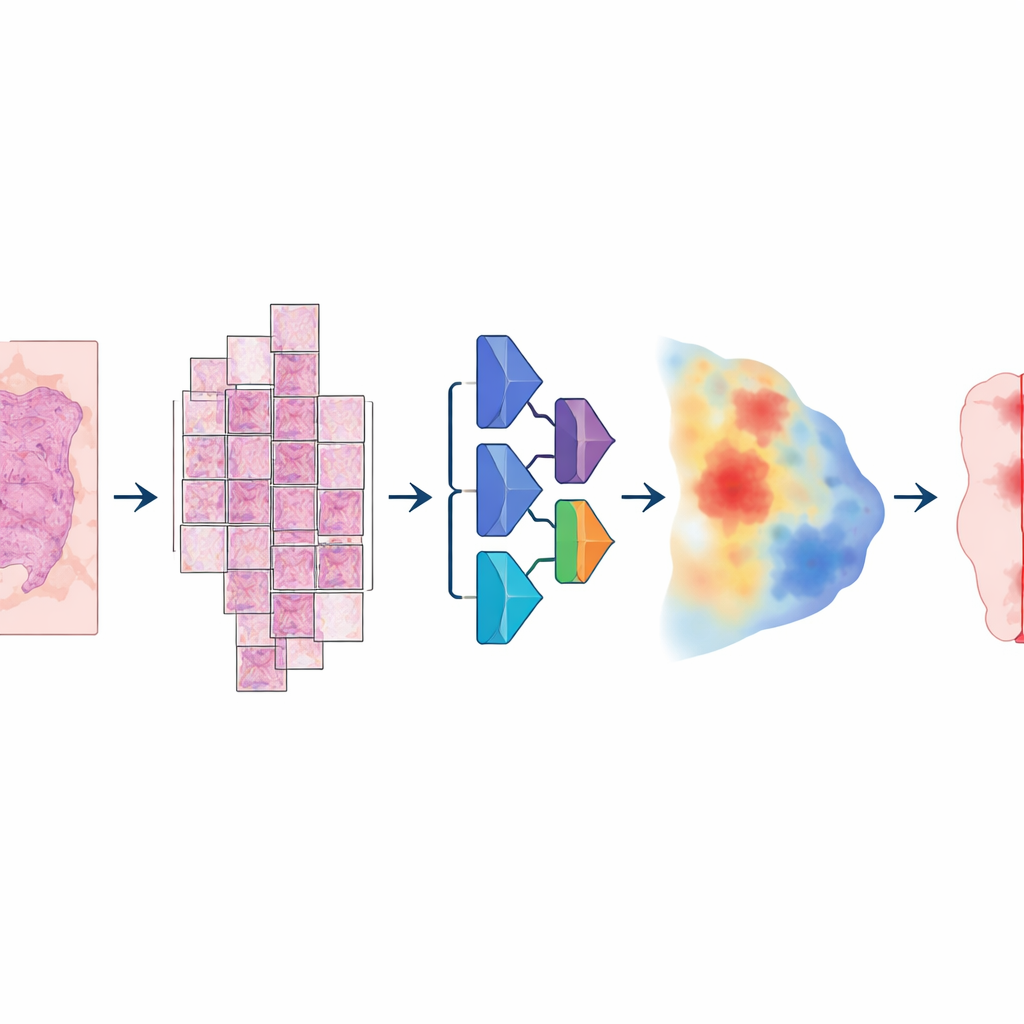
このモデルを構築するため、研究者らは異例に大きく多様なデジタルスライド集を集めました:結腸直腸がん、子宮内膜がん、肺がん、前立腺がんの4,000人以上の患者から得られた20,000枚超の全スライド画像です。すべてのサンプルは標準的なホルマリン固定パラフィン包埋組織(FFPE)で、2種類の高解像度スライドスキャナーでスキャンされました。病理医が各スライドで腫瘍領域を丁寧に輪郭描画し、コンピュータが学習するための「ゴールドスタンダード」を提供しました。モデルは多段階のパイプラインに従います:巨大な画像を大きな重なりのあるタイルに分割し、各ピクセルが腫瘍である確率を推定する深層ニューラルネットワークに通し、それを滑らかなマップに再構成して最終的に腫瘍/非腫瘍のクリーンなマスクに変換します。
システムをテストする
重要なのは、チームが訓練性能で止まらなかった点です。彼らは同じモデルを、訓練に使われなかった乳がんや膀胱がんを含む6つのがん種にわたる3,000人以上の追加患者、および複数の病院とスキャナー由来のスライドで検証しました。精度は主に重なりの標準スコア(ダイス係数)で評価され、これはコンピュータの腫瘍輪郭が病理医の輪郭と完全に一致すると100%になります。結腸直腸、子宮内膜、肺、前立腺、乳がんの大きく連続した腫瘍サンプルでは、平均の重なりが80%を超え、しばしば90%に達しました。世界中の多くの研究室とスキャナーから集められたThe Cancer Genome Atlasの大規模外部コレクションでも性能は再び80%を上回り、モデルが元の施設を越えて一般化していることを示唆しました。
苦戦する場面と比較
主な弱点は、非常に小さく断片化した組織片を生じる処置で採取される早期膀胱がんに現れました。こうしたケースでは、モデルは腫瘍をまったくマークできないことが多く、特に腫瘍領域が非常に小さい場合に顕著でした。しかし、腫瘍を検出できた場合の病理医の輪郭との重なりは高く、最終しきい値を簡単に調整することで結果が改善することから、基礎となるネットワークはパターンを認識している一方で後処理がやや厳格すぎたことが示唆されます。研究者らはまた、各がん種ごとに単独で訓練した4つの「専門家」モデルも構築し、これらはいずれも自分の領域で汎用モデルを意味ある形で上回ることはありませんでした。対照的に、専門家モデルは他のがん種に適用すると大きく性能が低下することが多かったのに対し、汎用モデルは堅牢性を維持しました。ユーザーのヒントを必要とする一般的な医療用セグメンテーションツールと比較しても、新しいモデルは通常同等かそれ以上の性能を示し、かつ完全自動である点が優れています。
患者と医師にとっての意味
非専門家にとっての主要な結論は、よく設計された1つのAIシステムが、複数の主要ながん種にわたってデジタルスライド上の腫瘍組織を信頼してハイライトできるということです。各疾患やスキャナー向けにカスタム版を用意する必要はありません。これは病理医の代替ではなく、むしろ腫瘍の可能性が高い領域を事前に示し、一貫した測定を支え、専門家が最も難しい症例に集中できるようにする補助となります。現行バージョンはまだ非常に小さいあるいは早期の腫瘍、特に断片化した膀胱検体やその他の生検様組織を見落とすことがあり、最も微細ながんの痕跡を検出する用途には未だ適していません。それでも、この研究は現実世界の条件下で広範な「パンキャンサー」腫瘍セグメンテーションが実現可能であり、がんのグレード評価、治療反応予測、精密治療の指針となる将来の自動化ツールの堅牢な第一歩になり得ることを示しています。
引用: Skrede, OJ., Pradhan, M., Isaksen, M.X. et al. Generalisation of automatic tumour segmentation in histopathological whole-slide images across multiple cancer types. npj Precis. Onc. 10, 107 (2026). https://doi.org/10.1038/s41698-026-01311-6
キーワード: デジタル病理学, ディープラーニング, 腫瘍セグメンテーション, 全スライドイメージング, パンキャンサーモデル