Clear Sky Science · ja
MicroRNA-29bの喪失がDNMT3bを介したSTINGのダウンレギュレーションを促進し、KRAS変異大腸癌における放射線療法誘発抗腫瘍免疫を減弱させる
この研究が重要な理由
直腸癌や結腸癌の多くの患者にとって、放射線は手術前の治療の重要な一部です。しかし、腫瘍がほとんど縮小しないことがあり、癌が再発したり転移したりすることがよくあります。本研究は大腸癌でよく見られる遺伝的変化、KRAS変異に着目し、これらの腫瘍が放射線療法や新しい免疫療法に抵抗する理由を解き明かすとともに、体の免疫を再活性化するための戦略を提案します。
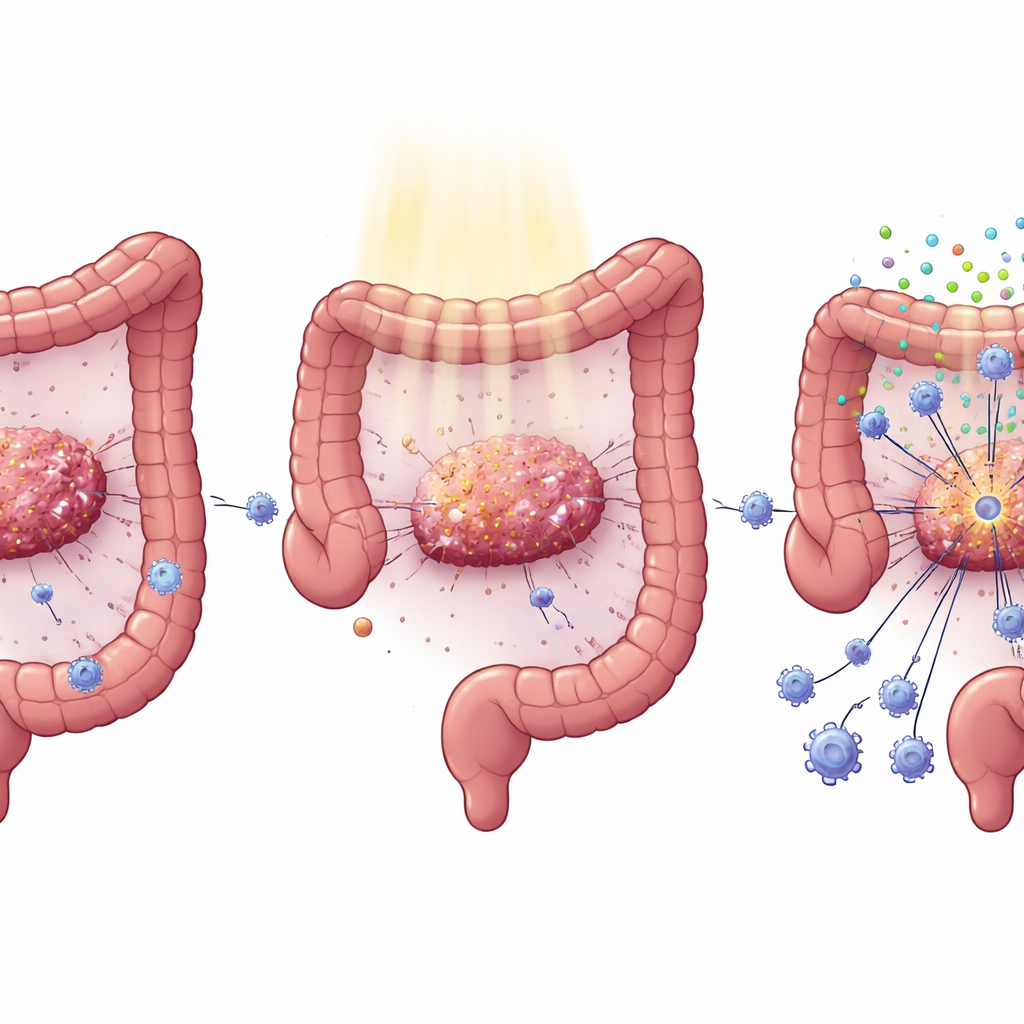
腫瘍を免疫攻撃から隠す一般的な変異
大腸癌ではKRAS遺伝子の変異が頻繁に見られ、腫瘍の増殖や転移を促す主要な因子です。臨床ではKRAS変異腫瘍が分子標的薬や放射線療法に対して反応が悪いことがすでに知られていました。大規模ながんデータベースの解析や患者試料の検討により、KRAS変異を持つ腫瘍は癌細胞を殺すCD8陽性T細胞が少なく、免疫を活性化するインターフェロンシグナルが弱いことが明らかになりました。直腸癌手術前に標準的な化学放射線療法を受けた患者では、野生型KRASの人々は治療後に腫瘍内のCD8陽性T細胞が大幅に増加しましたが、KRAS変異の患者では増加が乏しく、この差が予後の違いを説明する一因となっています。
がん細胞内の欠けた警報システム
放射線療法は腫瘍DNAを損傷するだけでなく、フレアのように働いて癌細胞からDNA断片を放出させ、cGAS–STINGと呼ばれる内部の警報経路を刺激します。STINGが活性化されると、細胞はI型インターフェロンやその他のシグナルを産生し、T細胞や樹状細胞などの免疫細胞を呼び寄せて活性化します。研究者らは、KRAS変異を導入した大腸癌細胞ではこの警報システムが鈍くなっていることを示しました:放射線後、これらの細胞は著しく少ないインターフェロンや関連分子しか産生しませんでした。マウスでは腫瘍のKRASを沈黙させるとSTINGレベルが回復し、インターフェロンシグナルが強まり、CD4およびCD8陽性T細胞の増加、制御性T細胞の減少、腫瘍制御の強化が見られました。これは照射された腫瘍だけでなく、非照射の遠隔“アブスコーパル”腫瘍にも及びました。
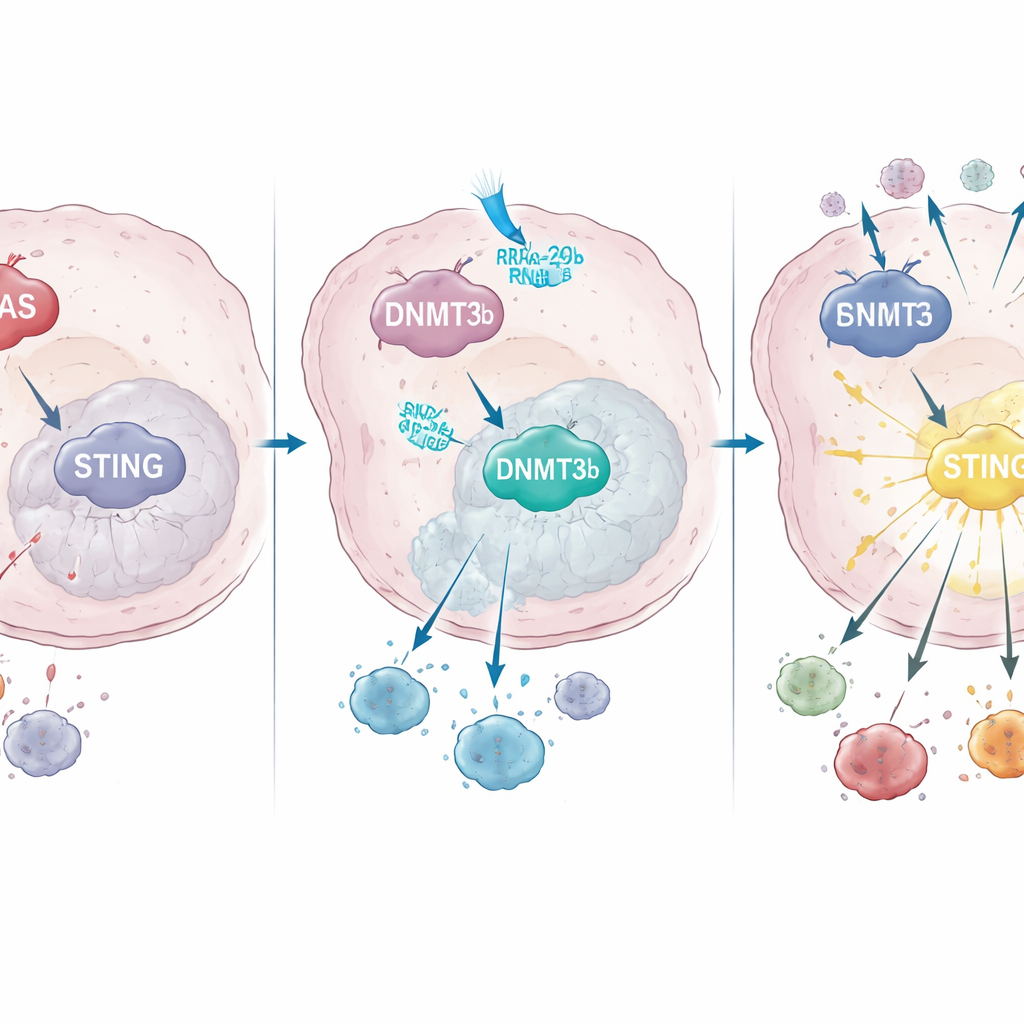
KRASが遺伝子制御を書き換えSTINGを遮断する仕組み
さらに解析を進めると、変異KRASはDNMT3bと呼ばれるDNA修飾酵素の活性を高めることが分かりました。DNMT3bは特定のDNA領域にメチル基を付加して近傍の遺伝子をオフにします。がん細胞株および患者試料の両方で、高いDNMT3bは低いSTINGと相関していました。STINGプロモーターの重要な領域(遺伝子の“オンスイッチ”)はKRAS変異腫瘍で強くメチル化されていましたが、野生型KRASの腫瘍ではそうではありませんでした。化学放射線療法後にSTINGを上方制御できた患者は腫瘍内のCD8陽性T細胞浸潤が多く、予後も良好であり、この経路が治療成功にとっていかに重要かを裏付けています。
警報を再起動できる小さなRNA
研究者らは次に、なぜDNMT3bがKRAS変異で増加するのかを調べました。microRNAシーケンスを用いて、通常はDNMT3bを抑制する小さな調節RNA、microRNA‑29b‑3pが同定され、変異KRASによって強く抑制されていることが分かりました。このmicroRNAをKRAS変異細胞に戻すとDNMT3bが低下し、STINGが回復し、放射線後のインターフェロン産生が増強されました。逆にこのmicroRNAを阻害すると反対の効果が出ました。腫瘍試料では、KRAS変異患者は低いmicroRNA‑29b‑3p、高いDNMT3b、低いSTINGの傾向があり、microRNA‑29b‑3pが高い患者は生存が長いという関連が観察され、この分子連鎖が臨床転帰に直結していることが示されました。
放射線療法と免疫療法を強化する標的遺伝子導入法
これらの知見を治療に結びつけるため、研究チームは無害なウイルスベクター(AAV)を設計し、主に大腸癌細胞で活性なプロモーターの下でmicroRNA‑29b‑3pを運ぶようにしました。KRAS変異大腸腫瘍を有するマウスモデルにこのAAVを投与し局所放射線療法と併用すると、照射腫瘍と遠隔の非照射腫瘍の双方が劇的に縮小しました。腫瘍ではDNMT3bが減少し、STINGやインターフェロンシグナルが増加し、T細胞や他の免疫細胞の濃厚な浸潤が見られました。同じmicroRNA‑29b‑3p治療をPD‑1を標的とする免疫チェックポイント阻害剤と組み合わせると生存がさらに改善し、この効果はCD8陽性T細胞に依存しており、免疫系が主要な役割を果たしていることが確認されました。
患者にとっての意味
簡潔に言えば、本研究はKRAS変異大腸癌が放射線で通常作動する内部の警報システムの“配線を切る”ことで免疫攻撃を回避している仕組みを明らかにしました。単一の小さなRNA、microRNA‑29b‑3pを回復させることでDNMT3bを低下させ、STINGを再活性化し、免疫学的に“コールド”な腫瘍を放射線やチェックポイント阻害剤に反応する“ホット”な腫瘍に変えられます。本研究はまだ前臨床段階にありますが、放射線と腫瘍標的型遺伝子療法を組み合わせてKRAS変異大腸癌の抵抗性を克服し、既存療法の有効性を多くの患者に広げる可能性を示しています。
引用: Chang, HY., Chen, JY., Ke, TW. et al. Loss of MicroRNA-29b promotes DNMT3b-mediated STING downregulation to attenuate radiotherapy-induced antitumor immunity in KRAS-mutated colorectal cancer. npj Precis. Onc. 10, 93 (2026). https://doi.org/10.1038/s41698-026-01290-8
キーワード: KRAS変異大腸癌, 放射線療法抵抗性, STING経路, microRNA-29b, 腫瘍免疫学