Clear Sky Science · ja
H&E染色標本から子宮内膜がんの分子サブタイプを予測する解釈可能な深層学習モデル
女性の健康にとってなぜ重要か
子宮内膜の内膜に発生する子宮内膜がんは女性に多いがんの一つであり、世界的に死亡率が上昇しています。現在、このがんは手術、放射線、化学療法、新しい免疫療法に対する反応が異なるいくつかの分子「フレーバー」に分類されることがわかっています。これらの分子サブタイプの同定はいまのところ高価で時間のかかる遺伝子検査を必要とし、多くの病院では容易に提供できません。本研究は、日常的に作成される標準的な病理スライド――すべての患者について既に撮影されているピンクと紫の組織画像――を注意深く設計した人工知能(AI)システムが読み取り、これらの分子サブタイプを正確に推定できるかを検討し、精密治療をより広く利用可能にする可能性を探ります。
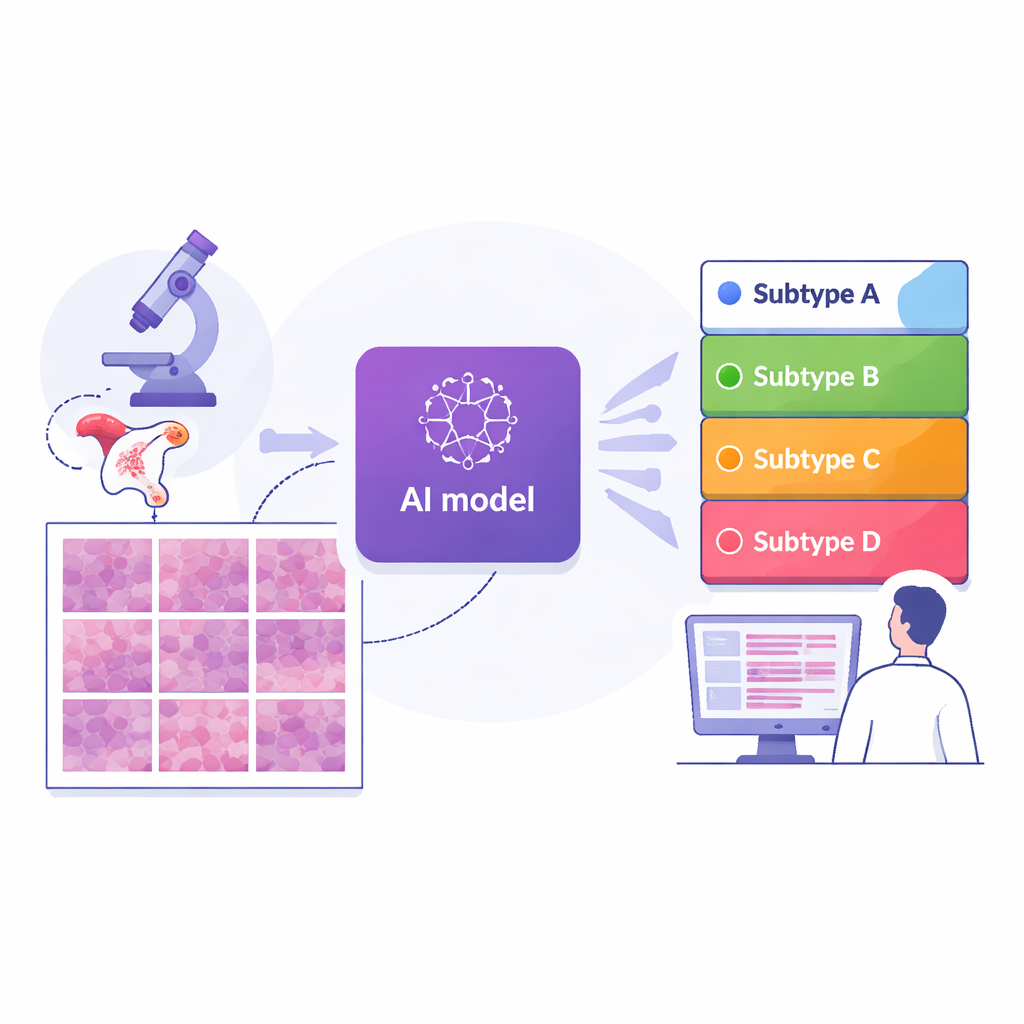
腫瘍の多様性を詳しく見る
すべての子宮内膜がんが同じ挙動を示すわけではありません。成長が遅く子宮内に留まるものもあれば、早期に転移して治療が難しいものもあります。現行のガイドラインは、DNA変化や細胞の遺伝子修復様式に基づき、これらの腫瘍を4つの分子サブタイプに分類します。これらのカテゴリーは予後を予測し、手術の範囲や免疫療法が有益かどうかといった判断を導きます。しかし、必要な遺伝子検査や特殊染色は高コストで専門的な解釈に依存し、小規模または資源の限られた病院では利用できないことが多いです。病理医は長年、多くの分子差が顕微鏡下での細胞や支持組織の外観に視覚的手がかりを残すと考えてきましたが、それらの手がかりは人間の目にはあまりにも微妙で複雑なため、一貫して評価することが難しい場合があります。
コンピュータに病理スライドを読ませる
研究チームは、上海の主要がんセンターで治療を受けた324人の女性から得られた364枚の組織スライドのデジタル画像を収集し、比較用に2つの独立した群も用意しました:国際公開データセットからの296枚と、蘇州の別の病院からの36枚です。すべての症例は事前に高度な遺伝子検査で4つの分子サブタイプのいずれかに分類されていました。研究者らは次に、全スライド画像を数千の小さなタイルに分割し、各タイルを見てそのタイルがどのサブタイプに属する可能性があるかを推定する深層学習モデル(画像認識に用いられるAIの一種)を訓練しました。タイルごとの予測をスライド全体で平均化することで、システムは患者ごとに単一のサブタイプ予測を出し、臨床で医師が腫瘍全体について考える方法を反映しました。
システムの性能
主要な上海群全体で、AIは高い精度を達成しました:4つのサブタイプを区別する全体スコア(推測で0.5、完全分離で1.0となる標準的な統計量)は約0.87でした。別の病院やスライドスキャナーで収集された二つの外部群で検証しても性能は堅調で、約0.84を示し、この手法が比較的堅牢であることを示唆しています。より複雑なアテンションやプーリング手法を用いるいくつかの先行するAI戦略と比較しても、このエンドツーエンドモデルは、現代的な画像解析のバックボーン上に構築されており、概して優れた性能を示しました。重要なのは、著者らがシステムを解釈可能に設計した点で、AIが意思決定に依拠した各タイルの領域を可視化するツールを用いて強調しました。
AIが腫瘍微小環境で「見た」もの
予測を駆動した特徴を理解するため、チームはAIのヒートマップを古典的な病理所見や個々の細胞の形状と配置の詳細な計測に結びつけました。あるサブタイプの腫瘍は支持組織への免疫細胞の密な浸潤を示し、別のサブタイプは構造細胞がぎっしり詰まっている傾向がありました。第三の群は高度に異常な腫瘍細胞の固まりを多く示し、攻撃的な挙動と関連するサブタイプは乳頭状の指状構造や非常に不規則な核を示しました。約2億4500万個の細胞を分割・解析することで、研究者らは細胞サイズ、変異、および間隔の違いを定量化し、特定の組み合わせが特定のサブタイプと一致することを示しました。これらの発見は、分子差が組織構造に識別可能な痕跡を残し、機械が体系的に検出できるという考えを支持します。
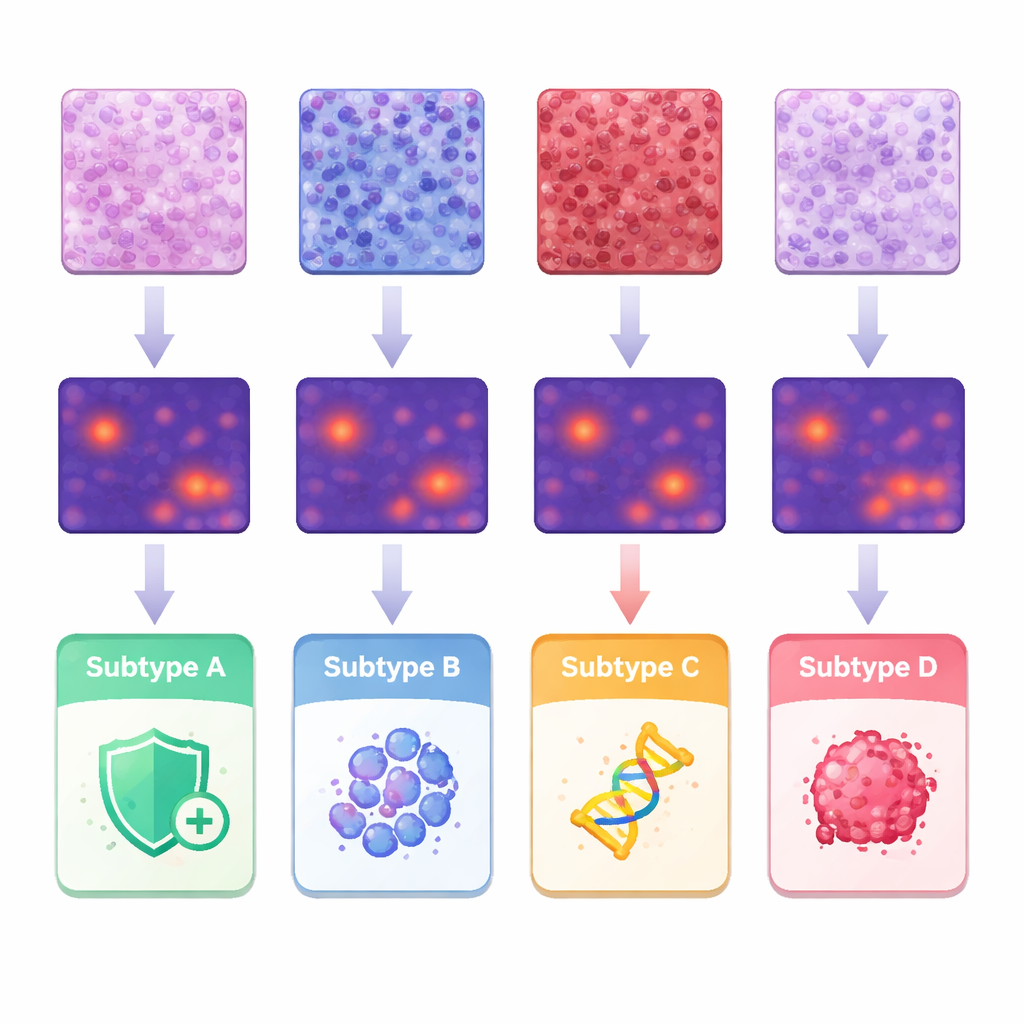
概念実証から臨床支援へ
この研究は遺伝子検査を置き換えることを目的とするものではなく、むしろすでに全ての生検で準備されている標準的な染色を用いる「H&E優先」のトリアージツールを提案します。実際には、AIが生成したサブタイプ確率マップが病理医にどの確定検査を優先的に注文するかを助け、限られた組織を最も情報量の多いアッセイに割り当て、特に完全な分子プロファイリングが得られにくい病院で治療判断を迅速化するのに役立つ可能性があります。研究はまた、最も稀なサブタイプでの性能が弱いことや、運用前により大規模で多様なデータセットが必要であることなど現在の限界も強調しています。それでも、日常の顕微鏡画像に複雑な分子ラベルを推定するのに十分な隠れた情報が含まれていることを示す説得力のある実証を提供し、子宮内膜がんの女性に対するより公平でデータ駆動型のケアへの道を開く可能性があります。
引用: Guo, Q., Cui, H., Zhang, Y. et al. An interpretable deep learning model for predicting endometrial cancer molecular subtypes from H&E-stained slides. npj Precis. Onc. 10, 71 (2026). https://doi.org/10.1038/s41698-026-01280-w
キーワード: 子宮内膜がん, デジタル病理, 深層学習, 分子サブタイプ, 精密腫瘍学