Clear Sky Science · ja
アルゴリズム支援の個別化治療設計が三重陰性乳がんマウスモデルの生存率を改善する
なぜ賢い化学療法が重要か
化学療法は命を救いますが、依然として「画一的」なやり方が主流です。同じ種類のがんの患者にはしばしば同じ薬剤量が同じスケジュールで投与されます。そのため、一部の人には強い副作用が現れ、他の人には十分な効果が得られないことがあります。本研究が問うのは単純だが強力な疑問です:サーモスタットが室温を適時調整するように、コンピュータアルゴリズムで化学療法を個々人にリアルタイムで最適化できたらどうか。攻撃性の高い乳がんの高度なマウスモデルを用いて、研究者らはそのような個別化投与が生存期間を延ばし、薬剤耐性の出現を抑えられることを示しました。
従来のがん薬スケジュールの問題点
現在、多くの患者は耐えうる最大量を決められた間隔で受けることが多く、いわゆる最大耐量(MTD)プロトコールが用いられています。これは、特定の腫瘍の増殖速度、患者の薬物処理能力、あるいは時間経過に伴う腫瘍の応答を考慮しません。その結果、腫瘍は一時的に縮小しても、より薬剤耐性の強いクローンが再発しやすく、患者は強い副作用に苦しむことになります。「メトロノミック」(少量を頻回投与する)などの改善試みも臨床試験では混合した結果に留まり、投与量やタイミングをどのように決めるべきかは明確になっていません。より合理的で個別化された化学療法のスケジューリング手法が求められています。
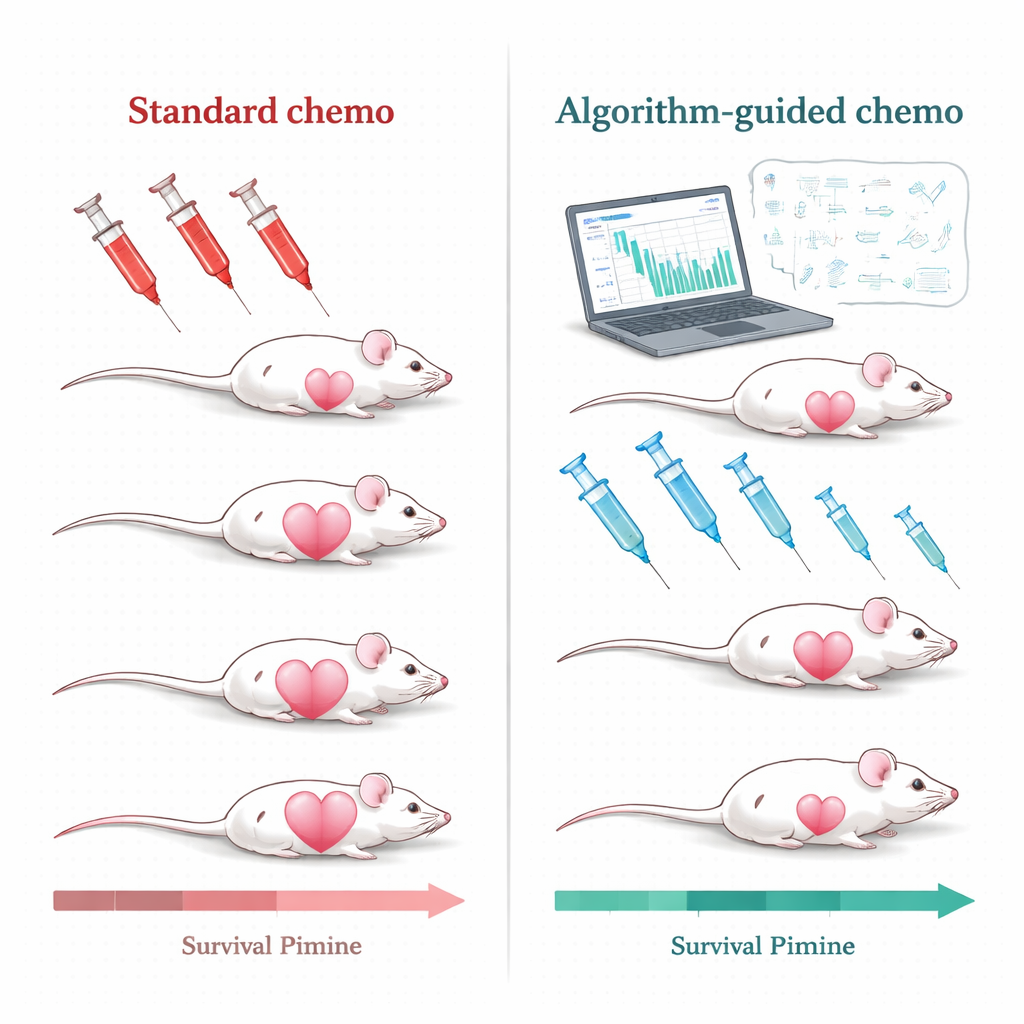
アルゴリズムで治療を調整する
研究チームは、ヒトでも治療が難しく化学療法に依存することの多い三重陰性乳がんを移植したマウスでこの課題に取り組みました。マウスには広く用いられる製剤、ペグ化リポソーム化ドキソルビシンが投与されました。従来のように腫瘍が一定サイズまで再増大したときに高用量を繰り返すのではなく、研究者らは腫瘍の増殖、治療下での縮小、そして薬物の血中動態を記述する数学モデルを構築しました。これらのモデルには臨床的に現実的な簡単な入力を与えました:反復した腫瘍サイズの測定と血中薬物濃度。これらのデータからコンピュータアルゴリズムが各マウスに個別化された治療計画を作成しました。
コンピュータ支援の2つの方法
研究では2種類のアルゴリズム支援治療設計を試験しました。一つ目はPDPKと呼ばれるアプローチで、初期データを用いて30日間の比較的少量を繰り返すスケジュールを設計し、血中薬物濃度を安定して低めに保つことを目指しました——腫瘍を抑制できるだけの水準は保ちつつ、毒性を抑える設定です。二つ目はモデル予測制御と呼ばれる方法で、アルゴリズムは毎日の最新の腫瘍測定に基づいて計画を更新し、腫瘍を徐々に低下させるように投与量を調整しました。どちらの方法も基本的には同じ考え方に依拠しています:腫瘍を持つマウスの現実的な“デジタルツイン”を用いて事前に多様な投与パターンをシミュレーションし、安全性制約の下で最も効果が期待できるパターンを選ぶのです。
生存期間の延長と薬剤耐性の抑制
チームがこれらのアルゴリズム誘導下のレジメンを、従来の高用量かつ腫瘍再増大トリガー型のプロトコールと比較したところ、顕著な違いが見られました。従来療法では腫瘍は初期に急速に縮小することが多い一方で、最終的には再発し、繰り返しの大用量投与は薬剤耐性の出現を助長しました。対照的に、アルゴリズムで設計された治療の多くは腫瘍をより厳密に制御し、再発までの期間を延ばし、多くの場合、試験期間中に明確な耐性の兆候を示しませんでした。数十匹のマウスを通じて、PDPK群とモデル予測制御群はいずれも標準スケジュール群より有意に長く生存し、いくつかのアルゴリズムベースの戦略は強い統計的に有意な生存改善を示しました。
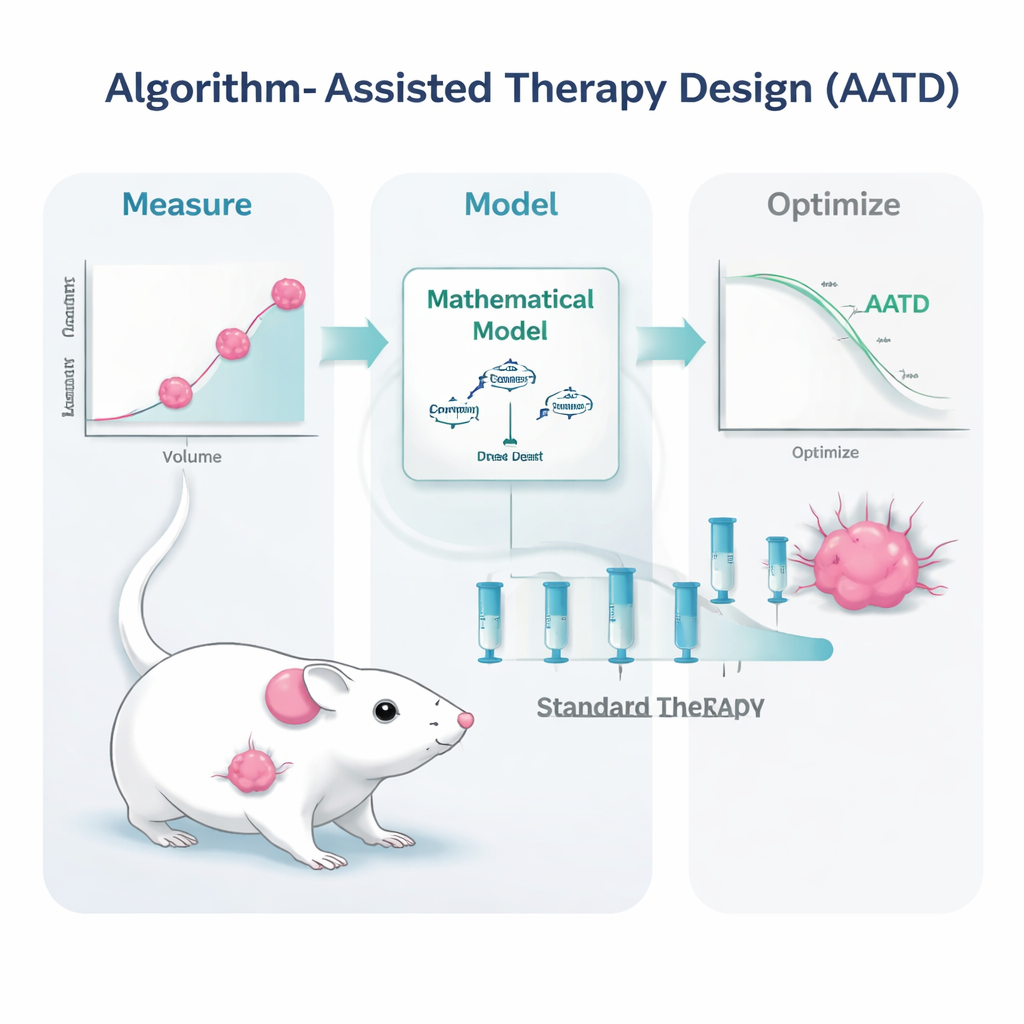
将来の患者にとっての意義
この研究はマウスで行われましたが、主要要素である腫瘍サイズの測定、血中薬物濃度のモニタリング、そしてコンピュータモデルの運用は、現代の画像診断や検査手法を用いればヒト患者でもすでに可能です。本研究は「標準投与量は何か?」と問う代わりに、「この患者自身の腫瘍挙動と薬物処理特性を踏まえて、今この時点で最適な用量とタイミングは何か?」と医師が問える未来を示唆します。より頻回の測定や柔軟な投薬の実務上の課題など現実的なハードルは残りますが、メッセージは明確です:化学療法は一律で鈍いものに留まる必要はありません。アルゴリズムの助けを借りれば、より精密で適応的な手段となり、攻撃性の高いがんの長期制御を患者によりよい形で提供できる可能性があります。
引用: Gombos, B., Léner, V., Drexler, D.A. et al. Algorithm-assisted individualized therapy design improves survival in a mouse model of triple-negative breast cancer. npj Precis. Onc. 10, 84 (2026). https://doi.org/10.1038/s41698-025-01245-5
キーワード: 個別化化学療法, 三重陰性乳がん, アルゴリズム支援治療, 数学的腫瘍モデリング, ドキソルビシン投与量