Clear Sky Science · ja
空間トランスクリプトミクスが小細胞肺がんにおける分子異質性と亜型特異的治療標的を明らかにする
この肺がん研究が重要な理由
小細胞肺がんは死亡率の高いがんの一つで、主に喫煙歴のある人に発症し、化学療法後に速やかに再発することが多い。臨床では全ての小細胞肺がんが同じように振る舞うわけではないことは知られているが、各腫瘍内で異なるがん細胞型や免疫細胞がどのように配置されているかを可視化する手段は限られていた。本研究は、腫瘍スライド上の数千の微小スポットで遺伝子発現を読み取る新しい技術を用い、各サンプルの「分子マップ」を作成した。これを専用の計算解析と組み合わせることで、より正確な亜型特異的治療の指針となりうる隠れたパターンを明らかにした。
腫瘍をその場でマッピングする
研究チームは、術前に薬物療法を受けていない限局期小細胞肺がんの患者21例から腫瘍試料を解析した。組織をすりつぶして空間情報を失う代わりに、空間トランスクリプトミクスを適用した。これは組織断面上の多数の定義されたスポットでどの遺伝子が活性化しているかを測定する手法で、各スポットは元の位置に残るため、がん細胞、正常細胞、免疫細胞がどこに存在するかと遺伝子活性を結びつけることができる。さらに二つの重要なツールを加えた:腫瘍細胞が周囲組織にどれだけ浸潤しているかを定量化する新しい「Edgeindex」スコアと、スポットが腫瘍か非腫瘍かを自動判定する人工ニューラルネットワーク(機械学習の一種)である。
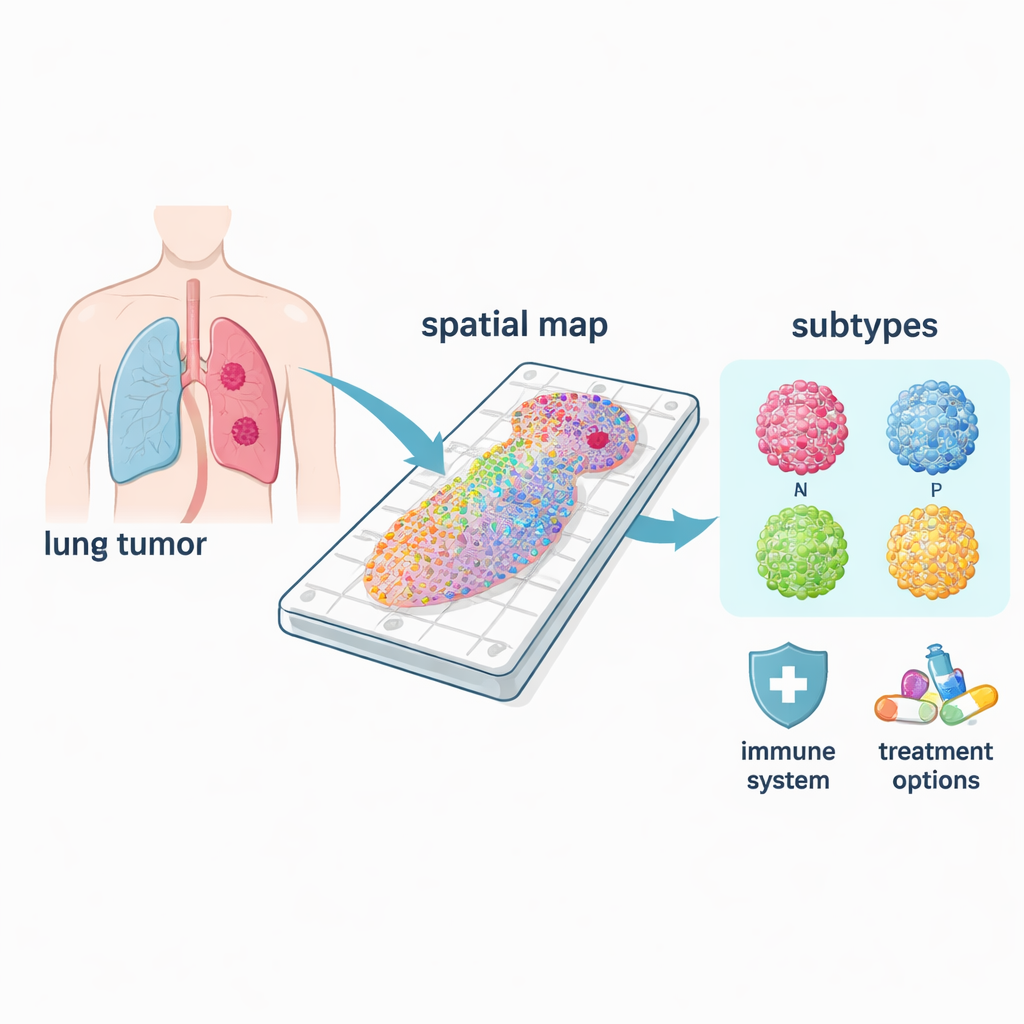
一つの病気に複数のがんタイプが存在する
小細胞肺がんは単一の病気ではなく、少なくともASCL1、NEUROD1、POU2F3、YAP1と呼ばれる主要な分子亜型を含む。これらはそれぞれを規定する主要な制御遺伝子に由来する名称である。空間マップを用いることで、各亜型が腫瘍内のどこに優勢か、そしてそれぞれの生物学がどのように異なるかを観察できた。一般的なASCL1およびNEUROD1亜型は細胞分裂プログラムと強く結びつき、高増殖性という特徴と一致した。一方、POU2F3領域は免疫関連経路に結びつき、YAP1領域は代謝や組織再編成に関連するシグナルを示した。これらは転移や治療抵抗性に関係する可能性がある。これらのパターンが空間的に解像されるため、混合腫瘍の中で真の“ドライバー”亜型を特定できる点が、バルク検査では見落とされがちな利点である。
浸潤する境界と免疫の変化
本研究の主要な革新の一つであるEdgeindexは、腫瘍細胞が周囲の非腫瘍組織とどれだけ混在しているかを捉える。スコアが低い場合は緊密で境界の明瞭な腫瘍を反映し、スコアが高い場合は散在する島状構造や不整な侵襲性の境界を示す。Edgeindexが高い腫瘍は、細胞外マトリックス、転移、細胞死に関連する遺伝子プログラムが富んでいた。また顕著な免疫景観の変化を示し、ヘルパーT細胞やその他の獲得免疫の細胞が減少する一方で、特定のナチュラルキラー細胞や単球などの自然免疫細胞が増加していた。著者らはこれを「免疫ニッチの再構築」と解釈しており、腫瘍が精密で標的化された免疫応答を遠ざけ、がんを十分に制御できない、より非効率的な自然免疫優位の環境を残していると考えている。
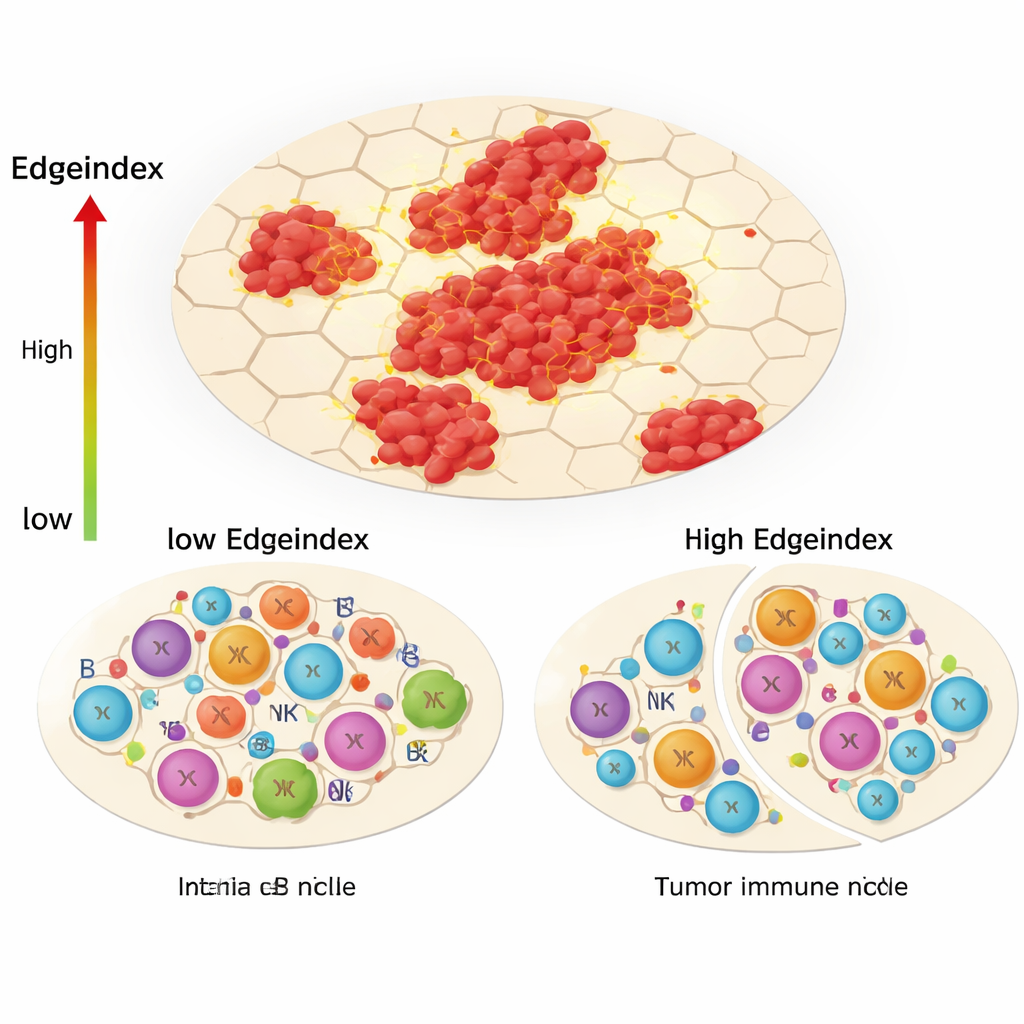
腫瘍内外の隠れた多様性
亜型や浸潤パターンに加えて、空間データはがん細胞集団とそれを取り巻く微小環境の双方が内部的に多様であることを明らかにした。各腫瘍内でスポットをクラスタリングすることで、がん領域と周辺の非腫瘍組織における異なる遺伝子発現上の「近隣」がいくつ存在するかを数えた。腫瘍内部の多様性が高いことは免疫関連経路と結びつき、周辺組織の特定のパターンは細胞周期活性や遺伝子調節に関連していた。研究者らは既知のシグナル分子を用いて異なる領域同士の“通信”の強さも評価した。領域間の通信がより強い腫瘍は免疫関連シグナルが強く出る傾向があり、免疫活動と腫瘍成長が空間的に緊密に絡み合っているという考えを補強した。
時間経過に沿った腫瘍発展の追跡
腫瘍細胞が病勢の進行に伴ってどのように変化するかを近似するために、チームは遺伝子活性に基づいて細胞を発達経路に沿って順序付ける“擬似時間(pseudotime)”解析を行った。サンプル全体で、1つの遺伝子UCHL1が繰り返しこれらの軌跡の中心にあることが確認された。UCHL1の高発現は腫瘍スポットにおける強い細胞周期活性と一致し、低発現は免疫や細胞死経路と整合した。UCHL1は神経系型のタンパク質で、これまで攻撃的な肺がんと結び付けられてきたため、これらの結果は、特に小細胞肺がんを駆動する神経内分泌様の細胞に対する有用な薬剤標的になり得るという見解を強める。
患者にとっての意義
平たく言えば、本研究は小細胞肺がんの顕微鏡スライドを、異なるがん亜型がどこに存在するか、どれだけ侵襲的か、周囲とどのようにやり取りしているか、免疫系がどのように応答または失敗しているかを示す豊かで層状の地図に変換した。新しいEdgeindexスコアとマッピング手法は、どの腫瘍が特に浸潤性が高いか、境界でどの免疫細胞が存在あるいは欠如しているかを浮き彫りにする。これらの空間パターンをDLL3、BCL-2、AURKA、IGF-1R/PARP、あるいは免疫チェックポイントを標的とする薬剤のような亜型特異的弱点に結びつけることで、本研究は患者ごとに最適化された治療戦略へと近づける。これらのツールはより大規模な研究での検証を要するが、治療選択肢が切実に求められるこのがん種に対して、より精密で効果的な治療への設計図を示している。
引用: Xie, T., Tang, L., Fan, G. et al. Spatial transcriptomics reveals molecular heterogeneity and subtype-specific therapeutic targets in small cell lung cancer. npj Precis. Onc. 10, 81 (2026). https://doi.org/10.1038/s41698-025-01243-7
キーワード: 小細胞肺がん, 空間トランスクリプトミクス, 腫瘍の異質性, 腫瘍免疫微小環境, プレシジョンオンコロジー