Clear Sky Science · ja
弱教師あり学習を用いた原発性皮膚メラノーマにおける転移リスクの早期検出
患者と医師にとってなぜ重要か
皮膚のメラノーマが致命的になりうるのは、その皮膚病変自体のせいではなく、腫瘍が無言のうちに他の臓器へ広がるためです。現在、医師は主に腫瘍の厚さや表面の潰瘍の有無を基に、どの患者が最も高リスクかを推測しています。本研究は、最新の人工知能(AI)が原発皮膚腫瘍のルーチンな顕微鏡画像からより多くの情報を読み取り、特に比較的小さく見える腫瘍の患者に対して危険ながんをより早期に示唆できるかを問います。
組織画像に潜む静かな警告サインを探す
研究者らは、426件の原発性皮膚メラノーマの標準的な顕微鏡スライドのデジタル画像と、腫瘍の厚さ、潰瘍、分裂能、腫瘍サイズといった基本情報を収集しました。これらの腫瘍の約3分の2はその後リンパ節や遠隔臓器への転移を起こし、残りは少なくとも3年間の追跡期間中には転移を示しませんでした。病理医に特定領域を手で注釈させる代わりに、チームはコンピュータに各スライドの全領域を調べさせ、大きな画像を多数の小さなパッチに切り分けました。問いは単純です:各患者が最終的に転移したか否かだけを学習させたコンピュータが、高リスクと低リスクの腫瘍を分ける視覚パターンを見つけられるか、ということです。
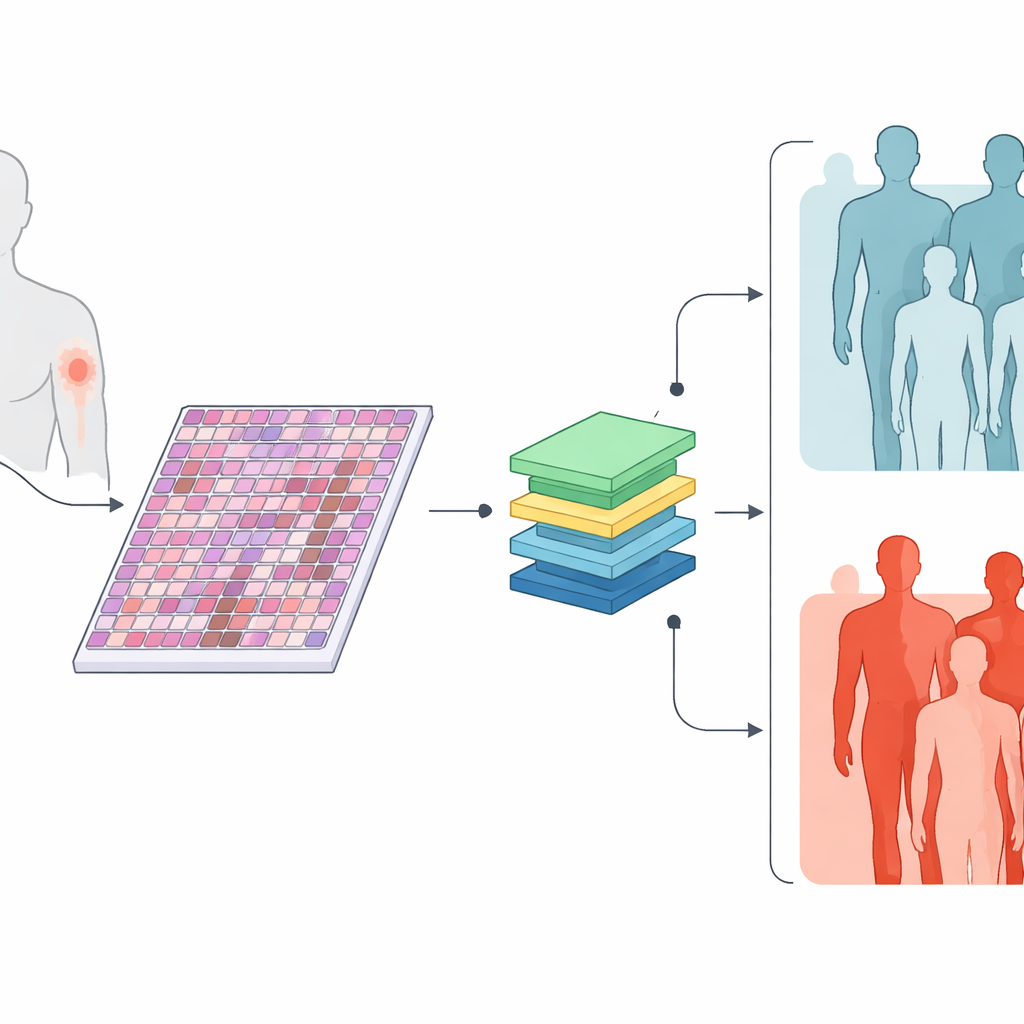
組織を地図のように読む機械を教える
チームは、膨大な医療画像とテキストのコレクションで事前学習された最近のAI手法をメラノーマに適用しました。1つのモデル、TransMILは組織画像のみを用いました。別のモデル、MultiTransは画像情報と腫瘍の臨床的特徴を簡潔に表したテキスト説明を組み合わせました。3つ目のより単純なモデルBertMLPは臨床情報のみを使用し、画像は無視しました。未使用の別群のスライドで評価したところ、画像ベースの両モデルは転移ありと転移なしを約85%の確率で正しく識別し、臨床データのみのモデルより全体精度が高まりました。これは、顕微鏡画像に現在のルーチン測定では十分に捉えられていない将来の挙動に関する豊富な手がかりが含まれていることを示唆します。
判断が最も難しい領域での強力な支援
画像ベースAIの利点は、医師が積極的治療の要否を判断するのに最も苦労する中間的な厚さの腫瘍群で最も明らかでした。これらのT2メラノーマにおいて、画像モデルは臨床情報のみのモデルを明確に上回り、後者は過度に多くの腫瘍を低リスクと分類する傾向がありました。画像ベースのシステムはより厚い腫瘍でも良好に機能しましたが、そうした症例は標準指標で既に危険と認識されることが多いです。最初に非転移性と分類されたが後に転移した複数の患者では、AIモデルが何年も前に原発腫瘍を高リスクと正しく示しており、こうしたツールが将来より早期でより標的を絞った治療を支援する可能性を示しています。
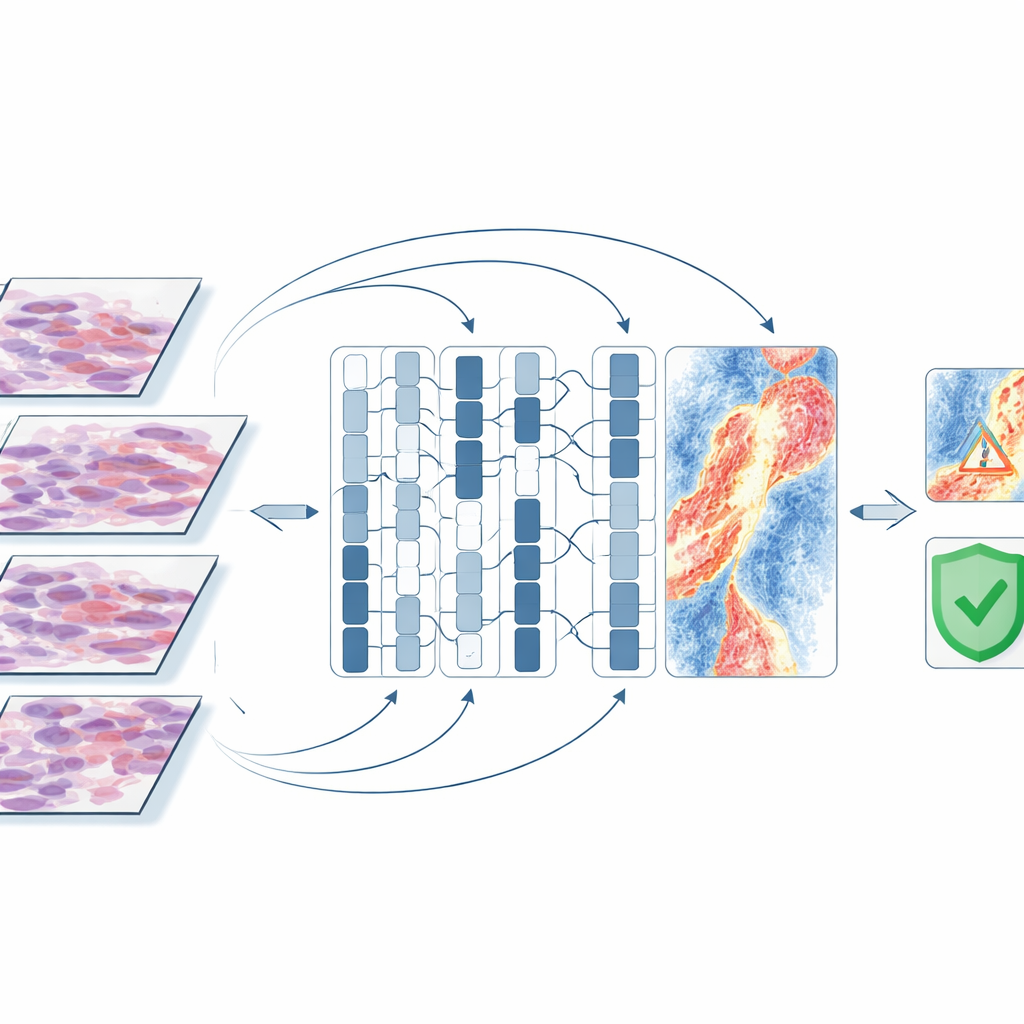
AIが腫瘍内で「注目」するもの
コンピュータが手がかりとして何を使っているかを理解するため、研究者らは予測に影響の大きいスライド領域を強調する注意マップを生成しました。最終的に転移した腫瘍では、モデルはしばしば腫瘍細胞の密な塊ではなく、周囲の環境――血管、表面の壊死や潰瘍部分、皮膚深部の炎症細胞の帯状領域など――に注目していました。転移しなかった腫瘍では、強調領域は損傷の少ない連続した表面層である傾向がありました。誤分類された症例では、無個性の結合組織や脂肪、スライド作製時のアーティファクトが含まれており、明確な組織シグナルが弱い場合にコンピュータが苦戦したことを示唆します。これらのパターンは、メラノーマ細胞がリンパ管や血流へと逃れるメカニズムに関する現在の理解と一致しており、AIの判断に生物学的な妥当性を与えます。
限界、次のステップ、そして意味すること
この研究は単一の病院で数百例を対象に行われ、モデルは異なる施設での検証や生存時間の予測にまだ使われていません。アプローチは病理医に取って代わるものではなく、むしろルーチンなスライドから自動抽出される新たなリスク情報の層を付け加えるものです。それでも、弱教師ありAIが原発メラノーマ組織から手間のかかる手動注釈なしに有意な転移の警告兆候を発見できることを示しています。より大規模で多施設の検証を経て、皮膚写真や遺伝子発現検査など他のデータと組み合わせられれば、こうしたツールは一見早期の段階に見えるが実際には高い転移リスクを抱える患者をより適切に特定し、より厳重な経過観察や早期の予防的治療を提供するのに役立つ可能性があります。
引用: Dahlén, F., Shujski, I., Yacob, F. et al. Early detection of metastatic risk in primary cutaneous melanoma using weakly supervised learning. Sci Rep 16, 11234 (2026). https://doi.org/10.1038/s41598-026-45588-w
キーワード: メラノーマ, 転移リスク, デジタル病理, 人工知能, 弱教師あり学習