Clear Sky Science · ja
Pyrococcus furiosusのドリチルリン酸マンノース合成酵素の結晶学的データは、酵素がその糖脂質生成物を反転させうることを示唆する
高温性微生物が細胞外被膜を保つ仕組み
沸点に近い環境で生きる多くの微生物は、細胞表面の保護的な糖被膜によって生存しています。この被膜を構築するには、膜の一側で作られた後に反対側へ移動させる必要のある特殊な脂質–糖分子が必要です。本研究は、耐熱性微生物由来のそのような分子を合成する酵素の一つを解析し、驚くべきことに同じタンパク質が生成物を膜を横切って反転(フリップ)させる手助けもする可能性があることを示唆しています—一つで二つの役割を果たすかもしれません。
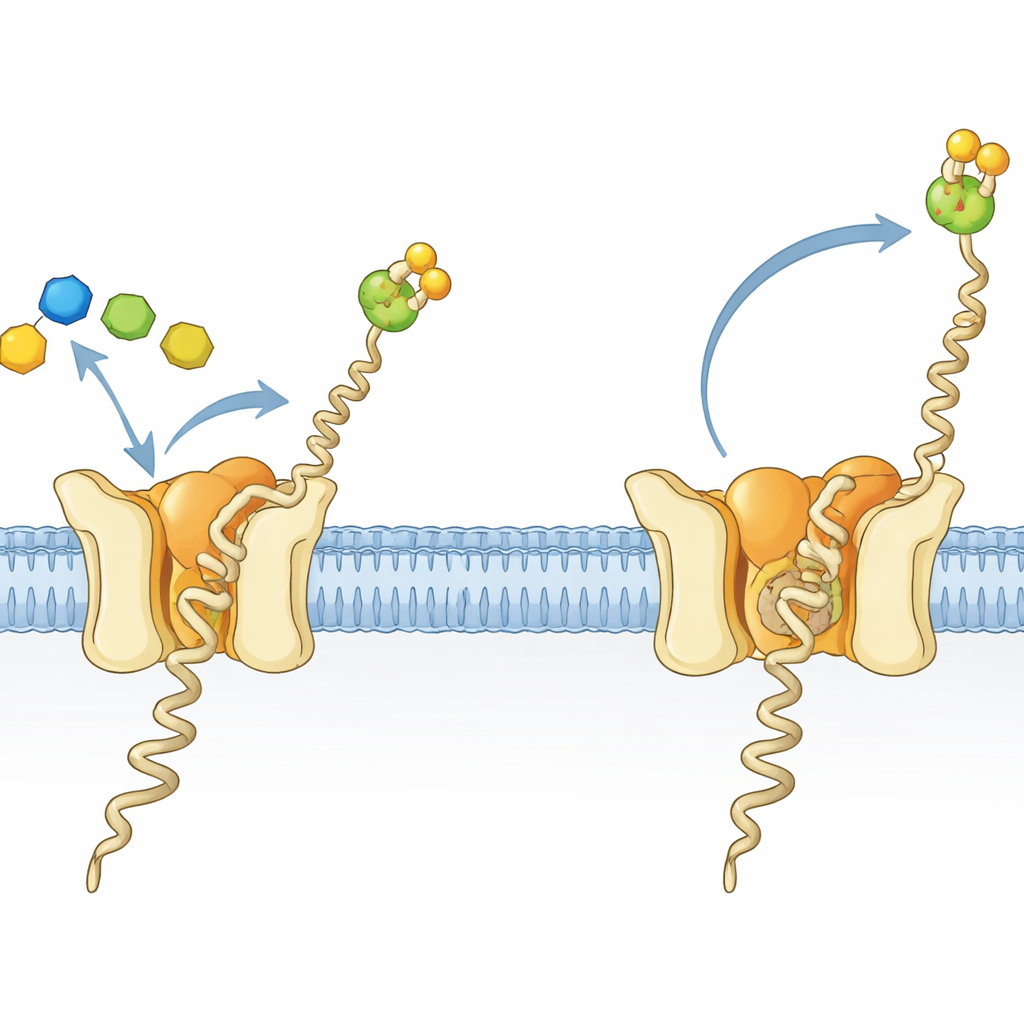
重要な糖–脂質のための小さな工場
すべての生物の細胞は多くのタンパク質に糖鎖を付加して飾り付けを行っており、これは正しい折りたたみ、安定性、細胞間コミュニケーションに不可欠です。古細菌と真核生物では、これらの飾り付けの重要な構成要素がドリチルリン酸マンノース(Dol-P-Man)と呼ばれる糖–脂質です。Dol-P-Manは膜に埋め込まれた長い疎水性の尾部と、水性環境に突き出す糖–リン酸の頭部からなります。Dol-P-Manはドリチルリン酸マンノース合成酵素(DPMS)によって作られ、可溶性の供与体からマンノースを膜結合脂質へ転移します。超好熱古細菌Pyrococcus furiosusでは、DPMSは単一鎖のタンパク質(タイプIII DPMS)で、可溶性の触媒領域が四本のヘリックスからなる膜貫通部に接続されており、その役割は不明でした。
反応の瞬間をとらえる
研究者たちはP. furiosusのDPMSを基質とともに結晶化し、X線結晶構造解析で反応の経過を追いました。新しい構造は、これまでの3つの構造と合わせて、糖が転移される瞬間の周辺を捉えた一連のスナップショットを示します。ある状態では、供与体(GDP-マンノース)とDol-Pに類似したアクセプターが反応性のマンノース炭素をDol-Pのリン酸基の直前に配置する精密な幾何学で結合しており、理想的な「転移前」配置になっています。酵素上のループは前後の扉のように働き、供与体と金属イオンを閉じて保持した後、再配置してDol-Pが入る経路を開き、糖が渡された後に使い終わったGDPが出て行けるようにします。これらの詳細は、酵素が膜表面で効率的かつ正確に糖転移を行う仕組みを明らかにします。
膜内に隠れた逆向きの生成物
より驚きだったのは、同じ結晶の中で見られた別の明確な状態です。ここでは、生成されたDol-P-Man分子は活性部位にはなく、タンパク質の膜貫通部のより深い位置に「逆向き」に収納されています。糖–リン酸の頭部は2対のヘリックス(TMD1とTMD2)の間にある極性ポケットに位置し、疎水的な尾部はヘリックスが形成する溝に沿って伸びています。重要なアミノ酸であるフェニルアラニンが、このポケットへのアクセスを遮断したり開いたりするゲートとして働くように見えます。電子密度の質や結晶中でのタンパク質のパッキングの仕方は、この反転したDol-P-Manが結晶接触のアーティファクトではなく、酵素が採り得る実在し十分に占有された状態であることを示唆しています。
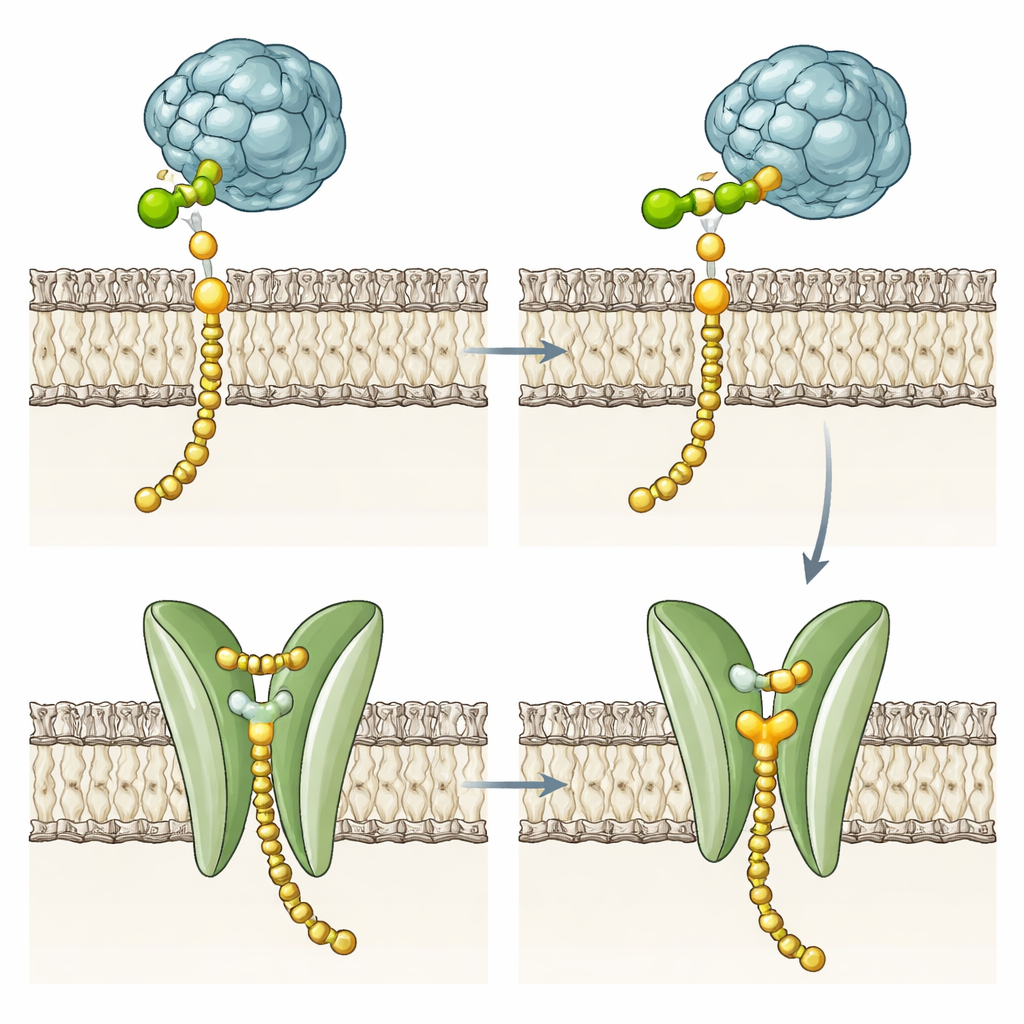
変異酵素が示す第二の役割の示唆
膜貫通領域が糖転移化学反応に必要かどうかを検査するため、研究チームは複数の変異体を作製しました。彼らはヘリックスの大部分またはすべてを欠失させたり、酵母のDPMS由来の別の膜区間と置き換えたり、主要なポケット残基やフェニルアラニンのゲートを変えたりしました。驚くべきことに、これらの変異体は多くが膜中でやや不安定なものもある一方で、ほとんど元の酵素と同様の速度でDol-P-Manを合成しました。これは、核心的な化学反応が可溶性の触媒領域に存在し、四ヘリックス束はマンノースをDol-Pに結合させるためには必須でないことを示します。代わりに、保存された極性ポケット、溝、ゲーティング残基は、特に剛直な膜を持ち自発的な脂質反転が熱力学的に高コストとなる超好熱古細菌において、生成物の取り扱いに特化した役割を示唆します。
二重機能酵素が重要な理由
構造学的および変異解析の証拠を総合すると、著者らはタイプIII DPMSを「ムーンライティング」タンパク質であると提案します。まず内側の膜面でDol-P-Manを合成し、その後膜貫通領域が糖–脂質分子を反転させて頭部が細胞外側に現れるのを助け、細胞の糖被膜を構築する他の酵素群がそれを取り込めるようにするのです。進化は主に極端な高温性古細菌でこの混成的な設計を選好したようで、合成部位を専用の反転溝に近づけることで無駄や熱損傷を最小化できると考えられます。本研究はフリッピング活性を直接証明するものではありませんが、過酷な膜障壁を越えて重要な脂質中間体を生成し再配置する酵素の具体的な構造モデルを提示しています。
引用: Gandini, R., Keskitalo, M.M., Reichenbach, T. et al. Crystallographic data for Pyrococcus furiosus dolichylphosphate mannose synthase suggest that the enzyme could flip its glycolipid product. Sci Rep 16, 9076 (2026). https://doi.org/10.1038/s41598-026-44343-5
キーワード: ドリチルリン酸マンノース, 脂質フリッパー, 古細菌, タンパク質の糖鎖付加, 膜酵素