Clear Sky Science · ja
定量病理学を用いた歯原性粘液腫スペクトラム病変の多施設臨床病理学的研究
患者と歯科医にとってなぜ重要か
顎骨の深部では、まれな腫瘍が何か月も、あるいは何年も静かに成長してから発見されることがあります。これらは歯原性粘液腫や粘液線維腫と呼ばれ、悪性ではありませんが、拡大して骨を弱め、手術を複雑にすることがあります。長年にわたり病理医は主に眼視でこれらを判断してきたため、同じタイプの病変について病院ごとに記述や分類に差が生じていました。本研究は強力な画像解析ツールを顕微鏡スライドに導入し、人工知能(AI)が医師にこれらの腫瘍をより明確かつ一貫して見せるのにどう役立つかを示します。
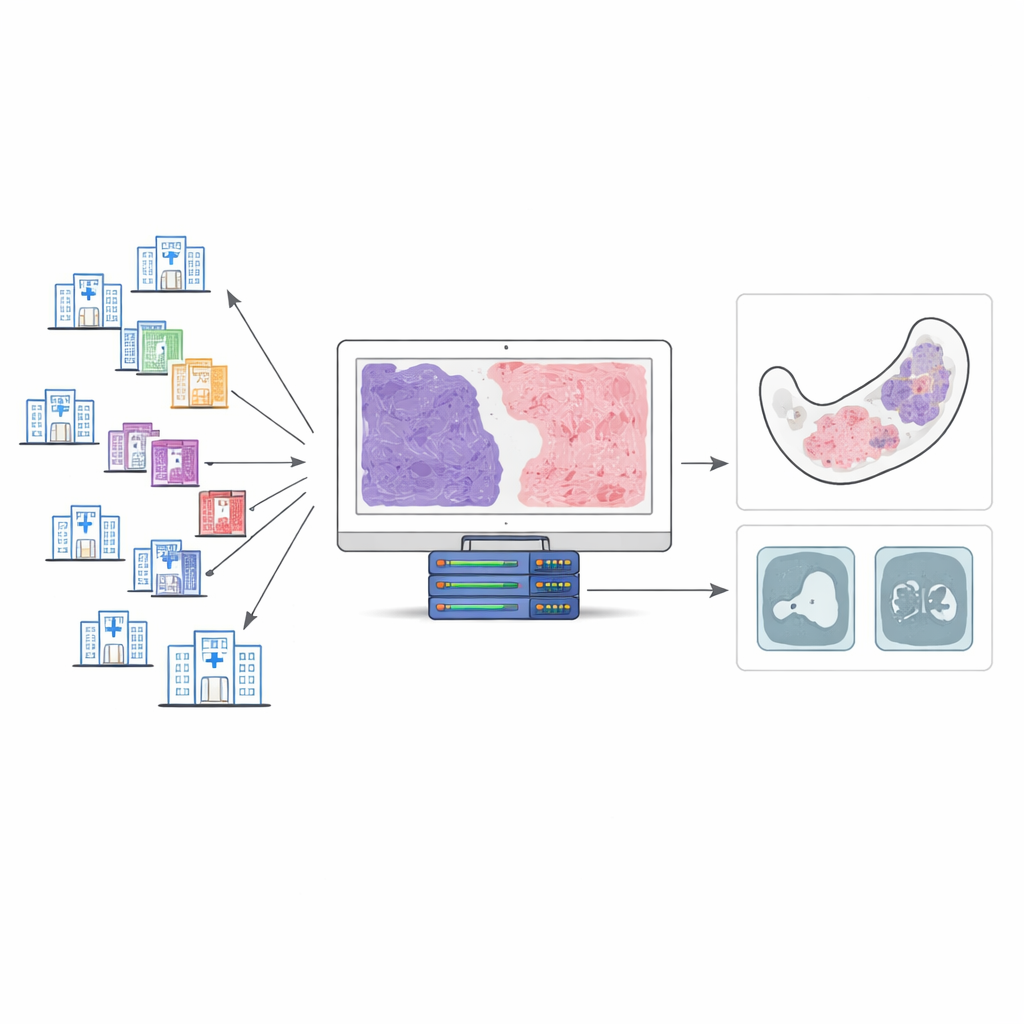
見た目は紛らわしく似ているまれな顎の腫瘍
歯原性粘液腫と歯原性粘液線維腫は歯の形成に関わる組織から発生します。どちらも柔らかくゼリー状の腫瘍で顎骨内に存在します。顕微鏡下では、ゆるい粘液様領域とより密な線維性の帯が混在しています。伝統的に病理医は腫瘍内の線維成分と粘液成分の比率を推定して区別しようとしてきました。しかし、これらの腫瘍は稀であり、どの程度の線維組織があれば診断を別のラベルに変更すべきかについて普遍的に合意された基準はありません。その結果、症状や画像所見が似ている患者でも、病院によって非常に似た病変に異なる名称が付けられることがあります。
顕微鏡スライドを数値に変える
研究チームは20年にわたり34施設で治療された患者から143の組織サンプルを収集し、最終的に厳格な品質基準を満たす100症例に注目しました。すべてのサンプルは線維組織を周囲の腫瘍と異なる色に染める特殊染色(Masson三色染色)で処理されました。2名の専門口腔病理医が各症例を慎重にレビューし、線維組織の割合を10%刻みで推定しました。これらの専門家の推定は、AIシステムを同じ作業を自動的かつ完全に定量的に行うように学習させるための基準となりました。
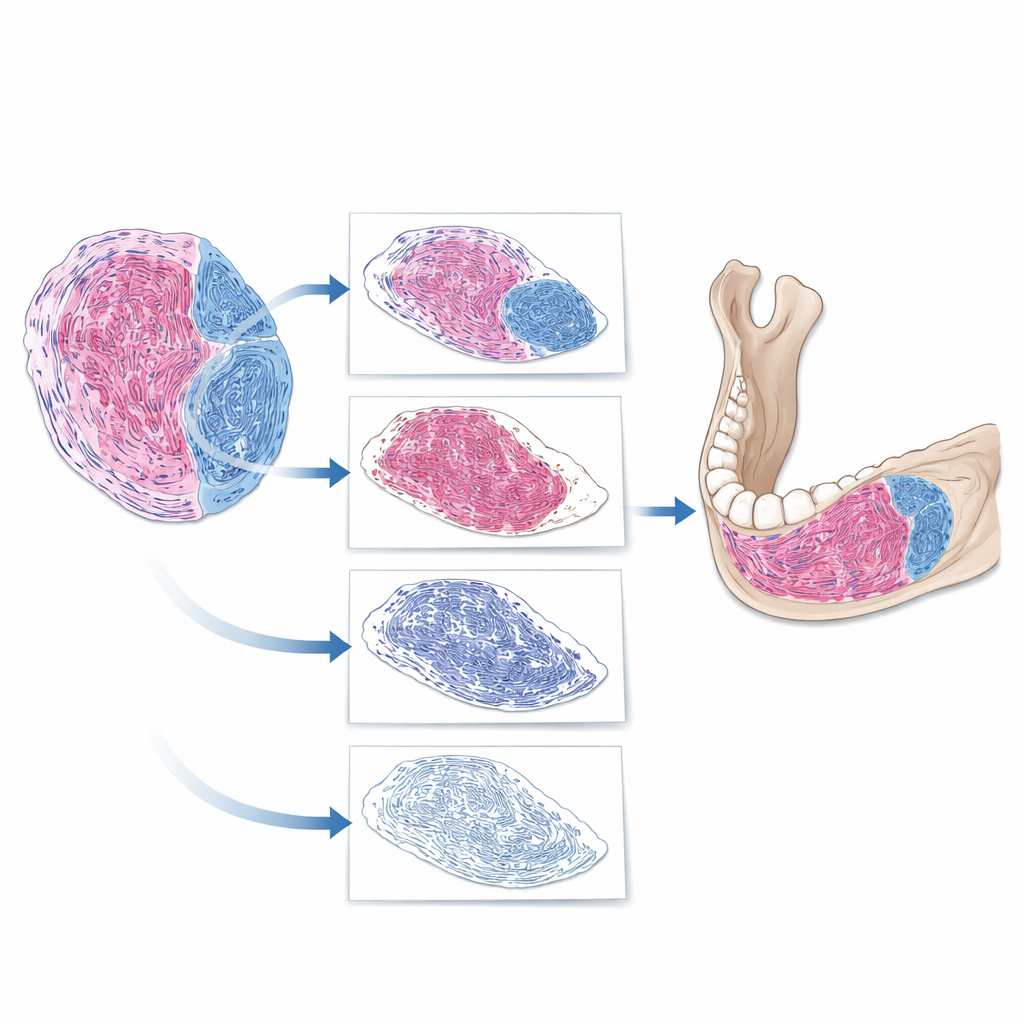
AIは腫瘍スライドをどう「読む」か
チームは全スライド画像を解析する段階的なデジタルパイプラインを構築しました。まずソフトウェアはスライド上の背景と実組織を分離しました。次に骨や歯などの近傍構造から腫瘍を切り出しました。最後に腫瘍内で細胞核を除外し、残りの物質に着目して線維染色が染まった領域を同定しました。ここからAIは線維組織比率、つまり線維組織面積を総腫瘍面積で除した値を算出しました。研究者がAIが生成した値と専門家の評価を比較したところ、多くの症例で概ね10パーセンテージポイント程度のズレにとどまり、相関は強いものでした。これはAIが専門家の判断を信頼性をもって再現し、あいまいな印象ではなく正確な測定値として表現できることを示唆します。
線維成分が腫瘍の見た目に示すこと
こうした測定値を用いて、研究者は線維含有量が臨床所見や画像所見とどう関係するかを検討しました。線維組織の割合は施設間で大きく異なり、これは当初病理医が腫瘍に付けたラベルの差を反映していました。画像特徴を詳しく見ると、ひとつの腔のみを示す単房性病変では複数の小室を持つ多房性病変よりも線維組織の割合が高い傾向が明らかになりました。これは、より線維性で密な組織はより固い単一腔の塊を形成しやすく、より緩い粘液に富む組織はいくつかの空間に分かれやすいという考えと一致します。
将来の診断と治療にとっての意義
本研究は病名を変えたり病理医を機械で置き換えたりすることを目的としていません。むしろ、AIに基づく定量病理学が多施設にわたるまれな顎腫瘍に共通のものさしを提供できることを示しています。腫瘍組織の微妙な質感を再現性のある数値に変えることで、日常の診断がどれだけ主観的判断に依存しているかを明らかにし、その変動を減らす手段を提示します。患者にとっては、これらの病変の解釈がより一貫することで治療判断が明確になり、施設間での転機比較がしやすくなる可能性があります。同様の手法が他のまれな腫瘍にも拡張されるにつれ、AI支援の顕微鏡診断は病理医の病変の見え方を静かに変え、評価をより比較可能で最終的により有用なものにするかもしれません。
引用: Harazono, Y., Fukawa, Y., Iwasaki, T. et al. Multicenter clinicopathological study of odontogenic myxoma spectrum lesions using quantitative pathology. Sci Rep 16, 11221 (2026). https://doi.org/10.1038/s41598-026-42019-8
キーワード: 歯原性粘液腫, 顎骨腫瘍, デジタル病理学, 人工知能, 線維組織比率