Clear Sky Science · ja
MR温度計測を用いたマイクロ波アブレーション手技のプロトコル最適化のための目標温度と加熱時間の定量的ex vivo評価
腫瘍治療をリアルタイムで見る
医師が肝臓の腫瘍を熱で焼灼するとき、手技の最中にどの部分が破壊されているかを正確に把握したいと考えます。磁気共鳴画像法(MRI)は、体内で熱が広がる過程を「温度として可視化」する手段を提供します。本研究は、マイクロ波アブレーション中に肝組織をどの程度の温度でどれくらいの時間加熱すれば、MRIで明瞭かつ信頼できる温度マップが得られるかを検討したものであり、より精密で低侵襲ながん治療に向けた重要な一歩を探ります。
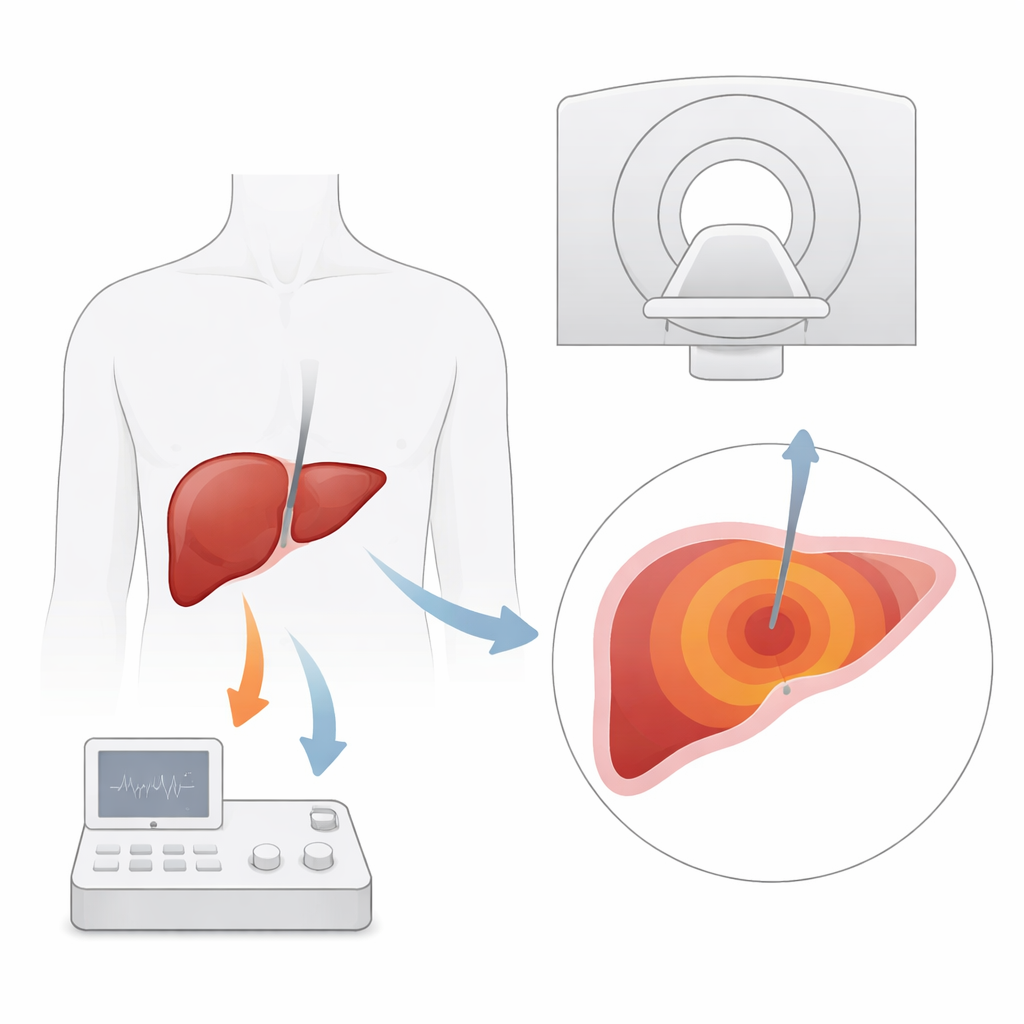
なぜ熱療法はより良い可視化を必要とするのか
マイクロ波アブレーションは細い針を使ってエネルギーを注入し、肝内の腫瘍組織を加熱して壊死させます。手術を受けられない肝癌や転移の患者にとって特に重要な選択肢です。従来の画像ガイド(超音波やCT)は針の位置決めに用いられますが、小さな腫瘍の明瞭な描出や、治療中に熱がどこまで広がったかを追跡するのは苦手です。MRIは軟部組織を高精細に描出できるだけでなく、水分子の性質を利用して温度変化を測定できる点が際立っています。理論的には、これにより肝臓の温度分布をリアルタイムで監視し、腫瘍と安全余白が確実に壊死しているかを確認できます。
過度の加熱が視界を遮るとき
しかし実際には、組織が非常に高温になるとMRIによる温度マップの信頼性が低下することがあります。高温では組織内の水分が沸騰して微小な気泡が生じ、磁場を乱します。これらの乱れは偽の温度読取値や異常な形状としてマップ上に現れ、真のアブレーション領域の境界を判別しにくくします。研究者らは、わずかに低い目標温度を用いることで、処理領域は小さくなるかもしれないが、よりクリーンで信頼できるMRIマップが得られるのではないかと考えました。彼らの目的は、画像の明瞭さと十分な組織破壊を両立させる温度と加熱時間の組み合わせを見つけることでした。
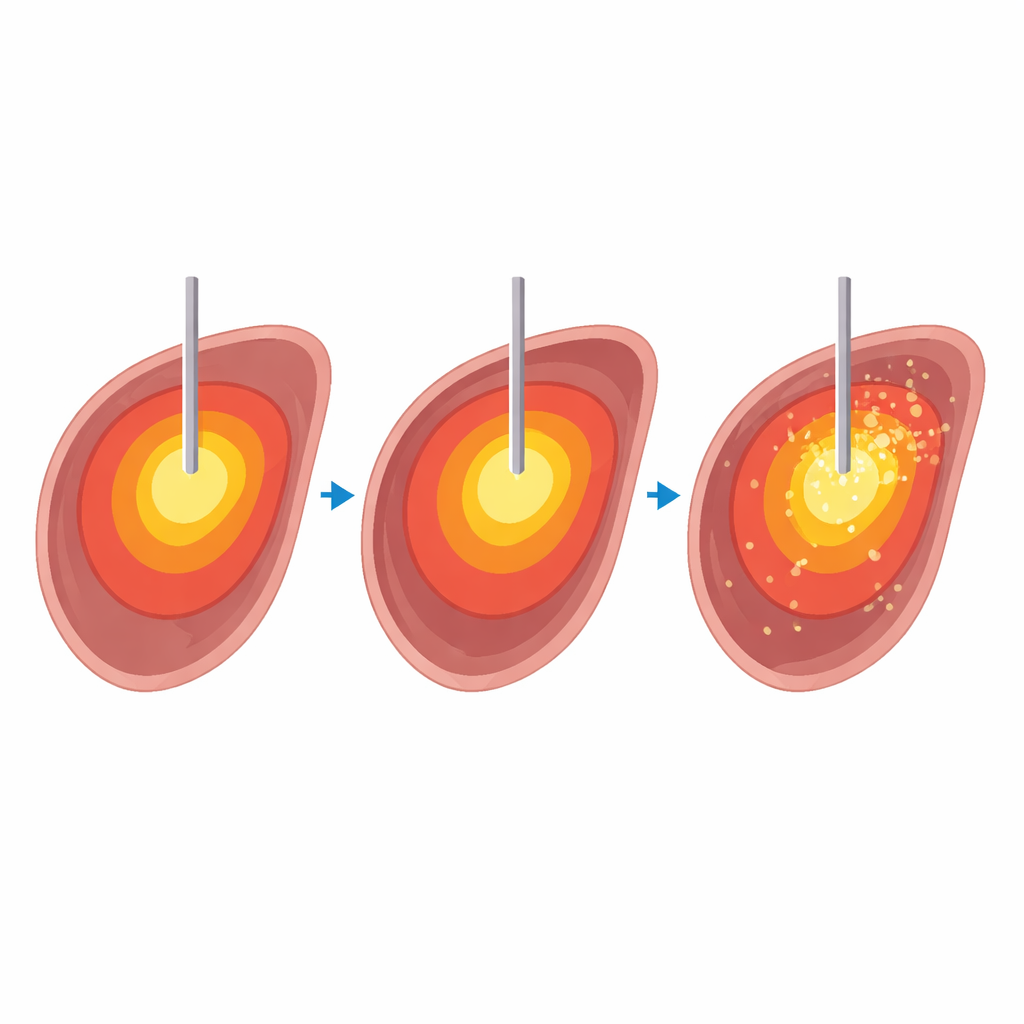
供試動物の肝臓で加熱設定を検証
安全かつ精密に検討するため、チームは屠殺後間もない10頭分のウシ肝臓で計32回のマイクロ波アブレーションを行いました。1.5テスラMRIスキャナ内で、肝組織を目標温度60、80、100、120℃の4段階に、5〜15分の4つの加熱時間で加熱しました。各アブレーション中に高速MRIシーケンスで3次元の温度マップと「熱線量(thermal dose)」マップを数秒ごとに生成しました。加熱後、肝臓は針跡に沿って切開され、肉眼で見える壊死領域の面積を測定し、MRIマップで予測された面積と比較しました。2名の放射線科医が、加熱領域の円形性や規則性、気泡や針によるアーチファクトの影響度を考慮して、MRIマップの品質を5段階で評価しました。
低温の方がマップは鮮明
実験は明確なトレードオフを示しました。高温ほど期待通り壊死領域は大きくなりましたが、MRI温度マップは100℃を超えると著しく劣化しました。より高温ではアブレーションの形状が不規則になり、気泡による歪みで針近傍に低下あるいは負の温度値が現れることがありました。対照的に、60℃と80℃ではMRIマップは滑らかでより円形に近く、組織切片で観察された実際の病変サイズと良く一致しました。統計解析でも、低温時にはMRI推定面積と実際の壊死面積の間に強い相関が確認され、高温ではその相関が弱まるか消失しました。加熱時間を延ばすことで低温による総ダメージを部分的に補えましたが、120℃で得られた最大の病変に完全に匹敵することはできませんでした。
より安全で賢いアブレーションの二段階戦略
これらの結果に基づき、著者らは将来のMRI誘導治療に対する実践的な妥協案を提案します。第1段階として約80℃で15分間の加熱を行うことで、画像品質とアブレーション領域の大きさ、組織学的な細胞死の有効性のバランスが良好であると示されました。より大きな治療領域が必要な場合は、二段階アプローチを勧めます:まず低温のフェーズで明瞭な熱マップを取得して被覆範囲を確認し、配置と余白が満足できると判断したら第2段階で温度を上げて壊死領域を拡大する。第2段階では温度マップの信頼性が低下することを受け入れる必要がありますが、全体としては実用的な戦略となり得ます。
将来の患者ケアへの含意
専門外の読者に向けた主なメッセージは、「温度を少し下げる」ことが、少なくとも制御された実験条件下では、熱を用いるがん治療をより安全かつ精密にする可能性があるという点です。低めの目標温度はMRI温度マップをはるかに鮮明にし、実際にどこが壊死したかを把握しやすくしました。欠点は、低温では壊死領域が小さくなるため、大きな腫瘍にはより長時間の治療や多段階の治療が必要になり得ることです。本研究は血流や呼吸運動のない非生体の動物肝臓で行われたため、患者での追加検討が必要です。それでも、本研究はMRIを単に針の誘導に使うだけでなく、焼灼をリアルタイムで監視・微調整するプロトコル設計に道を開き、肝腫瘍患者の治療成績向上に寄与する可能性を示しています。
引用: Nardone, L., Tan, A.S.M., Bour, P. et al. Quantitative ex vivo assessment of target temperature and ablation duration for protocol optimization of microwave ablation procedures with mr thermometry. Sci Rep 16, 8153 (2026). https://doi.org/10.1038/s41598-026-41656-3
キーワード: マイクロ波アブレーション, MRI温度計測, 肝癌, 熱アブレーション, 画像誘導療法