Clear Sky Science · ja
潜在的な抗がん用途のためのMgドープCuFe2O4ナノ粒子の合成と特性解析
なぜ微小な磁石ががんに効く可能性があるのか
化学療法や放射線治療といったがん治療は、腫瘍だけでなく正常組織にもダメージを与えることがあります。研究者たちは、がん細胞を正常細胞よりも選択的に攻撃するより賢い治療法を探しています。本研究は、鉄、銅、マグネシウムから作られた超小型の磁性粒子を検討し、がん細胞に取り込まれて内部から自滅プログラムを誘導することを目指しています。結果は、粒子の組成やサイズを精密に調整することで、正常細胞を温存しつつ腫瘍細胞に対して特に致死的にできる可能性を示唆しています。
賢い金属粒子の構築
研究チームは、鉄を含む微小結晶「ナノフェライト」の一群を作製しました。これは銅とマグネシウムをさまざまな比率で鉄と酸素と組み合わせたものです。直径わずか約17~30ナノメートルのこれらの粒子は、細胞内に入り込むのに十分小さいサイズです。チームは複数の高性能顕微鏡やX線手法を用いて、粒子が適切な結晶構造を持ち、化学的に純度が高く、おおむね球状のクラスターを形成していることを確認しました。銅とマグネシウムを等量に混ぜた組成では最も小さい粒子が得られ、表面積が増加して化学反応性が高まる傾向があることが分かりました。
がん細胞での粒子の試験
次にチームは、各粒子タイプが培養したヒトがん細胞にもたらす毒性を評価しました。対象は前立腺(PC‑3)、大腸(Caco‑2)、乳房(MCF‑7)、肝臓(HepG‑2)のがん細胞で、比較用に正常な腸細胞も安全性確認として用いられました。3種とも用量依存的にがん細胞を傷害しましたが、その強さは異なりました。銅とマグネシウムを混合した粒子が全体として最も有効で、特に前立腺と大腸がん細胞に対しては比較的低用量で細胞の半量を死滅させました。重要なのは、正常細胞はより高い用量に耐えられたことで、将来の治療に不可欠な選択性が示唆されます。
がん細胞を制御された自己破壊へ追い込む
ナノ粒子がどのように細胞を殺すのかを理解するために、研究者たちはアポトーシス(損傷した細胞が破裂せずに自ら分解していく整然とした死)を調べました。フローサイトメトリーの解析により、処理された前立腺および大腸がん細胞が健常な状態からアポトーシスの初期・後期へ強く移行していることが示されました。ここでも混合銅‑マグネシウム粒子が最も強い効果を示し、処理群の総アポトーシス率は未処理細胞の何倍にも達しました。また、やや増加したネクローシス(より混沌とした細胞死)も観察され、複数の損傷経路が関与している可能性を示唆しています。
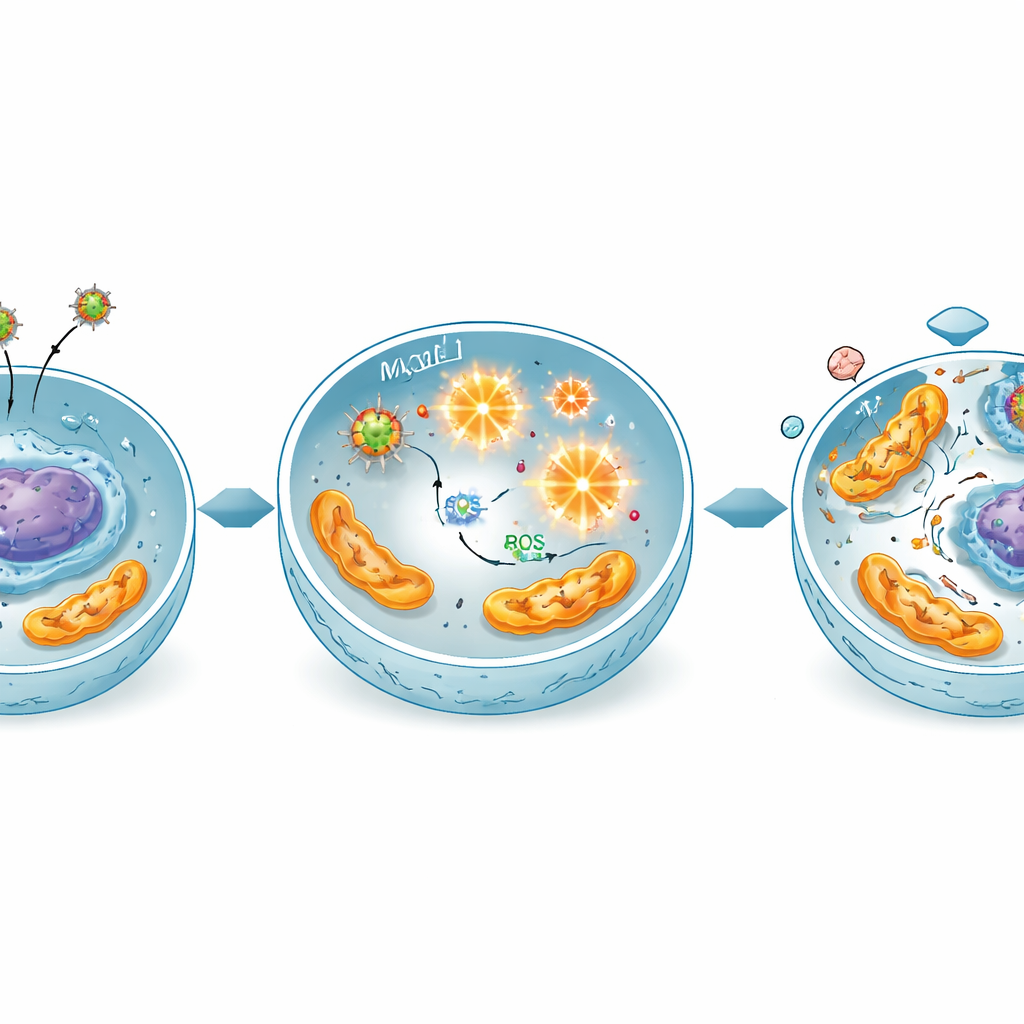
がん細胞を有害な酸素化学で過負荷にする
この効果の中心には化学的な連鎖反応があると考えられます。これらの鉄ベースの粒子は小さな触媒のように働き、細胞内に自然に存在する過酸化水素を高反応性の活性酸素種に変換します。測定では、特に混合銅‑マグネシウム粒子に処理されたがん細胞でこれらの活性酸素の生成が大きく増加していることが示されました。この酸化的な急増はミトコンドリアやDNAといった細胞成分を損傷します。遺伝子発現解析では、細胞死に関わる主要な“守護者”や“実行因子”遺伝子がオンになり、生存や細胞周期に関わる遺伝子は抑えられており、ストレス誘導のミトコンドリア依存アポトーシスという図式と一致しました。
将来のがん医療にとっての意味
総じて、本研究は金属の選択とナノフェライトのサイズ・構造の調整により、がん細胞を強力に自己破壊へと誘導しつつ正常細胞への影響を抑える粒子が作れることを示しています。特に銅とマグネシウムを等量含む組成が最も有効で、その小さな粒径と混合金属化学が細胞内侵入や活性酸素生成能力を高めていると考えられます。これらの結果はまだ細胞培養レベルに限られ、臨床応用からは遠いものの、腫瘍の“自己殺傷スイッチ”を誘導することで全身に広く毒性を及ぼす薬剤に頼らない、より精密なナノテクノロジーに基づく治療への有望な道筋を示しています。
引用: Ali, M., Zein, N., Abdo, M.A. et al. Synthesis, characterization of Mg doped CuFe2O4 nanoparticles for potential anticancer applications. Sci Rep 16, 8276 (2026). https://doi.org/10.1038/s41598-026-41540-0
キーワード: ナノ粒子, がん治療, 活性酸素種, アポトーシス, フェライト