Clear Sky Science · ja
弱教師ありでのソフトな専門家混合型ビジョントランスフォーマーを用いた汎がん種凍結切片分類
手術室でこれが重要な理由
外科医が疑わしい腫瘍を切除する際、通常は短時間でがんが完全に切除されたかを確認する必要があります。病理医は凍結した薄切片を急いで検査し、患者がまだ手術台にいる間に結論を出します。この高圧下のプロセスは、ぼやけた標本、微小な腫瘍、単純な時間制約によって妨げられがちです。本稿で述べる研究は、現実的な病院設備で動作する人工知能(AI)システムが、多臓器にわたって良性と悪性の組織を迅速かつ信頼性高く識別する手助けになる可能性を探っています。
組み込みの課題を伴う迅速な検査
凍結切片解析は現代手術の定番です:薄い組織片を凍結し、切片化して染色し、顕微鏡で良性か悪性か、切除断端が陰性かを判断します。恒久的標本とは異なり、凍結切片は亀裂、折り目、不均一な染色などのアーティファクトが生じやすい。境界例では病理医間で評価が分かれることもあり、時間の制約も常にあります。これらは専門医が限られる小規模病院や多忙な施設で特に深刻で、多数のがん種を少数の専門家でカバーしなければならない状況が生まれます。著者らは、堅牢なコンピュータ支援が凍結切片の判断をより一貫性があり、迅速で、広く利用可能にする可能性があると主張しています。
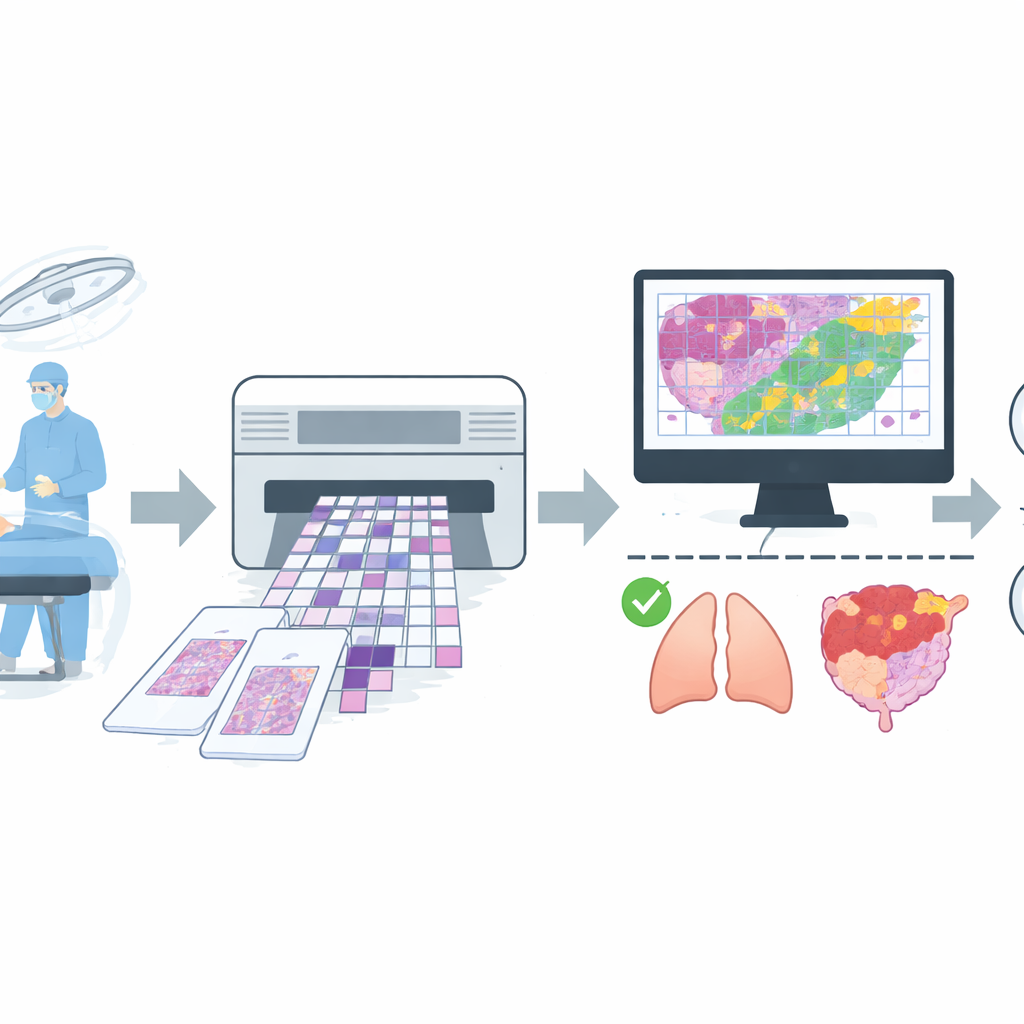
広範で現実的な画像集合の構築
そのような支援を訓練するために、研究チームは大規模な日常診療由来のデジタル画像コレクションを収集しました。主要病院での手術から得られた凍結組織の全スライド画像を4,754枚集め、重大なアーティファクトや診断が不確実なスライドを除外するための厳格な品質基準を適用しました。最終的なデータセットは4,667枚のスライドを含み、各スライドは迅速な凍結読影と後のより注意深い恒久切片報告との一致に基づき、単純に良性または悪性とラベル付けされました。スライドは肺、乳房、甲状腺、リンパ節、女性生殖器などの一般的な部位を網羅し、胃、肝臓、皮膚のような頻度の低い混合グループも含まれていました。データは訓練、ファインチューニング、最終テストのために分割され、同一患者由来の画像が複数のグループに重複しないよう配慮されました。
弱い手がかりからAIが学ぶ仕組み
研究者らは、広大な画像内のパターン検出に優れるビジョン・トランスフォーマーというクラスのニューラルネットワークを基盤にモデルを構築しました。各大きな組織画像は自動的に多数の小さなタイルやパッチに切り分けられ、標準的なグラフィックスハードウェアで処理可能にされました。重要な工夫はネットワークの一部を「ソフトな専門家混合(soft mixture of experts)」に置き換えた点で、これは異なる視覚パターンにそれぞれ注力する多数の小さな専門家ブランチの集合です。専門家をオンオフで切り替えるのではなく、その寄与を滑らかに混合することで、学習の安定化と限られたデータの有効利用が図られます。病理医が腫瘍の輪郭を描いていなかったため、モデルは弱い教師あり学習から学ぶ必要がありました:スライド全体が良性か悪性かだけを知っている状態です。多重インスタンス学習の戦略により、悪性スライド内で最も疑わしいパッチが陽性例として昇格され、ネットワークが徐々に最も情報量の多い領域に焦点を絞れるようになりました。
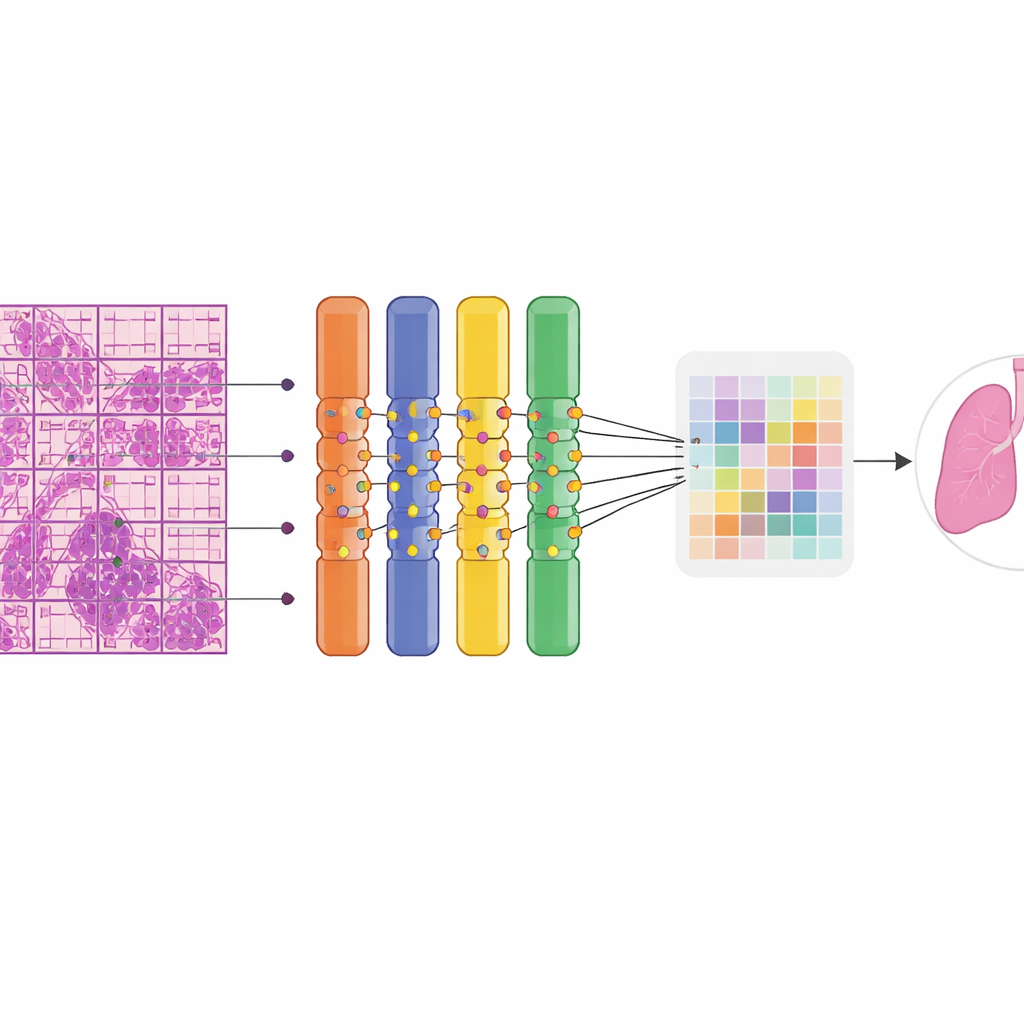
実際の性能
669枚の未見スライドで評価したところ、AIは良性と悪性を高い精度で区別しました。全体で約90%の正答率を示し、確率しきい値を跨いでも両群を優れた能力で分離しました。感度(真に悪性のスライドを検出する確率)は約5分の4程度で、特異度(良性スライドを良性と判定する確率)はさらに高かった。重要なのは臓器横断的に性能が強固であった点で、テストセット内の肺と乳房の悪性例はすべて正しく検出され、女性付属器腫瘍や混合の「その他」臓器のような希少群でも良好な結果を示しました。スライドに重ねたカラー熱マップは、モデルの注目領域が専門病理医が腫瘍と認める領域に集中していることを示し、リンパ節転移巣などを強調しつつ正常構造は大きく無視していました。システムは効率的に動作し、5GB未満のメモリで動作したため、高価なクラスターではなく一般に入手可能なグラフィックスカードでの運用に適しています。
限界、誤判定、改善の余地
著者らはAIが誤る状況も検討しました。偽陰性は極めて希薄な癌細胞、スキャンのぼやけた領域、あるいは悪性巣を覆い隠す強い炎症などで発生しやすかった。偽陽性は、反応性過形成や凍結時の組織変形のように顕微鏡的にがんに類似する良性条件で生じやすかった。ルーチンの外科ワークフローには腫瘍領域の詳細な境界情報が含まれていないため、熱マップが専門家のマーキングとどれだけ一致するかを定量的に示すことはできず、定性的なレビューに頼らざるを得ませんでした。舌や一部の軟部組織腫瘍など一部の臓器タイプは依然としてデータが不足しており、システムの適用範囲を広げるにはより大規模で複数施設にまたがるコレクションが必要であることを示唆しています。
患者と病院にとっての意味
総じて、この研究は慎重に設計されたAIシステムが、手術病理の中核的なタスクである「リアルタイムに組織が良性か悪性かを判断する」支援に対して、正確で解釈可能な援助を提供し得ることを示しています。スライド全体のラベルだけで動作し、広く入手可能なハードウェアで稼働し、医師によるレビューのために疑わしい領域をハイライトすることで、より実用的な凍結切片判定の道筋を示します。患者にとっては単一の手術でより十分な情報に基づく処置につながる可能性があり、専門人材が限られる病院にとっては、高度なデジタルツールがより公平に高品質のがん医療を提供する未来を指し示しています。
引用: Wu, J., Yang, M., Li, J. et al. Pan-cancer frozen section classification using a soft mixture of experts vision transformer under weak supervision. Sci Rep 16, 10297 (2026). https://doi.org/10.1038/s41598-026-40924-6
キーワード: 凍結切片, デジタル病理, がん診断, ビジョン・トランスフォーマー, 弱教師あり学習