Clear Sky Science · ja
エナメル遺伝子のエクソン4由来マイクロRNAがエクソン4のスプライシングとアメロゲニン発現を制御してエナメル形成を調節する
小さなRNAが強い歯にとって重要な理由
歯のエナメル質は人体で最も硬い物質ですが、その形成が乱れると意外に脆くなります。本研究は、miR‑exon4と呼ばれる非常に小さな遺伝物質断片が、歯をつくる細胞にどのように働いて適切に硬化したエナメルを作らせるかを明らかにします。このマイクロRNAが主要なエナメルタンパク質と沈着のタイミングの両方を微調整することを示すことで、細胞内の微細なRNA処理が、遺伝性疾患である先天性エナメル形成不全に似た可視的なエナメル欠損につながることを示しています。
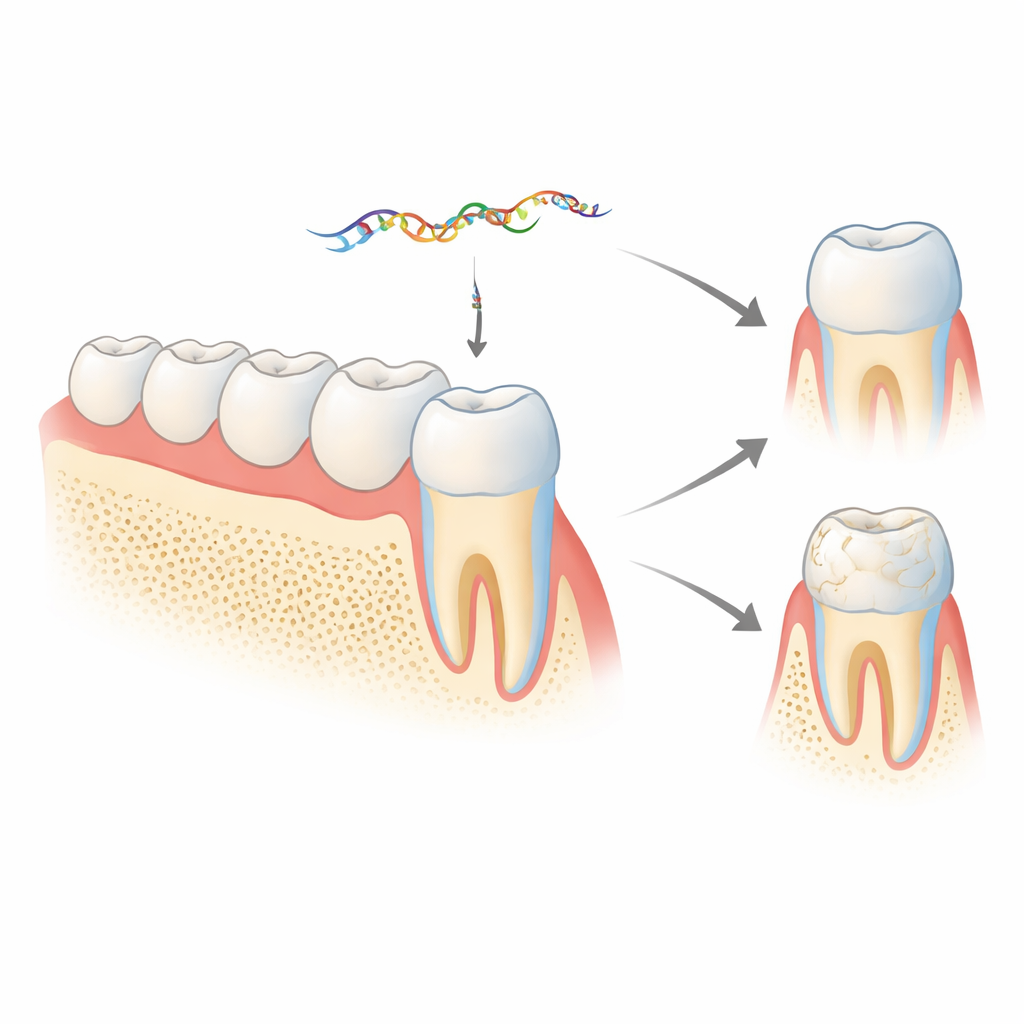
エナメル遺伝子に隠されたメッセージ
エナメルは主にアメロゲニンというタンパク質から作られ、これを分泌する細胞はアメロブラストと呼ばれます。アメロゲニン遺伝子(マウスではAmelx)はさまざまにスプライシングされ、歯の発生段階ごとに必要な複数のタンパク質アイソフォームを生み出します。短いセグメントであるエクソン4は通常最終的な翻訳メッセージから除かれますが、同グループの以前の研究は、排除されたエクソン4がごみではなくマイクロRNA(miR‑exon4)として処理され、骨やエナメルに重要な他の遺伝子を調節できることを示していました。本研究では、このマイクロRNAが減少または阻害されたときに生体内で何が起きるか、そしてそれがアメロゲニン自身の組み立てをフィードバック的に制御するかどうかを問い直しています。
歯形成細胞内の制御連鎖
研究者らはまず、マウスの歯でmiR‑exon4が培養細胞で以前にマッピングした制御連鎖に関与することを確認しました。正常なエナメル器官では、miR‑exon4は上流に位置する2つの遺伝子、NfiaとPrkchを抑えているため、これらが低く保たれると重要な転写因子RUNX2の量が上がります。アメロゲニン遺伝子を欠損したマウス、miR‑exon4を追加したマウス、あるいはmiR‑exon4阻害剤を投与したマウスを用いて、miR‑exon4を減らすとNfiaとPrkchが増加しRUNX2が減少し、逆にmiR‑exon4を加えると反対の効果が出ることを示しました。これにより、miR‑exon4–Nfia/Prkch–RUNX2経路が発生中の歯の中でもin vivoで働くことが確認されました。
乱れたシグナルから弱いエナメルへ
これらの分子変化が実際のエナメルにどう影響するかを見るため、研究者らは歯が活発に形成される1週間の間、マウスの子にmiR‑exon4を阻害しました。三次元X線イメージングにより、処置を受けた動物では切歯と臼歯の両方で高度に鉱化したエナメルが明らかに減少していることが示されました。ヒートマップと染色切片は、エナメル層に沿った鉱化の開始が遅れ、初期鉱化期が短縮されていることを示し、その結果表面が粗くなりエナメルと下位組織の境界がぼやけていました。同時に、アメロブラストにおけるRUNX2タンパク質量は低下し、一方でエクソン4を含むバリアントを含めたアメロゲニンタンパク質は増加しました。このパターンは、エクソン4を含む長いアメロゲニンの過剰産生がエナメル欠損を引き起こすという以前のモデルと一致しており、miR‑exon4の喪失によって誘発されるこのアイソフォーム過剰が正常な鉱化を直接乱す可能性を示唆します。
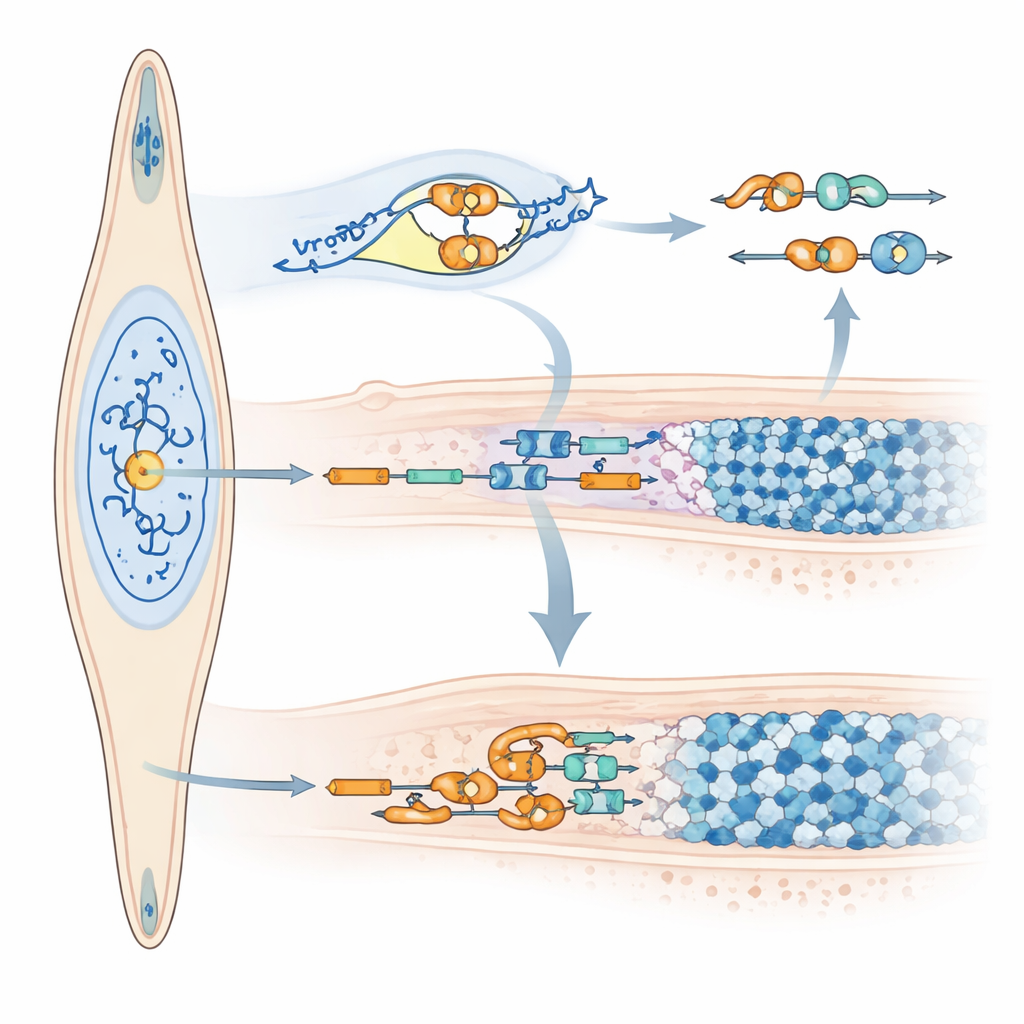
マイクロRNAがエナメルのメッセージをどう変えるか
アメロゲニンの量を変えるだけでなく、miR‑exon4はアメロゲニンmRNAの切断とスプライシングの仕方も変えます。短期的なmiR‑exon4の阻害は、総アメロゲニン量を変えずにエクソン4をまだ含むRNA分子を減少させ、エクソン4がより頻繁に除かれていることを示しました。研究チームはこの変化を複数のスプライシング調節因子遺伝子(SRSF群)の発現変動に結びつけ、miR‑exon4が減ると一部は上がり他は下がることを示しました。miR‑exon4を少なく産生するように改変したアメロゲニン遺伝子を持つ細胞モデルでも、同様にエクソン4のスキップが増えていました。決定的な点として、このマイクロRNA自体がスプライシングが行われる細胞核内に存在し、生化学的試験で隣接イントロンの特定の制御点でアメロゲニン前駆体RNAに結合していることが示されました。これらの発見は、miR‑exon4がスプライシング因子を調整して間接的にエクソン選択を形作ると同時に、エクソン4付近に直接結合してそれが保持されるか除去されるかに影響を与えるという二重の役割を支持します。
エナメルの健康にとっての意味
総じて、本研究はmiR‑exon4をエナメル形成の小さいが中心的な調整者として描きます。適切なレベルで存在すると、miR‑exon4はRUNX2の働きを支え、アメロゲニン産生のバランスを保ち、エクソン4が適切な時点で含まれるか除かれるかを助けます。miR‑exon4が欠如または減少すると、このバランスは崩れ、シグナル経路が乱れ、エクソン4の扱いが誤り、アメロゲニンアイソフォームが偏り、初期のエナメル鉱化が弱まります。これらの知見は、アメロゲニン遺伝子の特定の変異がどのように遺伝性のエナメル障害を引き起こすかを説明するのに役立ち、また核内マイクロRNAが人体で最も硬い組織の形成を形作る重要な役割を果たすことを強調します。
引用: Shemirani, R., Duong, T., Kim, R. et al. A splicing-derived microRNA from amelogenin exon4 regulates enamel formation via control of exon4 splicing and amelogenin expression. Sci Rep 16, 11044 (2026). https://doi.org/10.1038/s41598-026-40706-0
キーワード: 歯のエナメル質, アメロゲニン, マイクロRNA, RNAスプライシング, 先天性エナメル形成不全(amelogenesis imperfecta)