Clear Sky Science · ja
ABE9を融合したSpRY Cas9ニッカーゼによりバイスタンダーのない精密なマウスモデル作製が可能に
より鋭い道具でより良い疾患モデルを構築する
多くの重篤な疾患は、DNAの一文字の誤りによって引き起こされます。これらの病態を理解し最終的に治療するため、研究者はしばしば患者と同じ変異を持つマウスを作製します。しかし、DNAをそのように正確に書き換えるのは意外に難しく、従来の手法はゲノムに傷を残したり、余分な変異を導入して実験結果を曖昧にすることがあります。本研究は、狙った一つの塩基を変更しつつ近接する塩基やゲノム全体をほぼ手つかずに保つよう設計された、ABE9-SpRYと呼ばれる精緻な遺伝子編集ツールを紹介します。
大きな切断から穏やかなDNA調整へ
従来のCRISPR-Cas9編集は分子はさみのようにDNAの両鎖を切断します。細胞はこれらの切断を不完全に修復するため、小さな挿入や欠失が残り、遺伝子が予測できない形で失活することがあります。これは遺伝子をオフにするには有効ですが、正確な疾患原因変異を再現するには向きません。一方、塩基編集機はDNAを切断せず、化学的に一つの塩基を別の塩基に変換します—ここではAをGに変える—ことで二重らせんを保ちます。このアプローチは大きな欠失や再配列を劇的に減らしますが、以前のアデニン塩基編集器には三つの主要な問題がありました:近接する「バイスタンダー」塩基を編集してしまうこと、特定の短い配列タグの隣でしか作用できないこと、そして時に意図しないゲノム箇所で編集を起こすことです。
より選択的な分子ペンの設計
研究者らはこれら三つの制約を同時に克服することをめざしました。まず、非常に狭い範囲に活性を集中させて「編集ウィンドウ」を小さくし、近接する塩基の誤編集を大幅に減らす新しい塩基編集器バリアントABE9を出発点にしました。次にABE9を、SpRYと呼ばれる工学的に改変されたCas9ニッカーゼに融合しました。標準的なCas9が標的部位の隣に厳格な「NGG」配列を必要とするのに対し、SpRYははるかに広い配列を認識できます。これによりこれまで手の届かなかった疾患関連位置にも到達可能になります。こうして得られた融合ツールABE9-SpRYは、高い精度と広いターゲティング柔軟性を両立することを目指しています。
新しい編集器を細胞と胚で検証する
ABE9-SpRYが設計どおりに機能するかを確かめるため、研究チームは広く使われるより積極的な編集器ABE8e-SpRYと比較しました。標的はイオンチャネル(TPC1、TPC2、TRPM4)をコードする遺伝子中の疾患関連位置四箇所で、これらは心臓や肝臓の機能に重要です。培養したマウスの神経細胞では、ABE8e-SpRYが標的塩基をより効率的に編集しましたが、多くの近接塩基も変更しました。対照的にABE9-SpRYは全体の編集数は少なかったものの、「クリーン」な結果—意図した一塩基のみが変更され、局所領域に余計な変異がない—の割合がはるかに高かったのです。同じ傾向はマウス胚でも見られました。受精卵に編集成分を注入した場合、ABE8e-SpRYは標的遺伝子のほぼすべてのコピーを変換することが多かった一方で多くのバイスタンダー変化を伴いました。ABE9-SpRYは全体のコピー数では少なく編集しましたが、作用した箇所では通常、狙いどおりにDNA配列が正確に修正されていました。
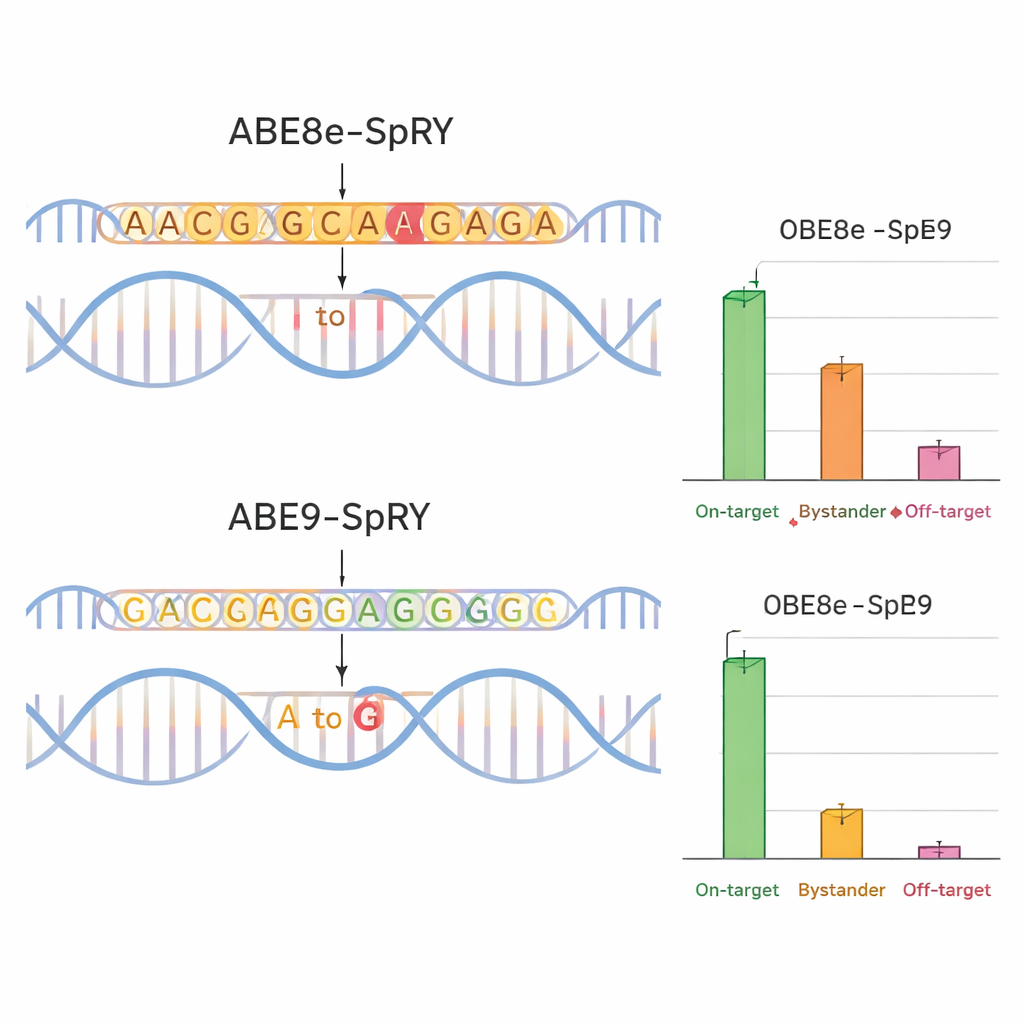
よりクリーンな編集、より少ない副作用
精度は局所的なDNA近傍だけの問題ではありません。チームは編集器がゲノムの遠隔領域を変えていないかも調べました。計算予測と標的シーケンシングを用いて、マウス胚の類似配列が存在する可能性のある部位でのオフターゲット変化を測定しました。ABE8e-SpRYはこれらの位置でしばしば意図しないA→G変換を導入し、時には驚くほど高いレベルに達しました。ABE9-SpRYはこのような事象がはるかに少なく、オフターゲット編集は稀で、Cas9非依存のDNA損傷を検出する特殊な試験でも検出可能な活性はありませんでした。重要なことに、ABE9-SpRYを単独で用いてマウスに二つの特定変異を導入した際、多数の創製動物が得られ、その多くで目的の編集が高頻度で存在し子孫に確実に遺伝し、やはりバイスタンダー変化や小さな挿入・欠失は最小限に抑えられていました。
ヒト幹細胞への精密編集の拡張
患者由来の幹細胞が疾患研究や薬剤評価にますます用いられているため、研究者らはヒトの誘導多能性幹細胞でもABE9-SpRYを試しました。彼らはマウスのサイトに相当する位置のヒトTPC1遺伝子を標的としました。蛍光レポーターで編集細胞を濃縮した結果、ABE8e-SpRYは生の編集率が高かったもののやはり複数の近接塩基を修飾しました。ABE9-SpRYは全体として編集アレル数は少なかったが、完全に正確に編集された配列—意図した変化のみで他に変化がない—の割合は著しく高く、破壊的な挿入や欠失も少なかったのです。クローンを単離して拡大して詳細に調べる幹細胞研究では、この種の「クリーン」な編集は単なる効率の高さより価値があります。
将来の疾患研究にとっての意義
一塩基の変化がどのように疾患を引き起こすかを解明しようとする研究者にとって、余計な意図しない変異は誤解を招く大きな原因となります。本研究は、ABE9-SpRYが生の編集速度ではやや劣るものの、マウスやヒト幹細胞のゲノムに対して一塩基の変化を書き込み、驚くほどの精度と広いターゲット柔軟性を示すことを示しています。これにより、特に一つの余分な変異でも生物学的解釈を混乱させたり治療候補を頓挫させたりする可能性がある状況において、ヒト遺伝性疾患の忠実な動物および細胞モデルを作るための有望な実働ツールとなります。
引用: Ong, J.K., Bhunia, S., Hilbert, B. et al. ABE9 fused to SpRY Cas9 nickase enables precise generation of bystander free mouse models. Sci Rep 16, 7463 (2026). https://doi.org/10.1038/s41598-026-40642-z
キーワード: アデニン塩基編集, CRISPR疾患モデル, マウス遺伝学, オフターゲット効果, ヒトiPSC遺伝子編集