Clear Sky Science · ja
コンピュータ支援創薬技術を用いた潜在的なグリオキサラーゼI阻害剤としてのヒドロキシトリアゾールの発見
小さな“細胞の掃除屋”を止めることががんと戦う手になる理由
がん細胞はしばしば非常に速く増殖するため、自らの廃棄物で溺れてしまうことがあります。彼らの生存トリックの一つは、糖の代謝による有害な副生成物を解毒する内蔵の清掃班です。本研究は、その清掃班の重要な一員である酵素グリオキサラーゼ‑Iをオフにする方法を、数万件の分子をコンピュータでふるいにかけ、有望な候補を実験で検証することで探るものです。目的は、将来がん細胞を内部から選択的に“毒する”手助けとなりうる新しい薬の出発点を見つけることです。
細胞内に隠れた廃棄物処理システム
すべての細胞は常に糖を分解してエネルギーを作り、この過程でメチルグリオキサールという反応性のある廃棄物が生じます。通常は、私たちの体はグルタチオンを助け分子として用いる二段階のグリオキサレーゼ系によってメチルグリオキサールを無害な乳酸に変換します。グリオキサレーゼ‑Iはこの連鎖の最初で最も重要な段階です。糖を猛烈に消費するがん細胞は、メチルグリオキサールが有毒レベルに達するのを防ぐためにグリオキサレーゼ‑Iに強く依存しています。この酵素が阻害されるとメチルグリオキサールが蓄積し、損傷を受けた細胞をプログラムされた死へと導くことがあります。したがって、グリオキサレーゼ‑Iは腫瘍代謝の根本的な弱点を突く抗がん薬の魅力的な標的です。
シリコンと統計で化学空間を探索する
研究者たちはランダムに物質を試す代わりに、コンピュータ支援創薬を使って5万点以上の市販小分子ライブラリを探索しました。専用ソフトはまず各分子をクリーンアップして標準化し、体内に近いpHでの3次元形状と挙動を予測しました。高速のバーチャルスクリーニング段階で各候補がグリオキサレーゼ‑Iの活性部位にどれほど適合するかをスコア化し、続いてサイズ、溶解性、その他の薬物らしさに関する簡単なルールで体内で働きそうにない分子を除外しました。さらに詳細なドッキングプログラムで、有望な分子が酵素内部でどのように向きをとり、特にグリオキサレーゼ‑Iの化学の中心に位置する亜鉛金属原子にどのように到達して掴むかを検討しました。
酵素の金属コアを掴む新しい方法
これまでのグリオキサレーゼ‑I阻害の試みは、金属に結合しやすいが安定性に欠けたり望ましくない副作用を引き起こすことのあるカルボン酸やヒドロキサム酸といったよく知られた化学基に着目してきました。本研究では代わりに、別種の「金属を掴む」ユニット、ヒドロキシトリアゾール環を見いだしました。購入と実験のために選ばれた上位16分子のうち、この環を持つ一つ(コード名SPB07393SC)が際立っていました。仮想ドッキングでは、そのヒドロキシトリアゾール基が亜鉛原子に到達し、二つの芳香環は酵素の近くの疎水性ポケットに収まっていました。数十ナノ秒にわたる複合体のコンピュータシミュレーションは、この分子が安定した距離、凝縮したタンパク質形状、持続的な水素結合ネットワークを伴ってしっかりと結合し続けることを示唆しました。
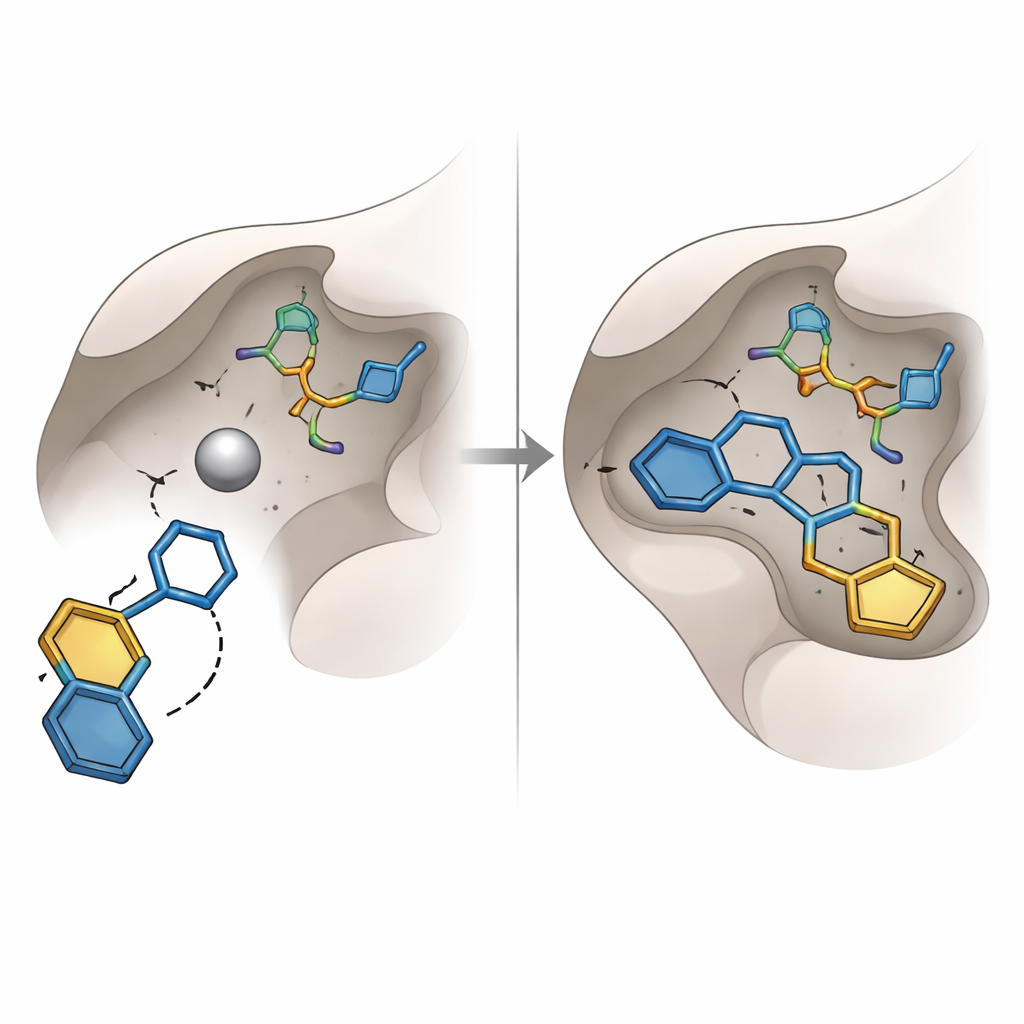
予測を実際に試す
コンピュータモデルが実世界でも効果を示すか確かめるため、チームは選択した分子が精製ヒト・グリオキサレーゼ‑Iの活性をプレートアッセイでどれだけ遅らせるかを測定しました。16候補中15は試験条件下でほとんど抑制効果が見られず、静的なドッキングスコアのみに頼ることの落とし穴を浮き彫りにしました。対照的にSPB07393SCは酵素を強く阻害し、中等度マイクロモーラー濃度での効力を示し、完成した薬というよりは堅実な初期“ヒット”に相当します。追加のソフトウェア解析は、この分子が許容できる溶解性、良好な吸収、必要なら脳に到達する能力、特定の遺伝子毒性や肝毒性を引き起こす可能性の低さを示唆しましたが、これらの安全性予測は実験的確認を必要とします。
将来のがん治療薬にとっての意義
この研究は、グリオキサレーゼ‑Iの中心にある亜鉛原子に薬物候補を固定する新たな手法としてヒドロキシトリアゾールを紹介し、創薬者が利用できる化学的工夫の選択肢を広げました。SPB07393SC自体は出発点にすぎませんが、酵素阻害力、予測される薬物様の挙動、運動を伴うシミュレーションでの安定した結合という組み合わせは、さらなる最適化に向けた有望なスカフォールドと位置づけられます。より広く見れば、本研究はコンピュータ主導のスクリーニングの強みと限界の両方を示しています。膨大な化学ライブラリを短時間で現実的な候補へと絞り込めますが、どの分子が実際にがん細胞の毒性廃棄物管理に必要な酵素を無効化するかを明らかにするには、慎重な実験が依然として不可欠です。
引用: Al-Qazzan, M., Al-Balas, Q., Alnajjar, B. et al. Discovery of hydroxytriazole as a potential glyoxalase-I inhibitor utilizing computer-aided drug design techniques. Sci Rep 16, 9945 (2026). https://doi.org/10.1038/s41598-026-40497-4
キーワード: グリオキサラーゼ I, がん代謝, コンピュータ支援創薬, 亜鉛結合阻害剤, 分子ドッキング