Clear Sky Science · ja
刺激応答性キトサン被覆フェライトナノキャリアによる標的性カプサイシン送達とコア依存のHepG2選択的生物活性
隠れた力を持つ香辛料
唐辛子は料理に辛みを与えるだけでなく、その辛さはカプサイシンという天然化合物によるもので、がん細胞を死滅させることもあります。しかし医薬品としての利用は難しく、水に溶けにくい、体内で速やかに消失する、高用量では健康な組織を刺激する、といった問題があります。本研究は、その刺激的な分子を小さく賢い粒子の中に収めることで扱いやすくし、カプサイシンを血流中で安全に運び、主に肝腫瘍内で放出する方法を探っています。
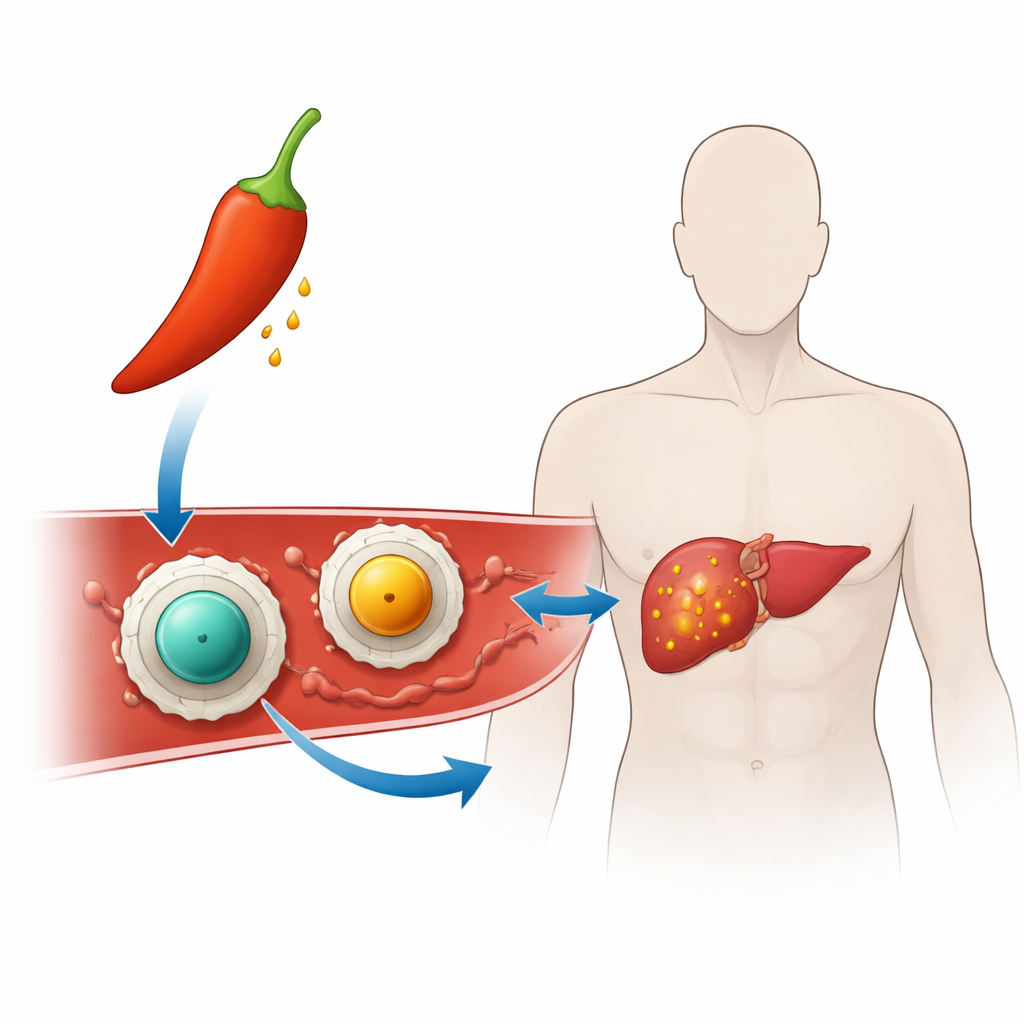
唐辛子を標的治療に変える
研究者たちは「ナノキャリア」を構築しました。これは砂粒より何千倍も小さい粒子で、カプサイシンをがん細胞まで運びます。各ナノキャリアはフェライト(亜鉛フェライトまたはマンガンフェライト)のような磁性鉱物からなる固いコアを持ち、その周りにキトサンという甲殻類由来の糖様物質の薄い被膜が巻かれています。キトサンは医療や食品製品でも用いられており、この被膜により粒子は水中で分散しやすくなり、細胞表面やDNAに付着しやすくなります。カプサイシンをこのキトサン殻に搭載することで、薬を安定に保ち、腫瘍内の過酷な環境に到達するまで隠しておけることを期待しました。
腫瘍環境でのスマートな放出
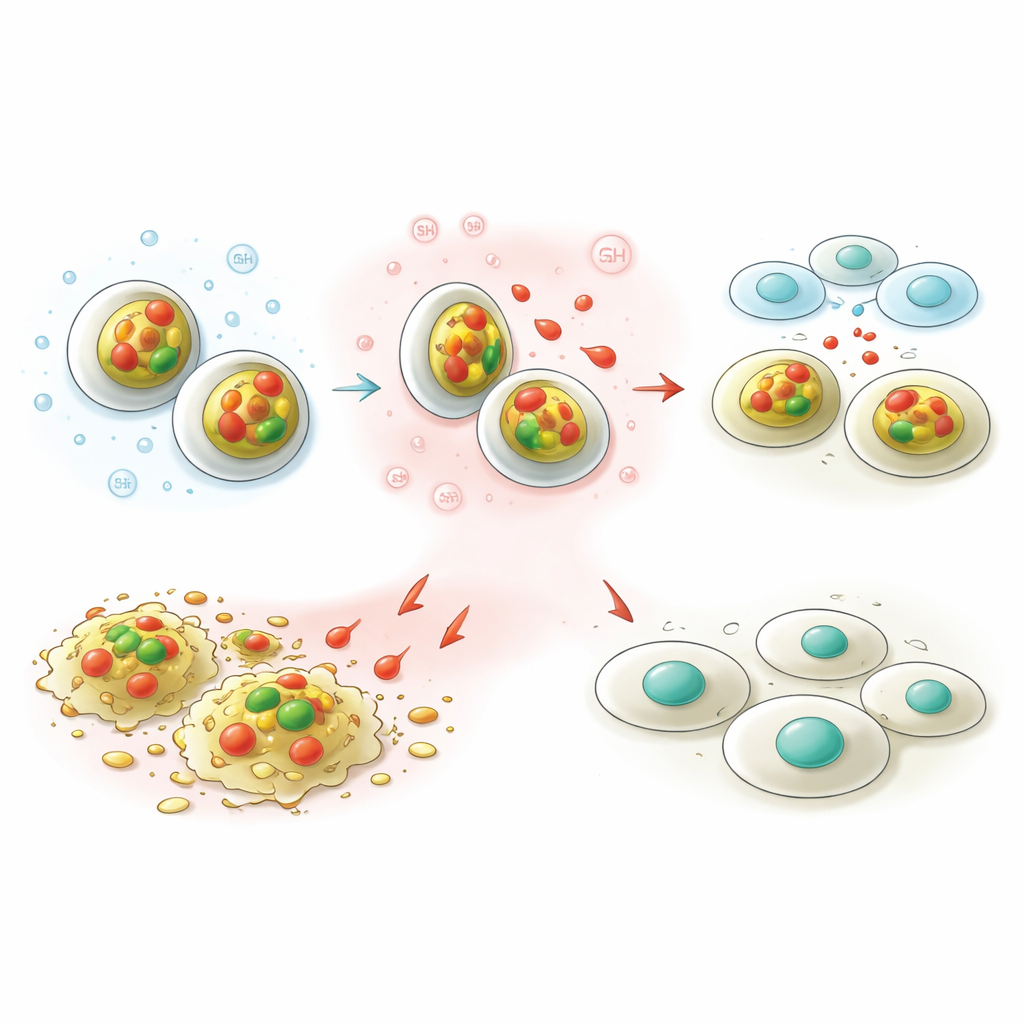
腫瘍の重要な特徴は、正常組織より酸性であり、グルタチオンのような特定の抗酸化物質が豊富であることです。研究チームはナノキャリアがこれらの条件を感知するよう設計しました。通常の血液pHの実験では、2日間で貯蔵したカプサイシンの10%未満しか漏出せず、循環中に貨物を安全に運べることが示唆されました。一方、腫瘍様の条件(より酸性でグルタチオンが豊富)では、粒子は約3分の1のカプサイシンを放出しました。この「オン・オフ」挙動は、薬が経路上で散逸するよりもがん細胞内で放出されやすくなることを意味し、有効性を高めつつ副作用を減らす可能性があります。
粒子の成分が安全性と性能に与える影響
遠目には2種類のナノキャリアは似て見えましたが、内側のコアは実際に違いを生みました。亜鉛ベースの粒子は小さめでカプサイシンをより強く保持する傾向があり、マンガンベースの粒子はより多孔質で薬を放出しやすい傾向がありました。両タイプとも強い正の表面電荷を持ち、細胞やDNAの負電荷表面と相互作用しやすくなっています。ヒト血液を用いた試験では赤血球への損傷は非常に低く、未充填の粒子は正常な肺細胞に対して穏やかであり、基本的な安全性が支持されました。カプサイシンを搭載するとどちらの系も肝がん細胞に対してより強力になりましたが、マンガン版は癌細胞へのダメージを強めつつ正常細胞への影響は比較的抑えるという最良のバランスを示しました。
がん以外の付加的保護効果
ナノキャリアはカプサイシンを運ぶだけではありませんでした。いくつかの実験では標準的な抗生物質と同等の効果で病原性細菌の増殖を抑制し、炎症や組織損傷に結びつく有害な活性酸素種を中和するのにも役立ちました。光学的に注意深く測定すると、カプサイシンがフェライト–キトサン粒子に詰められると、DNAへの結合がより強く、より安定になることが示されました。速い動力学実験は二段階の過程を明らかにしました。まずDNAは正に帯電した粒子表面に取り付く。その後、複合体が再配列してより緊密で長持ちする結合へと移行します。これらの強化された相互作用は、搭載粒子が単独のカプサイシンやフェライト粒子よりも抗がん、抗菌、抗酸化作用で強い効果を示す理由を説明している可能性があります。
患者にとっての意味
現時点では、これらの知見は培養皿での実験に基づくものであり、患者での結果ではありません。それでも、精巧に設計されたナノキャリアがスパイス由来の成分をより精密ながん治療へと変え得ることを示唆しています。適切なコア材と殻を選ぶことで、研究者たちはカプサイシンを安定に保ち、血中で安全に運び、特に肝がん細胞のような腫瘍様条件下で優先的に放出する小さな包装を作り出しました。検討されたデザインの中では、マンガンベースの粒子が標的性の高い抗腫瘍効果、正常細胞への低い害、そして抗菌・抗酸化の付加的利益という点で最も有望な組み合わせを示しました。今後の動物実験や安全性試験が進めば、このような“スマート”な唐辛子由来粒子は、いつか肝がんや他の疾患に対するより穏やかで焦点を絞った治療法の一助となる可能性があります。
引用: Bakr, E., Elshami, F.I., Okba, E.A. et al. Stimuli-responsive chitosan-coated ferrite nanocarriers for targeted capsaicin delivery and core-dependent HepG2-selective bioactivity. Sci Rep 16, 8957 (2026). https://doi.org/10.1038/s41598-026-40433-6
キーワード: カプサイシン, 肝臓がん, ナノ粒子, 標的化薬物送達, 刺激応答性キャリア