Clear Sky Science · ja
天然のグリコRNAのレクチンを用いた検出と発現プロファイリング
RNAは糖衣をまとっている
私たちの細胞には膨大な数のRNA分子が存在し、遺伝情報をタンパク質へと変換するメッセンジャーとして知られています。近年、驚くべき発見がありました:一部のRNAは複雑な糖鎖で飾られ、細胞の外側にも現れるようです。これらの「糖でコーティングされた」RNA、すなわちグリコRNAは、免疫細胞の移動、がんの転移、感染に対する身体の応答に影響を与える可能性があります。本稿で要約する研究は、これら検出の難しい分子を見つけるためのより簡便な方法を提示し、体内でどこに現れるかをマッピングして、診断や治療への新たな道を拓いています。
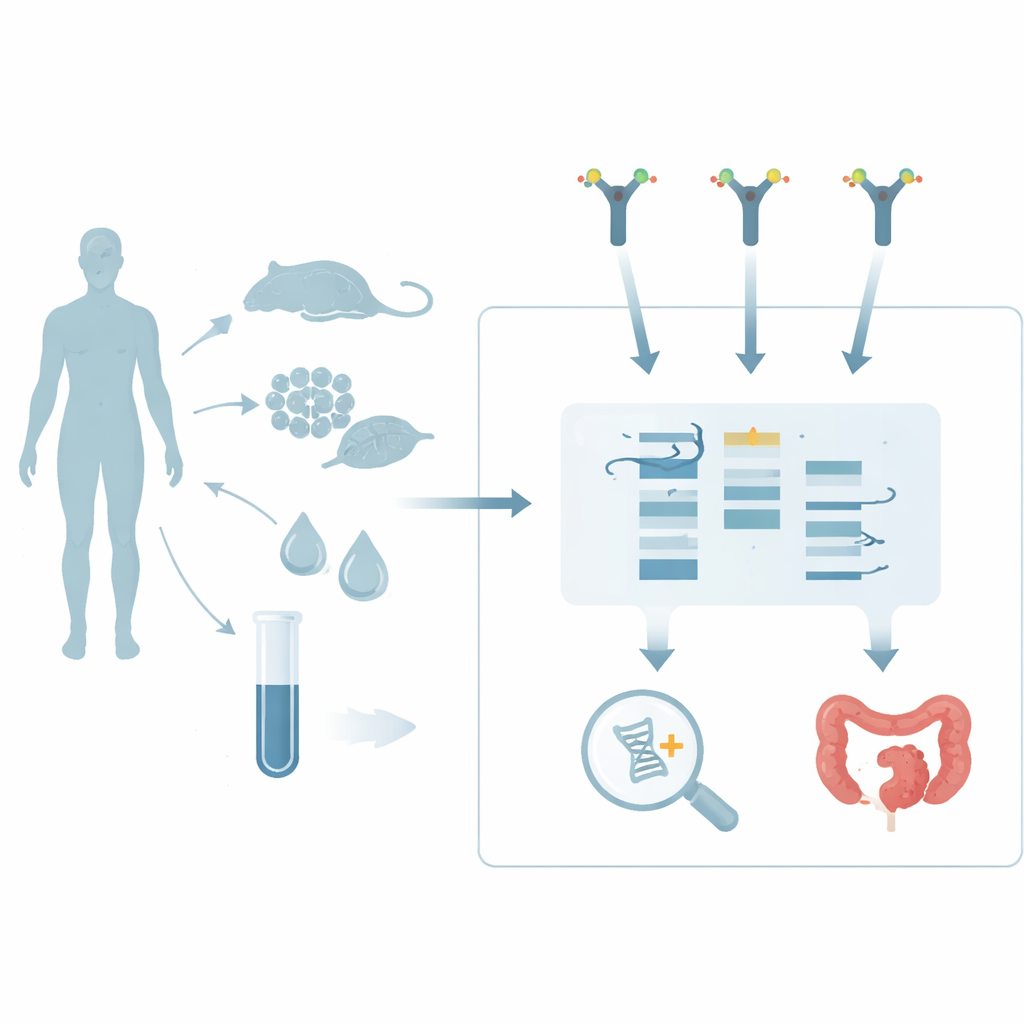
糖で覆われたRNAを見つける新しい方法
これまでグリコRNAを見つけるには高度な技術を要しました。ある方法では、生細胞や動物に人工の糖の構成要素を取り込ませ、合成された新しい糖鎖に後からタグを付けて可視化します。別の方法であるrPALは、精製されたRNA上の特定の糖を化学的に改変して検出できるようにします。どちらの手法も感度は高いものの欠点があります:一方はプローブを取り込む生体系に依存し、もう一方は特定の糖末端を持つグリコRNAの一部しか検出できません。本論文の著者らは、抽出したRNAに直接作用するより簡便な代替法を開発しました。彼らの手法であるレクチンを用いた検出(LBD)は、特定の糖形状を認識する天然のタンパク質であるレクチンがブロット上でグリコRNAに結合する性質を利用し、抗体がタンパク質に結合するのと同様に可視化します。
シンプルな実験手順の微調整
LBDを構築するために、研究チームはまず培養したヒト単球から総RNAを単離し、標準的なノーザンブロット法で分子量ごとに分離しました。次に、24種類のレクチンをテストして、rPALを参照法として用いながら明瞭なグリコRNAバンドを強調できるかを比較しました。いくつかのレクチンは機能しましたが、トマト由来のLELというレクチンが特に強いシグナルを示し、プローブの第一選択となりました。研究者たちはその後、RNAを膜へ移す方法、膜材質、バックグラウンドの非特異的結合を防ぐブロッキング、インキュベーション時間、使用するレクチン量などのルーチン手順を最適化し、信号が鋭く再現性のあるものになるまで調整しました。それらは一般的な分子生物学の実験室でも扱えるほど手順を簡便に保っています。
感度、特異性、観測対象の確認
重要な疑問は、LBDが感度と真の特異性の両方を備えているかどうかでした。著者らは、異なる量のRNAを用いてLBDをメタボリックラベリング法およびrPALと並行比較し、LBDが総RNAおよそ0.5マイクログラム程度という微量でも検出でき、既存法と同等の感度であることを示しました。特異性を試すために、RNA、DNA、タンパク質、あるいはグリコRNAを飾るN結合糖鎖を切断する酵素でサンプルを処理しました。信号を消したのはRNA自体を破壊する処理と糖鎖を除去する処理のみで、DNAを切る酵素やタンパク質を分解する酵素は影響を与えませんでした。細胞内で糖鎖合成を阻害する薬剤もLBDシグナルを大幅に低下させました。これらの検証により、レクチンベースの方法が汚染物質ではなく糖修飾されたRNAに反応していることが示されます。
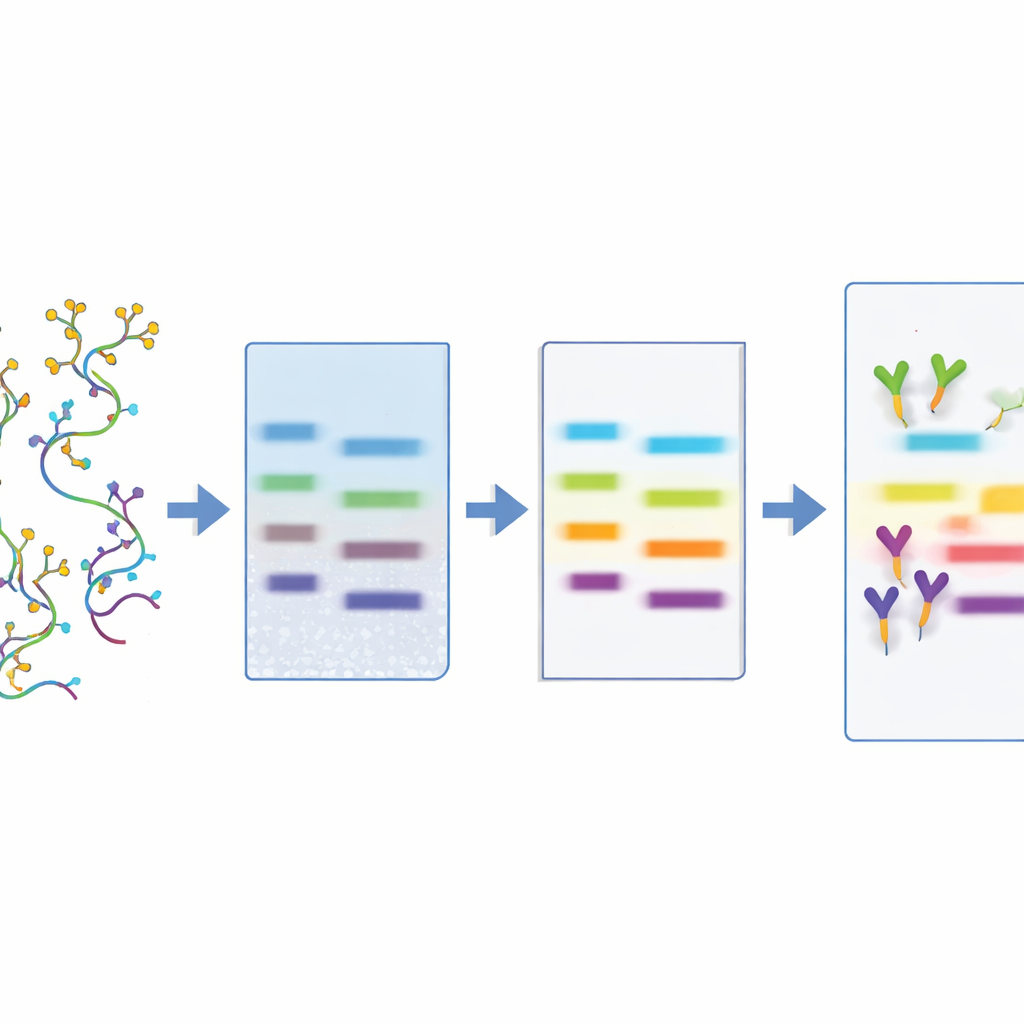
健康と疾患で糖衣RNAはどこに現れるか
手法が確立されたところで、チームはマウス、ラット、人由来の多様な細胞、組織、体液においてグリコRNAがどこに現れるかを調査しました。免疫関連細胞(単球、好中球、白血球など)、外界へのバリアを形成する臓器(腸や呼吸器など)、そして脳や心臓の特定領域で特に強いシグナルが検出されました。興味深いことに、肝臓、腎臓、骨格筋などの主要臓器ではグリコRNAはほとんど存在しないか低レベルでした。LBDはまた、いくつかの組織で複数のバンドを示し、異なるレクチンが異なるバンドのサブセットを認識したことから、多様な糖修飾を持つ複数のグリコRNA「フレーバー」が存在することを示唆しています。重要な点として、著者らはヒトの血漿、尿、糞便、羊水中に遊離のグリコRNAを検出しており、これらの分子が細胞外を循環し、比較的低侵襲な検体で検出可能であることが示唆されます。
がんとの関連と将来の医療応用
研究はまた、がんにおけるグリコRNAパターンの変化にも光を当てました。ヒトの対照組織を用いた比較では、乳がんや結腸がんの腫瘍で正常組織より高レベルのグリコRNAが観察され、転移性疾患で最も強いシグナルが検出されました。転移性乳がんでは、ゲル上でのグリコRNAバンドの移動度が原発腫瘍由来のものとは異なり、疾患進行に伴う構造的変化を反映している可能性が示唆されます。このような腫瘍に関連するバリアントは、攻撃的ながんの識別や標的療法の指針になる可能性があります。LBDは入手しやすい試薬を用い、生体動物でのラベリングステップを避けるため、多数のサンプルを実用的にスクリーニングし、異なる検出法間での比較を行える点で有用です。これにより、各検出戦略が重複するが同一ではないグリコRNA群をどのように強調するかが明らかになります。
日常の健康のためにこれが重要な理由
簡潔に言えば、この研究は細胞間の情報伝達に寄与する新たに認識された分子群を観察するためのツールキットを提供します。特に免疫系や微生物や毒素に直面する体表面での役割が注目されます。単純な糖結合プローブで組織、体液、がんにおけるグリコRNAを信頼性高く可視化できることを示したことで、炎症、感染、腫瘍転移の指標としてこれらの分子を育てるための基盤が築かれました。臨床で使えるより感度の高いアッセイや詳細な機能解析は今後必要ですが、レクチンを用いた検出法は多くの研究室がグリコRNAの分布と役割を探る敷居を大きく下げます。
引用: Li, Y., Qian, Y., Li, X. et al. Lectin-based detection and expression profiling of native glycoRNAs. Sci Rep 16, 9031 (2026). https://doi.org/10.1038/s41598-026-40291-2
キーワード: グリコRNA, レクチンを用いた検出, 細胞表面RNA, バイオマーカー, がん転移