Clear Sky Science · ja
デジタル病理におけるプロトタイプベースの説明可能な有糸分裂検出のための適応的事例選択
がん医療にとっての重要性
病理医が顕微鏡でがん組織を観察するとき、腫瘍細胞がどれだけ積極的に分裂しているかを数えることは、がんの攻撃性や治療方針を決めるうえで重要です。人工知能はデジタルスライド上でこれらの分裂細胞を素早く検出できるようになりましたが、その判断は専門家にとってもしばしばブラックボックスです。本論文は「適応的事例選択(Adaptive Example Selection, AES)」と呼ばれる手法を導入し、AIが過去の実例を示して各判断を支持または反証することで、有糸分裂検出の透明性を高め、臨床的信頼性を向上させる方法を提示します。
分裂細胞を見つける難しさ
有糸分裂像と呼ばれる分裂中の腫瘍細胞は、小さく稀で視覚的に多様です。一般的なピンクと紫の染色では、死にかけた細胞や特定の免疫細胞など、無害な構造と非常に似て見えることがあります。人間の専門家は巨大なデジタルスライドを隅々まで走査してこれらを探す必要があり、その作業は遅く、疲労を招き、評価の不一致が生じやすいものです。最新の深層学習システムはこのタスクで専門家と匹敵あるいは上回る性能を示しますが、各疑わしい細胞に対してスコアを出すだけで、その理由を明示しません。治療決定が患者の人生に大きく影響する医療の現場では、この説明の欠如がAIを日常診療に導入する重大な障壁となります。
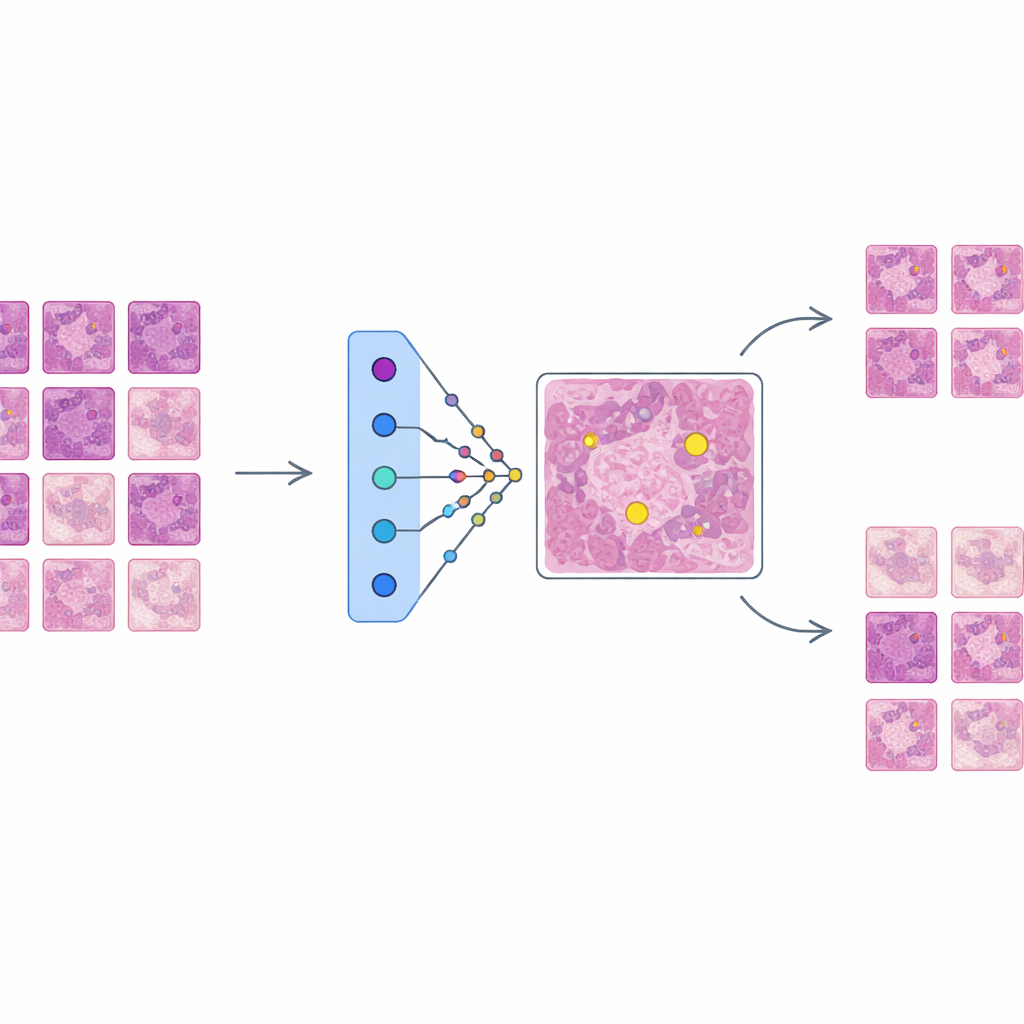
高性能だが不透明な検出器の構築
著者らはまず、Faster R-CNNアーキテクチャに基づく最先端の物体検出ネットワークを訓練し、MIDOG++と呼ばれる大規模かつ多様なデータセットで有糸分裂像を検出するようにしました。これらの画像はヒトおよびイヌの腫瘍から得られ、複数のがん種や研究所にまたがり、1万1千を超える入念にラベル付けされた分裂細胞を含みます。微細構造を保持するためにスライドは小さなパッチに分割され、染色や撮影の実際のばらつきを模した強いデータ拡張が施されます。得られた検出器は腫瘍種を超えて堅牢な性能を示し、F1スコアは最大で0.84に達し、正確である一方で複雑であることが確認されます。まさに臨床で信頼を得るには説明が求められるタイプのシステムです。
事例で自己説明するようにAIを教える
AESはこの訓練済み検出器の上に解釈可能性レイヤーとして置かれ、検出器の動作自体は変更しません。検出器が有糸分裂の可能性があると示した候補領域ごとに、AESは訓練データから取られた実際の組織パッチのライブラリを参照します。そのライブラリから、真の有糸分裂に似た「支持」事例と、非有糸分裂により近い「反証」事例の小さな集合を選び出します。内部的には、AESは検出器の信頼度スコアを滑らかな地形として扱い、ラジアル基底関数と呼ばれる数学的手法を用いて各事例の近傍での信頼度変化を近似します。局所的な信頼度に実質的な影響を与えるプロトタイプのみが保持されるため、単一の判断に対する説明は数百のほとんど無関係な例ではなく、通常約十件の厳選された事例で構成されます。
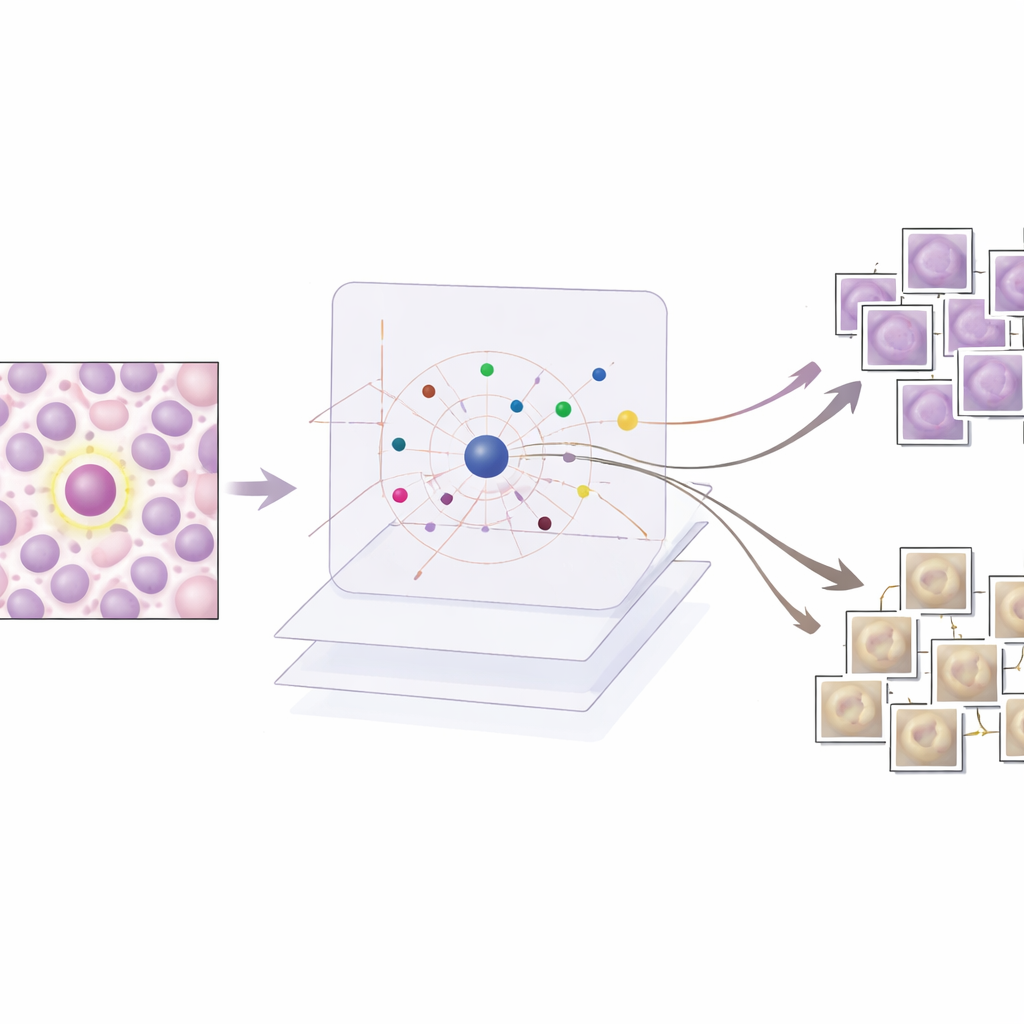
事例が示すAI判断の内実
研究者たちはAESを定量的にも定性的にも評価します。定量的には、およそ190枚のプロトタイプ画像からなる緊密な辞書が検出器の信頼度スコアを非常に高い精度で模倣でき、かつ1件あたりに提示する事例数を人間がレビュー可能な低レベルに保てることを示します。定性的には、三つの典型的なシナリオを検討します。検出器が明確に正しい場合、AESは判断を強く支持する有糸分裂プロトタイプのみを返し、臨床医にとって安心材料になります。誤警報の場合、手法は検出器がテクスチャやクロマチンパターンの類似性に惑わされた理由を示す類似有糸分裂例を提示し、しばしば不確実性を示唆する弱い非有糸分裂プロトタイプを併せて示します。見逃しが起きた場合、AESは主に非有糸分裂プロトタイプや曖昧な例を返す傾向があり、訓練データの盲点を指摘し、どこに新しいあるいはより良いラベル付き事例が必要かを示します。
ブラックボックスから協働ツールへ
各予測を実際にラベル付けされた少数の組織パッチに基づかせることで、AESは複雑なAI検出器を、過去の症例を参照して判断を正当化する人間の同僚のように振る舞わせます。システムは細胞が分裂している可能性を報告するだけでなく、支持・反証プロトタイプの組み合わせと影響度を通じてその理由と確信度を示します。この設計により、病理医は強い予測を素早く確認し、境界的または混乱する領域に注意を集中させ、さらなる訓練を導く体系的な誤りパターンを特定できます。有糸分裂検出のために開発された手法ですが、同じアプローチは他のデジタル病理のタスクにも拡張可能であり、AIを不透明な自動化から、臨床医が問い直し、信頼し、改善できる事例ベースの解釈可能なアシスタントへと移行させる助けになるでしょう。
引用: Banik, M., Kreutz-Delgado, K., Mohanty, I. et al. Adaptive example selection for prototype based explainable mitosis detection in digital pathology. Sci Rep 16, 9481 (2026). https://doi.org/10.1038/s41598-026-40283-2
キーワード: 説明可能なAI, デジタル病理学, 有糸分裂検出, プロトタイプベースのモデル, がん診断