Clear Sky Science · ja
FLASH効果を研究するための電子の直接レーザー加速に基づく超強度パルス状電離放射線源
なぜ超短パルス放射線が重要か
がん放射線治療は綱渡りです:腫瘍を死滅させるのに十分な線量を与えつつ、正常組織に長期的な損傷を与えないようにしなければなりません。最近注目されているFLASH効果は、極めて短く強烈なパルスで線量を与えることで正常組織を温存しながら腫瘍を攻撃できる可能性を示唆します。本研究は強力なレーザーに基づく新しい実験用放射線源を提示し、極めて短時間に高エネルギー電子を生成して、水や生体試料中の酸素が照射中に瞬時に消費される様子を観察します。これはFLASH効果の中心的な過程と考えられています。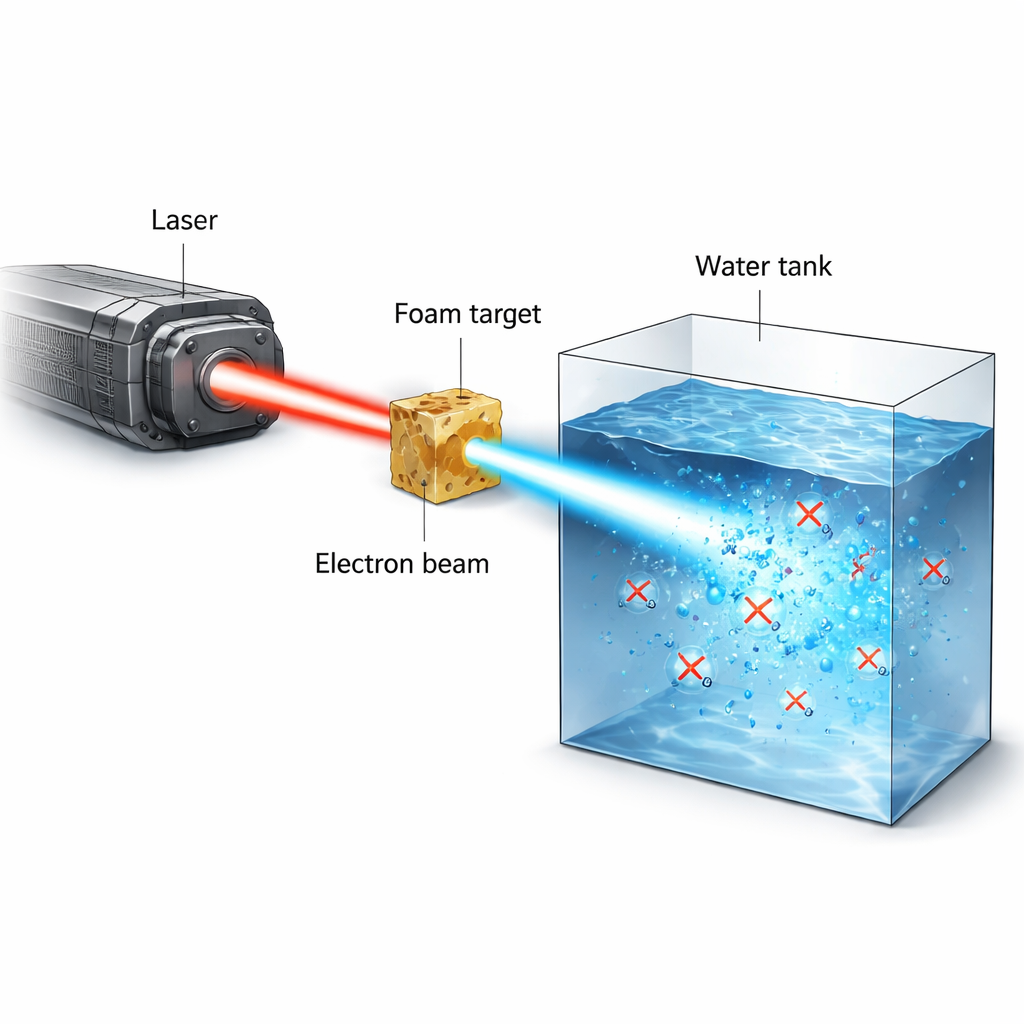
病院の装置からレーザー駆動ビームへ
従来の放射線治療は大型加速器由来のX線、電子、または陽子を用います。これらの装置は通常ミリ秒から秒単位で線量を与え、非常に精密ですが、水分子を分解して反応性酸素種を生成することで間接的にDNAを損傷し、正常組織にもダメージを与えます。血流の良い正常組織に存在する酸素はその損傷を悪化させる——これがいわゆる酸素効果です。FLASH放射線治療は、治療に必要な全線量を非常に短時間に超高線量率で与えることで、動物実験では腫瘍を遮蔽せずに正常組織を一時的に保護することを目指します。しかし、標準的な医療用加速器はこれらの極端な線量率に到達するのが難しく、高出力レーザーなどの代替源の探索を後押ししています。
フォームと光を使って強力な電子バーストを作る
研究チームはPHELIX高出力レーザーを用いて、数MeVのエネルギーを持つ高電流の狭い電子ビームを生成しました。まずレーザーが低密度ポリマーフォームをほぼ臨界密度のプラズマにイオン化します。続くサブピコ秒の超短パルスで、レーザーはプラズマチャネル内の電子を押し込み捕捉して直接高エネルギーに加速します。この過程は直接レーザー加速と呼ばれ、ピコ秒スケールのバーストで数十ナノクーロンの電荷を運べる集束したビームを生み出します。このビームが水や水に類似した物質に当たると、単一ショットで20〜50グレイの線量を沈着させうる—瞬間的な線量率は10^13グレイ/秒を超え、従来装置の到達範囲をはるかに上回ります。
酸素が一瞬で消える様子を観察する
このような強烈なバーストが組織類似条件の化学にどう影響するかを調べるため、チームは真空下で動作し、事前に完全に酸素飽和させた純水、培地、または溶解細胞を充填できる密閉水槽を構築しました。電子ビームは形状やフィルタリングを施され、水槽内の線量が高エネルギー電子で支配されるようにし、陽子やX線は遮蔽層やラジオクロミックフィルムで大幅に抑制または精密に評価しました。水槽内壁に置かれた光学センサーは、染料スポットの発光が酸素分子によって消光される度合いを測ることで溶存酸素を監視しました。各単一パルス照射後、センサーは酸素濃度の急激な低下を記録し、その後酸素がセンサー領域内に拡散するにつれてゆっくりと回復しました。フィルムデータ、シミュレーション、電子の既知の停止力を組み合わせることで、著者らは照射体積に与えられた線量を再構築し、測定された酸素消費と直接結びつけました。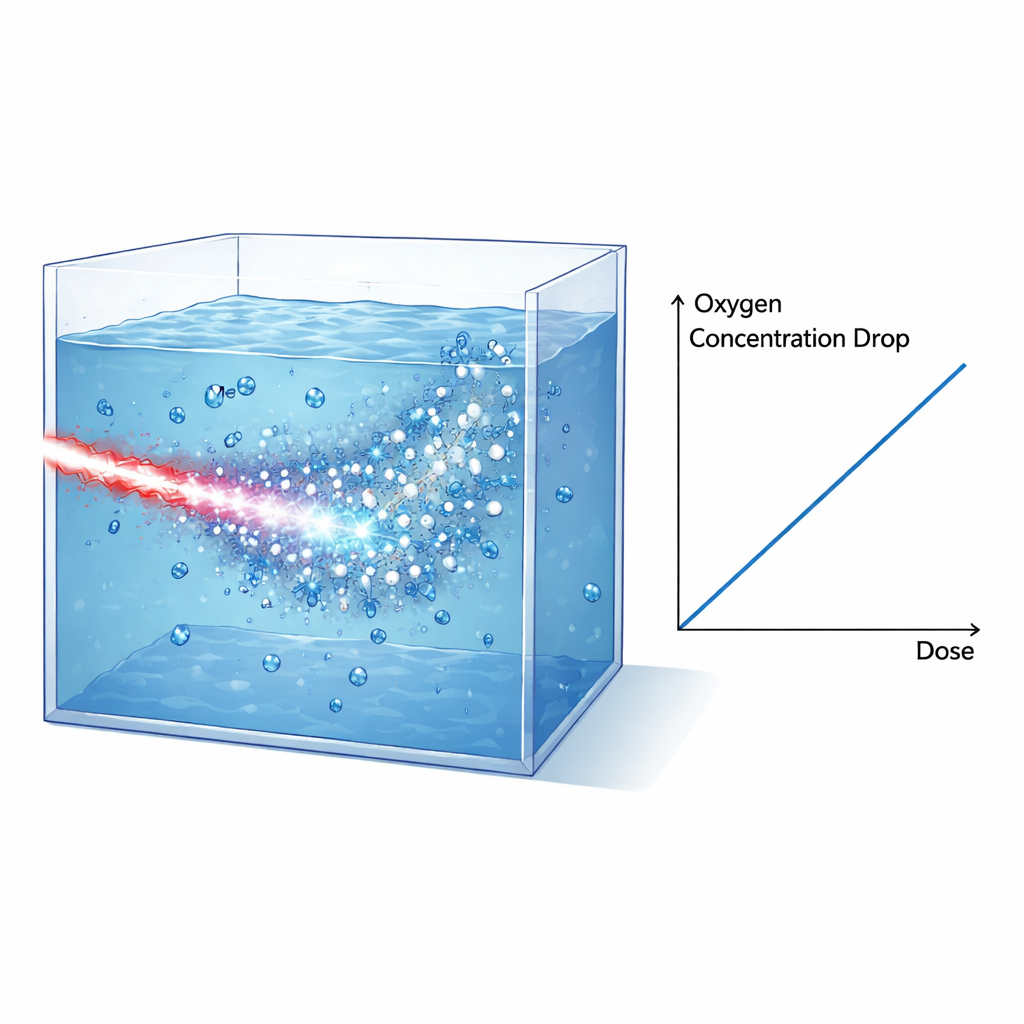
実験と理論を結びつける
重要な発見は、溶存酸素の減少が純水と培地の両方で与えられた線量に比例し、傾きが非常に類似していることです。X線によるわずかな追加線量を補正すると、水中で測定された酸素消費は約0.32マイクロモル毎リットル毎グレイになります。この値は、電子の軌跡を追い、照射後マイクロ秒以内に進行する急速な化学反応をモデル化する詳細なモンテカルロトラック構造シミュレーション(TRAX-CHEM)の予測と極めて良く一致します。重要なのは、このレーザー駆動のセットアップではほぼ全線量が約1ピコ秒以内に与えられる点で、これはその後に続く化学反応の特徴的な時間スケールよりずっと短い。つまり、実験はこれらのシミュレーションで仮定される理想条件をよく再現しており、基礎モデルの厳しい検証になっています。
FLASH研究のためのより良い試験場を構築する
理論の検証にとどまらず、著者らは結果を用いて改良された実験配列を設計します。幾何学を簡素化し、磁石を排し、ビームの周りに水と線量測定フィルムを対称的に配置することで、将来のセットアップでは複雑な再構築をせずに水槽内の線量を直接測定できるようになり、望ましくない陽子やX線の寄与をさらに抑制できます。シミュレーションは、薄いプラスチックや金属の層を追加するなど標的を変更することで、1ショットあたりのおおよその線量を約40〜80グレイの範囲で調整できることを示しており、FLASHに関連する幅広い条件を探る柔軟なプラットフォームを提供します。
将来のがん治療にとって何を意味するか
専門外の読者向けに言えば、本研究の核心はこのレーザー基盤の光源が極めて強烈で超短時間の電子パルスを作り出し、FLASH放射線治療で想定される条件を模倣し、ある点では上回るということです。本研究は、これらのパルスが水や生体試料中の溶存酸素を急速に消費することを示し、その振る舞いは高度な理論予測と一致します。酸素枯渇やそれに伴うラジカル化学はFLASHがなぜ正常組織を保護するかを説明する有力な候補であるため、このように制御可能で十分に理解された光源を持つことは大きな前進です。これはモデルを洗練するための強力な試験場を提供し、最終的には副作用を減らしつつがんをより効果的に治療できる将来の臨床機器の設計を導く手がかりになります。
引用: Gyrdymov, M., Bukharskii, N., Fabian, V. et al. Ultra-intense pulsed source of ionizing radiation based on direct laser acceleration of electrons for studying the FLASH effect. Sci Rep 16, 7164 (2026). https://doi.org/10.1038/s41598-026-40281-4
キーワード: FLASH放射線治療, レーザー駆動電子, 超高線量率, 酸素枯渇, 水の放射線分解