Clear Sky Science · ja
DPAS: 一クラス学習による病原性ペプチド同定のための疾患関連ペプチド異常スコア
なぜ小さなタンパク質断片が健康に重要なのか
ペプチド—短いタンパク質配列—は現代医学で注目を集めています。体内で精密なメッセンジャーとして働くことができ、医薬品や疾患マーカーとしての応用が増えています。しかし、どのペプチドが本当に疾患に結びついているかを特定するには、通常「疾患関連」と「非疾患」の明確な例が必要であり、生物学ではこれが得にくいことがしばしばです。本研究は、既知の疾患関連ペプチドだけを用いて潜在的に有害なペプチドを見つける新しい手法を紹介し、診断や治療の発見をより速く、かつ偏りを抑えて進める道を示します。
「非疾患」群を見つける難しさ
従来の計算モデルは、既知の陽性例(疾患関連)と、無害と考えられる陰性例を比べて学習します。ペプチド研究では、この第二のグループが問題になります。多くのペプチドは単に試験されていないため、「非疾患」とラベル付けすることは誤解を招き、バイアスを生みます。抗がんや抗炎症ペプチドに関する従来研究は高い精度を示しましたが、多くは手作りあるいは推定に基づく陰性データセットに頼っていました。その結果、こうしたモデルは稀なシグナルや、訓練データと似ていない新種の疾患関連ペプチドに対して脆弱である可能性があります。
推定ではなく既知のものから学ぶ
著者らは異なるアプローチを採ります。問題を二面に無理に分けるのではなく、疾患関連ペプチドを一つのまとまりとして扱い、「このグループは詳細に見てどのような特徴を持つか?」を問います。彼らは癌関連データベースから76万点以上の変異ヒトペプチドを収集し、各ペプチドを豊富な特徴量で記述します。これにはアミノ酸の出現頻度やアミノ酸ペアの配列、体積や親水性といった基礎的な物理化学的性質、そしてモチーフと呼ばれる短い反復配列パターンなどが含まれます。主成分分析(PCA)という手法で、この高次元の記述を主要な変動要因を保ちながら扱いやすい形に圧縮します。
一クラスモデルで異常ペプチドを見つける
この圧縮された特徴空間を用いて、チームは三つの「一クラス」モデル—単一群の形状を学習し、それに合わないものを検出するためのアルゴリズム—を訓練します。One-Class Support Vector Machine、Isolation Forest、そしてオートエンコーダと呼ばれるタイプのニューラルネットワークを試しています。オートエンコーダは各ペプチドの特徴を狭い内部表現に圧縮し再構成することを学びます。学習した疾患パターンに属するペプチドは正確に再構成され、異常なものは再構成誤差が大きくなります。正規化した異常スコアを比較すると、オートエンコーダが典型的なペプチドを最も密にクラスタリングし、内部群と外れ値の分離が最も明瞭であることが示されます。再構成誤差の95パーセンタイル付近に閾値を設定すると、モデルは大多数のペプチドを疾患関連の可能性が高いと分類しつつ、少数を一貫して異常として検出します。
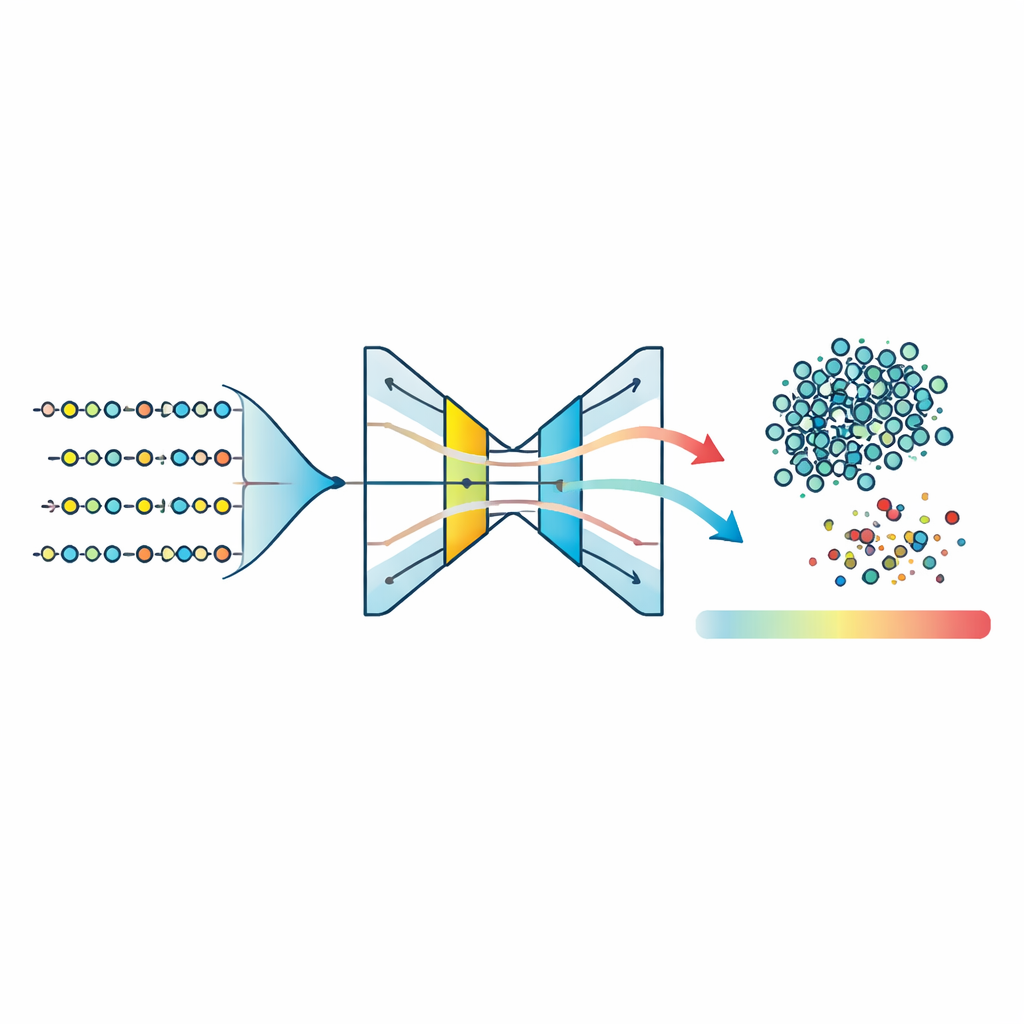
複雑なスコアを単一の意味ある数値に変換する
生物学的に解釈しやすくするため、著者らはDisease Peptide Anomaly Score(DPAS)を導入します。このスコアは二つの要素を組み合わせます:オートエンコーダにとってそのペプチドがどれだけ異常に見えるか(正規化された再構成誤差)と、特徴が予測にどれだけ寄与するかを示す説明手法(SHAP)で計測される貢献度です。実際には、モチーフや特定の物理化学的特性が特に情報量が大きいことが明らかになりました。DPASはこれらの信号を統合し、構造的に異常であり生物学的に意味のある特徴によって裏付けられるペプチドに高いスコアを与えます。上位のペプチドはモチーフ検索ツールで調べられ、リン酸化部位、金属結合領域、シグナル伝達や酵素制御に関わる他の調節パターンといった既知の機能的シグネチャに結びつけられます。
将来の診断や薬への示唆
実務的にいうと、本研究は「どれが確実に無害か」を仮定せずに疑わしいペプチドを見つけるための賢いフィルターを提供します。確認された疾患関連例だけから学習し、DPASで新たな候補をランク付けすることで、研究者は実験検証のために生物学的に妥当性のある短い優先リストを作成できます。上位候補の多くが既知の機能的モチーフを含むことは、それらが疾患過程に関与している可能性を支持します。方法は依然として仮定に依存し、完全な検証のための実験的に証明された「安全な」ペプチドが欠けている点は残りますが、信頼できる陰性例が乏しい他の生物学的データ型にも適用しうる、より現実的で透明性の高いペプチドバイオマーカー探索の基盤を提供します。
引用: Khalid, Z., Khalid, R. & Sezerman, O.U. DPAS: disease-associated peptide anomaly score for identifying pathogenic peptides via one-class learning. Sci Rep 16, 9170 (2026). https://doi.org/10.1038/s41598-026-40099-0
キーワード: 疾患関連ペプチド, 異常検知, オートエンコーダ, バイオマーカー発見, 一クラス学習