Clear Sky Science · ja
RBP4はPI3K/AKTシグナル伝達経路を抑制しマクロファージのM1型極性化を促進することで舌扁平上皮癌の進行に干渉する
舌癌に新しい発想が必要な理由
舌癌は発話、摂食、味覚を奪い得る疾患であり、手術、化学療法、放射線療法を行っても長期生存率が満足できる水準に達しないことが少なくありません。本研究は、血中に存在する意外な助っ人、ビタミンAを運ぶタンパク質RBP4に着目し、それが舌腫瘍の増殖を遅らせると同時に体内の免疫防御を活性化する仕組みを示しています。がん細胞内および周囲の免疫細胞でこの分子がどのように働くかを明らかにすることで、将来的に治療をより効果的かつ侵襲性を低くできる新たな戦略を示唆します。
舌腫瘍に隠れたタンパク質
研究者らはまず、大規模ながん遺伝子データベースを解析し、舌扁平上皮癌の患者予後を予測し得る免疫関連遺伝子を探索しました。数百の候補の中で、血流中でビタミンAを輸送することで知られるタンパク質RBP4が特に興味深い存在として浮上しました。腫瘍サンプルと隣接する健常な舌組織を比較すると、RBP4の発現は一貫して腫瘍側で大幅に低下していました。このパターンは複数の独立したデータセットおよび20例の患者組織サンプルで確認され、RBP4の喪失が本疾患の共通した特徴であることを示唆しました。
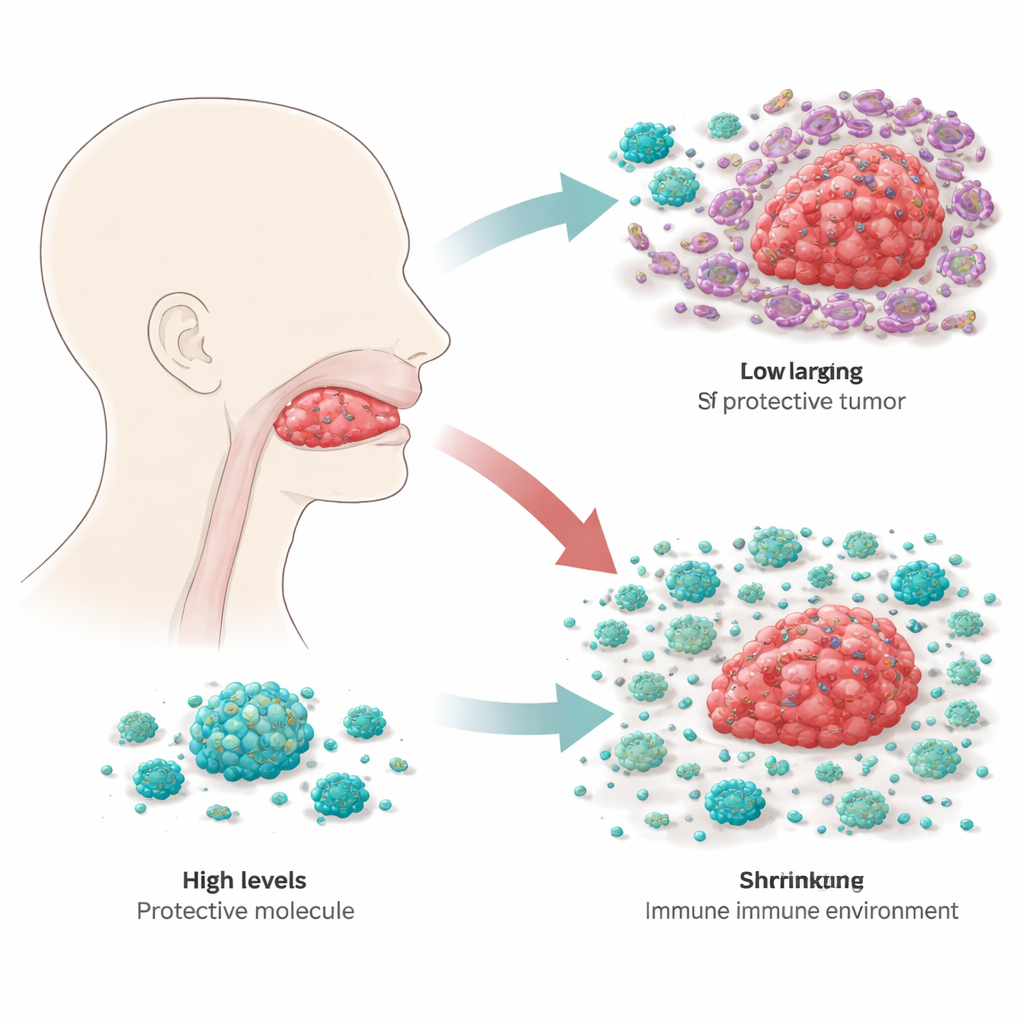
腫瘍内からの成長抑制
RBP4が舌癌細胞内で実際に何をするのかを調べるため、研究者らは腫瘍細胞株を改変してRBP4を過剰発現させるか、著しく減少させる系を作成しました。培養皿上では、RBP4が高い細胞は増殖が遅く、RBP4が減少した細胞は増殖が速く、人工膜を越えて移動・侵襲する能力が高まり、転移や再発に関連する挙動を示しました。これらの改変細胞をマウスに移植すると、RBP4過剰の腫瘍は小さく留まり、RBP4が低い腫瘍はより攻撃的に増大しました。細胞内部の主要な成長制御スイッチを追跡したところ、RBP4は多くのがんが頼る主要な増殖経路であるPI3K–AKT–mTORを抑制していることが示されました。RBP4が高いとこの経路の活動は低下し、腫瘍細胞は遊走に有利な可塑的で移動性の高い状態を取りにくくなります。
免疫細胞を腫瘍殺傷者に変える
がんは孤立して増殖するわけではなく、免疫細胞、血管、支持細胞からなる腫瘍微小環境の中で生きています。ここで大きな役割を果たすのが、腫瘍を攻撃することも助けることもある大食細胞(マクロファージ)です。解析の結果、RBP4が多い腫瘍は炎症と腫瘍殺傷に関与する“M1”型マクロファージが多く含まれる傾向があり、逆に腫瘍増殖を支持しがちな“M2”型が優勢ではないことが分かりました。細胞培養系では、精製されたRBP4あるいはRBP4を分泌するように改変した舌癌細胞に曝露されたマクロファージは、このM1の腫瘍攻撃的な状態へと偏移しました。一方、がん細胞でRBP4が減少していると、マクロファージはより腫瘍寄りの表現型へと傾きました。
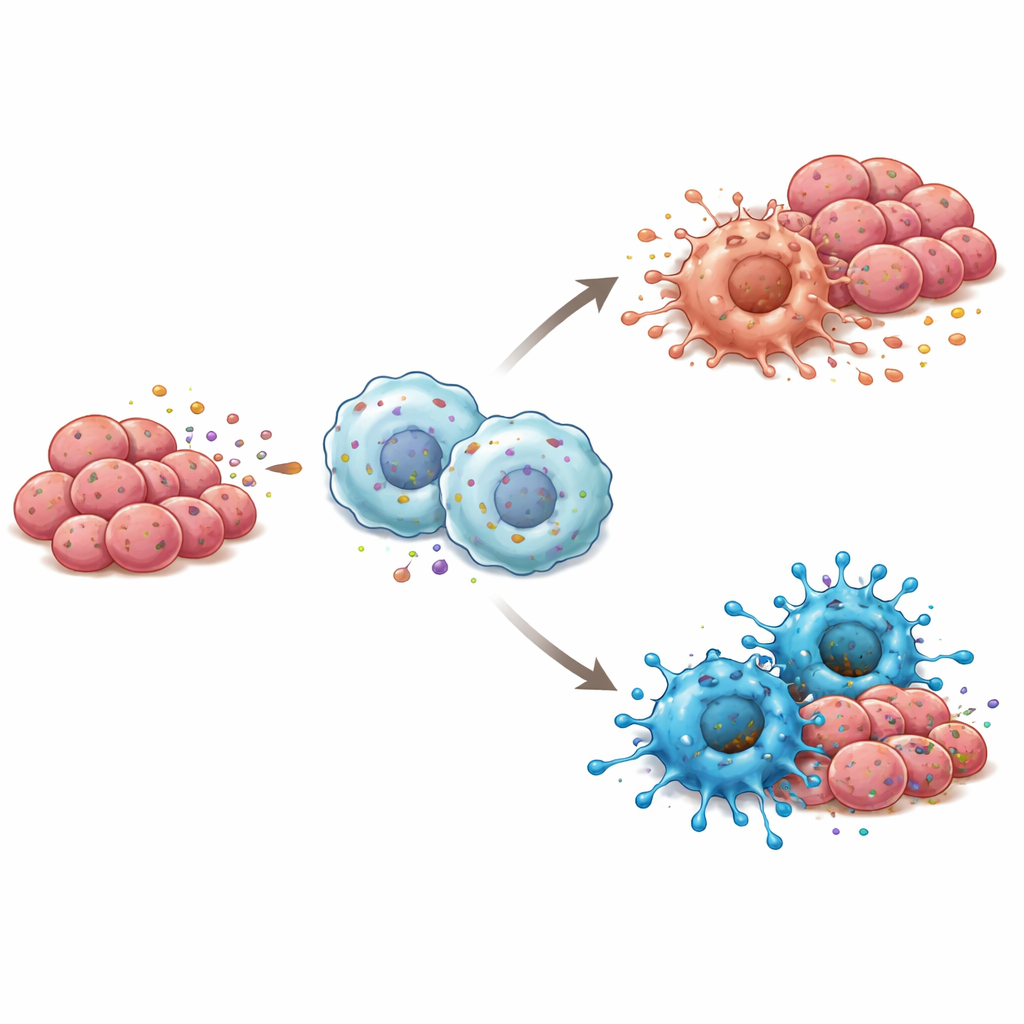
免疫シフトの背後にあるシグナル経路
RBP4がマクロファージを腫瘍に対してより攻撃的な立場に促す仕組みを探るため、研究者らはこれら免疫細胞内でどの内的アラームシステムが作動しているかを調べました。その結果、RBP4はマクロファージ表面のセンサーであるTLR4を刺激し、さらに炎症応答を駆動するマスター・スイッチであるNF-κBを活性化することが分かりました。化学的阻害剤でTLR4を遮断するとこの連鎖反応は止まり、RBP4の存在下でもマクロファージはM1状態を取れなくなりました。マウスモデルでは、RBP4を多く含む舌癌細胞とマクロファージを混合して形成した腫瘍は増殖が遅く、M1型細胞の割合が高く、TLR4およびNF-κB活性も強く観察され、これらの経路がRBP4の免疫効果の鍵であることを補強しました。
今後の治療にとっての意味
総じて本研究は、RBP4を舌癌に対する二重のブレーキとして描いています:腫瘍細胞内部では過剰な成長回路を抑え、腫瘍の周辺ではマクロファージをより警戒する防御者に変えるのです。RBP4が標的とどのように相互作用するか、いかに安全に増強するかといった未解決の問題は残るものの、本研究はRBP4の作用を回復または模倣することが腫瘍拡大を遅らせ、体の免疫的プレッシャーを強化する可能性があることを示唆しています。患者にとっては、腫瘍を切除するだけでなく、その内部配線や局所の“生態系”を再構築して再発を防ぐ将来の治療法の可能性を示すものです。
引用: Yan, Y., Miao, N. & Wang, X. RBP4 interferes with tongue squamous cell carcinoma progression by inhibiting the PI3K/AKT signaling pathway and promoting macrophage M1-type polarization. Sci Rep 16, 9375 (2026). https://doi.org/10.1038/s41598-026-39915-4
キーワード: 舌癌, RBP4, 腫瘍微小環境, マクロファージ, PI3K AKT 経路