Clear Sky Science · ja
PAR1キナーゼファミリーの2つのメンバー、PAR1bとPAR1aの間にある暗黙の冗長性 — PAR1bノックアウトマウスの生存において
破損したDNAに対する細胞の“代替プラン”の見つけ方
細胞は常にDNA損傷に直面しており、修復機構が働かないとがんや発生時の致死につながります。本研究はマウスで見つかった驚くべき救済メカニズムを探ります。すなわち、有名ながん関連遺伝子BRCA1の働きを助ける重要なたんぱく質が欠けたとき、近縁の別のたんぱく質が静かにその役割を引き継ぐという現象です。この研究は、初期胚が生存のために遺伝子制御系をどのように書き換えるかを示し、なぜある遺伝的欠損が致死であり、別のものは思いのほか耐えられるのかについて新たな洞察を与えます。
細胞の構造を整えるファミリーに隠れた役割
研究者らはPAR1キナーゼと呼ばれる酵素群に着目しました。これらは細胞内部の組織化を助けます。メンバーの一つであるPAR1bは、BRCA1を細胞核に誘導し、そこでBRCA1が正確なDNA修復を監督し、脆弱な複製部位を保護することが示されていました。マウスでBRCA1を完全に失うと胚早期に致死になることから、その重要性が裏付けられます。しかし興味深いことに、PAR1bを完全に欠くマウスは成体まで生存します。PAR1bはBRCA1の上流に位置するため、この不一致は別のPAR1キナーゼが特定の条件下でPAR1bの代わりをひそかに務めていることを示唆しました。
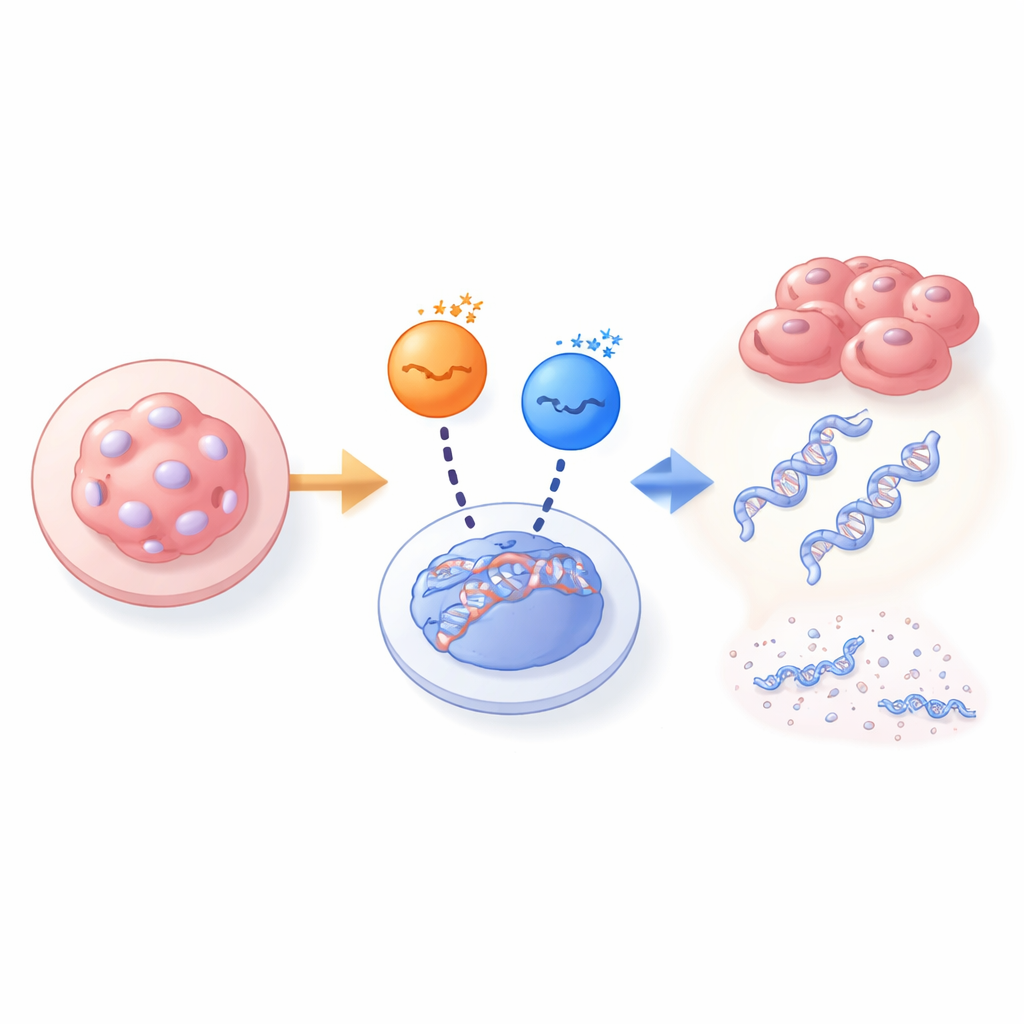
一方のキナーゼが失敗すると、別のものが代わりを務める
この謎を解くため、研究チームは正常胚由来とPAR1bを全く持たない胚由来のマウス胚性線維芽細胞を比較しました。正常細胞ではPAR1bを抑えると核内のBRCA1が著しく減少し、DNA切断のマーカーが急増して細胞増殖が阻害されました。PAR1a、PAR1c、PAR1dといった他のPAR1キナーゼをノックダウンしてもほとんど影響はありませんでした。しかしPAR1b欠損胚由来の細胞では、PAR1bが欠けているにもかかわらず核内にBRCA1が残り、DNAも比較的無傷でした。これらPAR1b-null細胞ではPAR1aを除去することが致死的になり、PAR1cやPAR1dの除去はそうではありませんでした。この依存性の切り替えは、PAR1aがPAR1bのBRCA1誘導の役割を引き継いでいることを示していましたが、それはPAR1bが最初から欠損していた胚でのみ起きていました。
生存戦略としての早期エピジェネティック再配線
研究者らは、この隠れたバックアップ機構がエピジェネティクス、すなわち遺伝子配列を変えずにDNAの包装や化学的な標識で遺伝子のオン/オフを制御する仕組みに結び付くと考えました。クロマチンの開放性を全ゲノムで解析したところ、正常細胞とPAR1b欠損細胞の間でDNAアクセス性が異なる領域が数千箇所見つかりました。多くの変化は染色体の巻きつけや修飾を制御する遺伝子に関わるもので、遺伝子制御ネットワークの広範な再プログラミングを示唆します。顕著な影響の一つは53BP1遺伝子に及びました。53BP1は通常、BRCA1の精密な修復法に対立する手早い修復経路へ細胞を誘導するタンパク質です。PAR1b欠損細胞では53BP1遺伝子本体のクロマチンがより緊密にパッキングされ、そのRNAとタンパク質レベルが大きく低下していました。
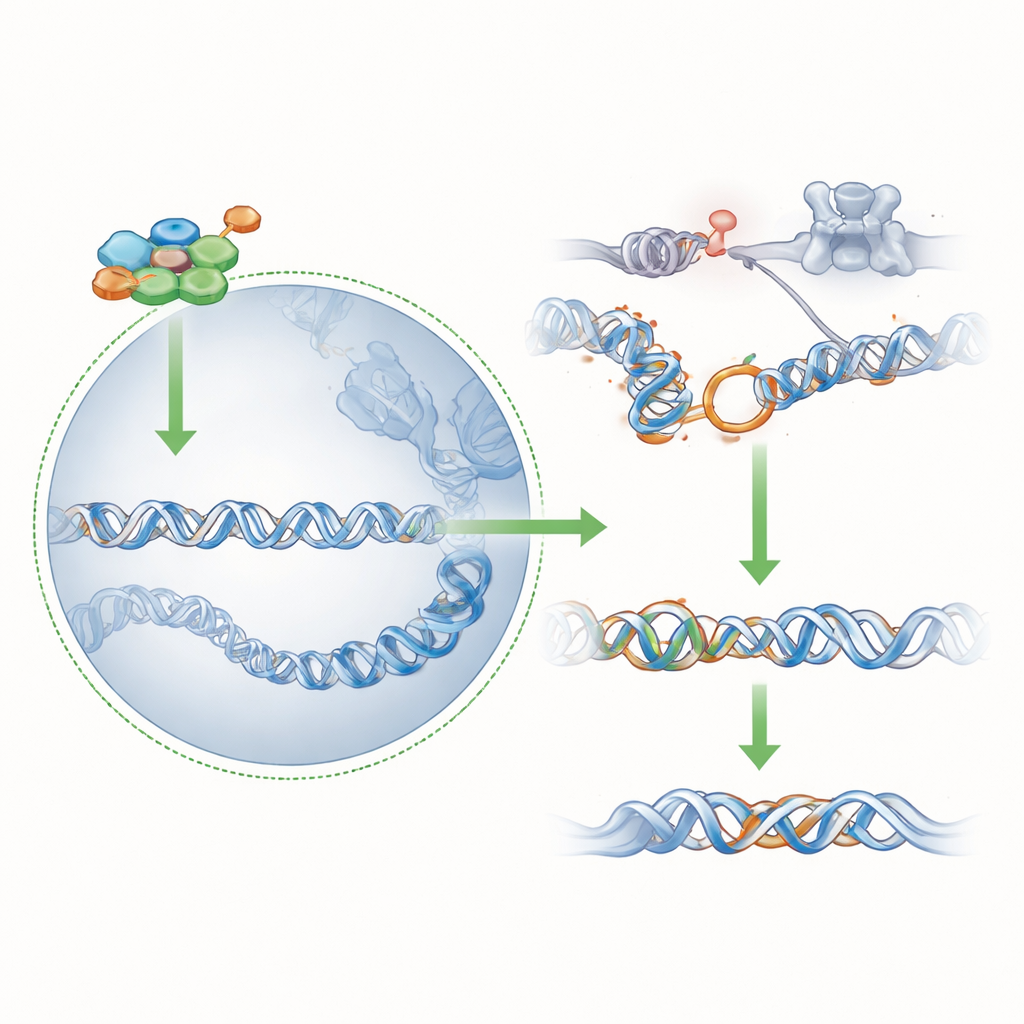
修復経路間のバランスを傾ける
53BP1を抑えることで、胚はBRCA1への完全な依存を実質的に減らします:PAR1bではなくPAR1aによって運ばれる控えめな核内BRCA1の量でも、十分な正確な修復を支えて細胞を生存させることが可能になるのです。全てのPAR1キナーゼを抑える細菌由来タンパク質を用いた実験は、PAR1b欠損細胞におけるBRCA1の核内存在が依然としてPAR1ファミリーの活性、特にPAR1aに依存していることを裏付けました。総じて、結果はPAR1bの早期喪失がクロマチンとDNA修復ネットワークの急速な再形成を誘発し、BRCA1の拮抗因子である53BP1を沈静化し、PAR1aがPAR1bの代役を務められるようにする様子を描き出します。
疾患と治療への含意
本研究は「暗黙の冗長性」という概念を提唱します。これはバックアップ機能が存在するが通常は休眠しており、主要構成要素が発生の非常に早い段階で失われたときにのみ顕在化する、という考え方です。マウスではこれによりPAR1bの喪失がBRCA1の喪失とは異なり胚の生存を可能にします。また、致命的なPAR1b変異をもつ人の一部が生存しているのは類似のバックアップ機構が働くためかもしれないことを示唆していますが、その結果として脳機能、代謝、がんリスクに影響が出る可能性もあります。長期的には、早期のエピジェネティック調整がどのように53BP1を沈黙させ、BRCA1の制御をPAR1bからPAR1aへと移行させるかを理解することで、PAR1bを失った細胞を保護したり、がん治療でDNA修復経路を精密に調整したりするための戦略を生み出す可能性があります。
引用: Murata-Kamiya, N., Del Valle Lazarte, A.A., Kikuchi, I. et al. Cryptic redundancy between PAR1b and PAR1a, two members of the PAR1 kinase family, in the survival of PAR1b-knockout mice. Sci Rep 16, 5971 (2026). https://doi.org/10.1038/s41598-026-39737-4
キーワード: BRCA1, DNA修復, キナーゼの冗長性, エピジェネティック制御, 胚発生