Clear Sky Science · ja
低酸素誘導因子1αはTIMP3を介した血管新生と浸潤の制御を通じて膀胱がん進展に二重の役割を果たす
酸素欠乏の腫瘍が重要な理由
がん細胞はしばしば急速に増殖して血液供給を追い越し、腫瘍の一部が酸素不足に陥ります。この低酸素環境は細胞に生存プログラムのスイッチを入れさせ、がんを治療しにくくすることがあります。泌尿器系の一般的な腫瘍である膀胱がんにおいては、HIF-1αと呼ばれるタンパク質が制御する酸素感知プログラムが主に腫瘍の成長と転移を助けると長く考えられてきました。本研究はその役割を詳しく調べ、驚くべきひねりを発見しました。特定の条件下ではHIF-1αを抑えることで膀胱がん細胞がむしろより攻撃的になることがあり、その逆説の中心にあるのが別のタンパク質であるTIMP3です。
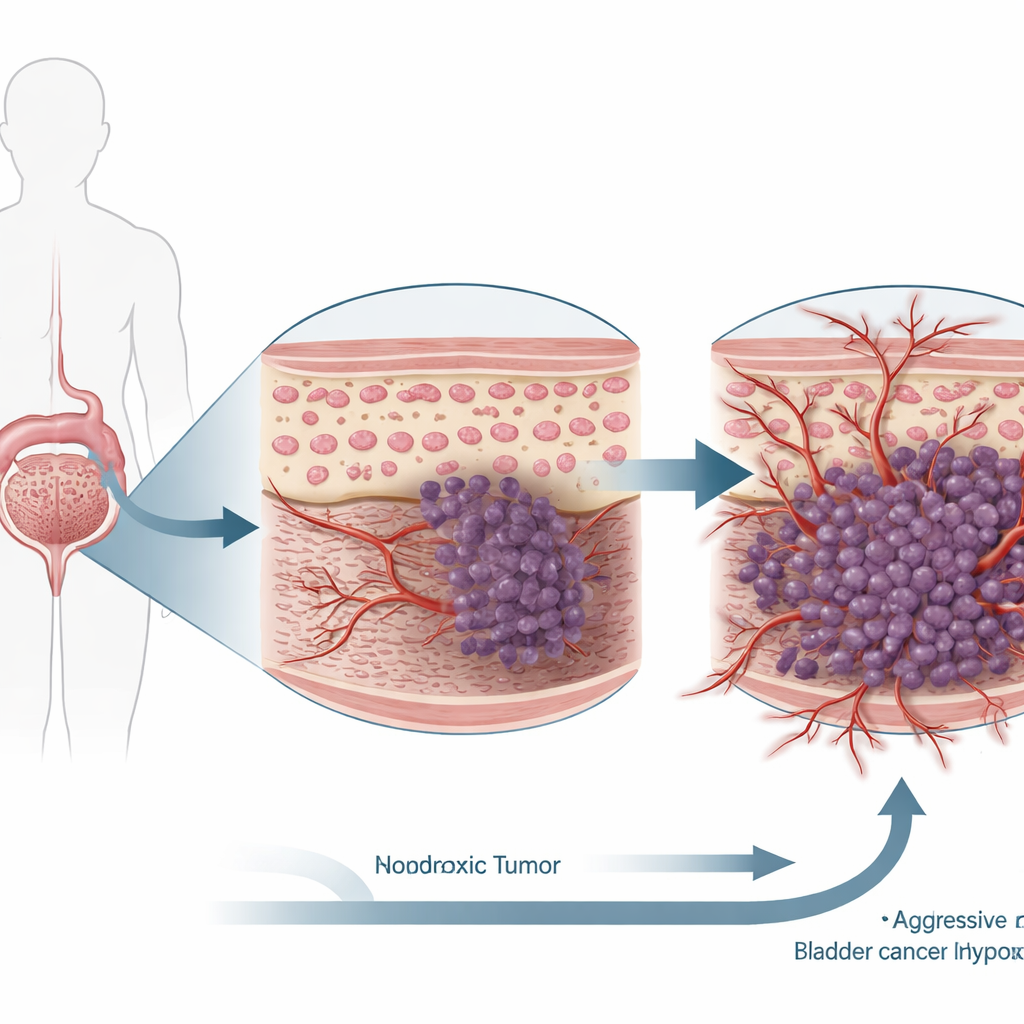
膀胱がん細胞を詳しく見る
研究者らは2つの確立されたヒト膀胱がん細胞株を用い、通常の酸素濃度または低酸素状態に暴露して、実際の腫瘍内にある酸素の少ない環境を模倣しました。次に遺伝学的手法でこれらの細胞のHIF-1αを低下させ、この変化が細胞分裂速度、細胞死の起こりやすさ、移動能、障壁を越えて侵入する能力、そして新生血管を誘導する力といった基本的ながんの挙動にどのように影響するかを測定しました。並行して、患者の膀胱腫瘍試料を検査し、がん組織と周囲の正常膀胱組織でのHIF-1αおよびTIMP3の量を比較しました。
低酸素下での予想外の役割の反転
患者試料はHIF-1αが正常組織よりも膀胱腫瘍で高いことを確認し、腫瘍促進因子としての既存の評価と一致しました。しかし、低酸素条件下の細胞実験ではHIF-1αを減少させると、多くが予想するのとは逆の効果が現れました。HIF-1αがノックダウンされ酸素が不足していると、がん細胞は時間経過でより速く増殖し、プログラム化された細胞死が起こりにくくなり、移動や障壁を越えた侵襲能が高まりました。さらに血管内皮細胞を刺激して、より密で広がりのある管状ネットワークを形成させ、腫瘍への血液供給の増加を示す兆候を示しました。要するに、低酸素環境でHIF-1αが減ると、膀胱がん細胞はより悪性の振る舞いを示したのです。
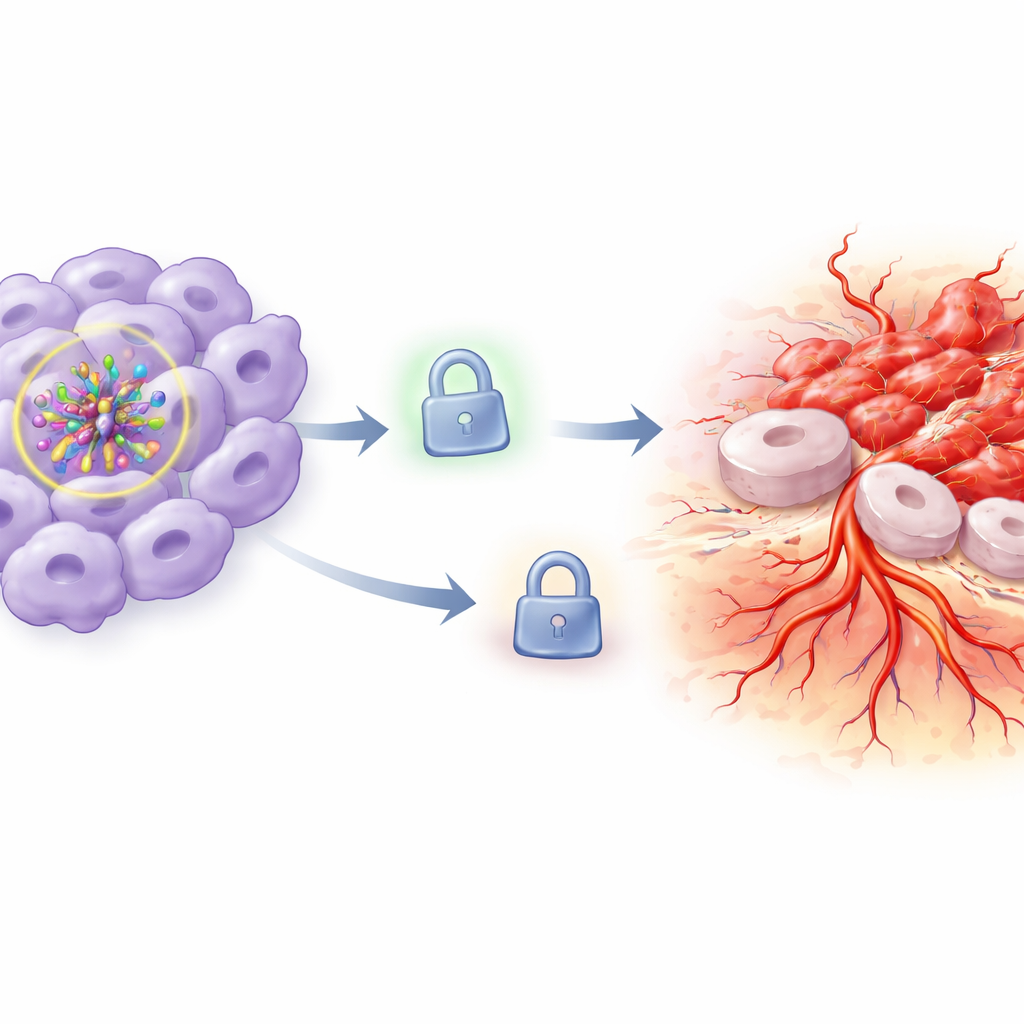
腫瘍拡大に対するブレーキの消失
なぜこのようなことが起きたかを解明するため、研究チームはTIMP3に注目しました。TIMP3は周囲の基質を分解する酵素を阻害して組織破壊や新生血管の成長を抑える、通常はブレーキとして働くタンパク質です。通常酸素下でHIF-1αが低下した細胞ではTIMP3の量は比較的高いままでしたが、酸素が低下するとTIMP3タンパク質は急激に減少しました。TIMP3の喪失は観察された侵襲と血管形成の増加とよく整合します。すなわちブレーキが弱まると、がん細胞は周囲をより容易に再構築して拡大できるようになります。研究者らは次に、低酸素下でHIF-1αがノックダウンされた状態でTIMP3を過剰発現させる実験を行いました。TIMP3を回復させると、攻撃的な振る舞いは部分的またはほぼ完全に逆転しました。細胞の増殖は抑えられ、死は増え、移動・浸潤は減り、誘導される管状構造も数や長さが減少しました。
将来の治療への意味
これらの発見は、HIF-1αが膀胱がんにおいて二面性を持つことを示唆します。一方では、腫瘍中で全体量が高く既知のがん促進プログラムを推進します。もう一方では、強い酸素欠乏下でTIMP3の保護的存在を維持するのに役立っているらしいことが示されました。その文脈でHIF-1αを除去すると、意図せずTIMP3が低下し、より浸潤的で血管促進的な挙動を解き放つ可能性があります。治療においては、単にHIF-1αを阻害するだけでは逆効果になりかねず、医師は同時にTIMP3や同様の抑制機構を維持する方法を見つける必要があることを意味します。本研究は、単一の標的だけでなく、腫瘍がその厳しい低酸素環境に反応する方法を形づくるチェック&バランスの広いネットワークを理解する重要性を強調します。
引用: Wang, X., Guo, J., Zhang, R. et al. Hypoxia-inducible factor 1α exerts dual roles in bladder cancer progression through TIMP3-mediated regulation of angiogenesis and invasion. Sci Rep 16, 8425 (2026). https://doi.org/10.1038/s41598-026-39635-9
キーワード: 膀胱がん, 腫瘍低酸素, HIF-1α, TIMP3, 血管新生