Clear Sky Science · ja
スーダン由来Escherichia coliにおける正統的および新規の耐性関連ミスセンス変異の構造モデリングとドッキング解析
日常の健康にとってこれが重要な理由
抗生物質耐性感染症はもはや珍しい医療上の好奇心ではなく、尿路感染症、手術、集中治療など日常的な治療を脅かす問題になっています。本研究はスーダンのEscherichia coliを詳細に調べ、細菌タンパク質に生じる微小な遺伝的変化が一般的な抗生物質の働きをどのように変えるかという具体的な問いに迫ります。高価な実験ではなくコンピューターによる構造モデリングを用いることで、標準的な検査や世界的なデータベースが見落としがちな隠れた耐性パターンを明らかにしています。特に耐性が急増している資源の限られた地域で重要な知見です。 
細菌の道具箱を覗く
研究者らは「ミスセンス」変異——1塩基の変化でタンパク質の構成アミノ酸が別のものに置き換わる変化——に着目しました。スーダンで採取された55株のE. coliの全ゲノム配列を解析し、フルオロキノロン、マクロライド、リファンピシンなど主要な抗生物質クラスの直接標的となる細菌タンパク質に焦点を絞りました。これらの標的にはDNAをねじる酵素(ジャイレースとトポイソメラーゼIV)、タンパク質合成を担うリボソーム、RNAポリメラーゼなどが含まれます。これらのタンパク質で見つかった71の変異のうち、19は複数の予測ツールでタンパク質機能を損なう可能性が高いと判定され、しかも注目すべきことに、その多くは世界的な耐性データベースにまだ登録されていない新規変異でした。
馴染みの標的における新たな問題点
最も重要な変化はいくつかがリボソームタンパク質L22に集中していました。L22は新たに合成されたタンパク質がリボソームから出るトンネル形成に関与しており、この領域はエリスロマイシンのようなマクロライド抗生物質の結合部位にもなっています。本研究は、これまで報告のなかったL22の変異が多数、しかも単一株内に集中して存在することを明らかにし、それらの多くがこのトンネルやリボソームRNAとの接触点に位置していました。計算解析は、これらの変化のいくつかが局所構造を不安定化させたり柔軟性を高めたりしてトンネルの形状を変え、マクロライド分子が以前ほどぴったり合わなくなる可能性を示唆しました。同時に、DNA処理タンパク質ParCやParE、RNAポリメラーゼには古典的な耐性変異も確認され、スーダン株が世界的な耐性の特徴を共有しつつも地域固有の変化を抱えていることが示されました。
形状変化が抗生物質の結合を弱める仕組み
研究チームは配列リストを超えて、これらの変異が抗生物質と標的の三次元的な適合をどのように変えるかを検証しました。分子ドッキングシミュレーションを用い、異なる薬剤が正常型と変異型タンパク質にどのように結合するかを比較しました。トポイソメラーゼIVタンパク質ParCでは、薬剤接触部位近傍の主要な変異がフルオロキノロンのトロバフロキサシンの結合を予測上大幅に弱め、酵素–DNA–薬剤接合部での把握が緩くなることを示しました。関連するParEでは、変異によりノボビオシンの結合がやや低下しました。対照的にジャイレースのGyrAに見つかった新規変異は酵素構造を不安定化させるように見えたものの、フルオロキノロンのモキシフロキサシンの結合親和性を明確に変化させるわけではなく、耐性は必ずしも薬剤を単純に弾くことで生じるわけではなく、酵素の性能を微妙に乱すことで現れる場合があることを示唆しました。 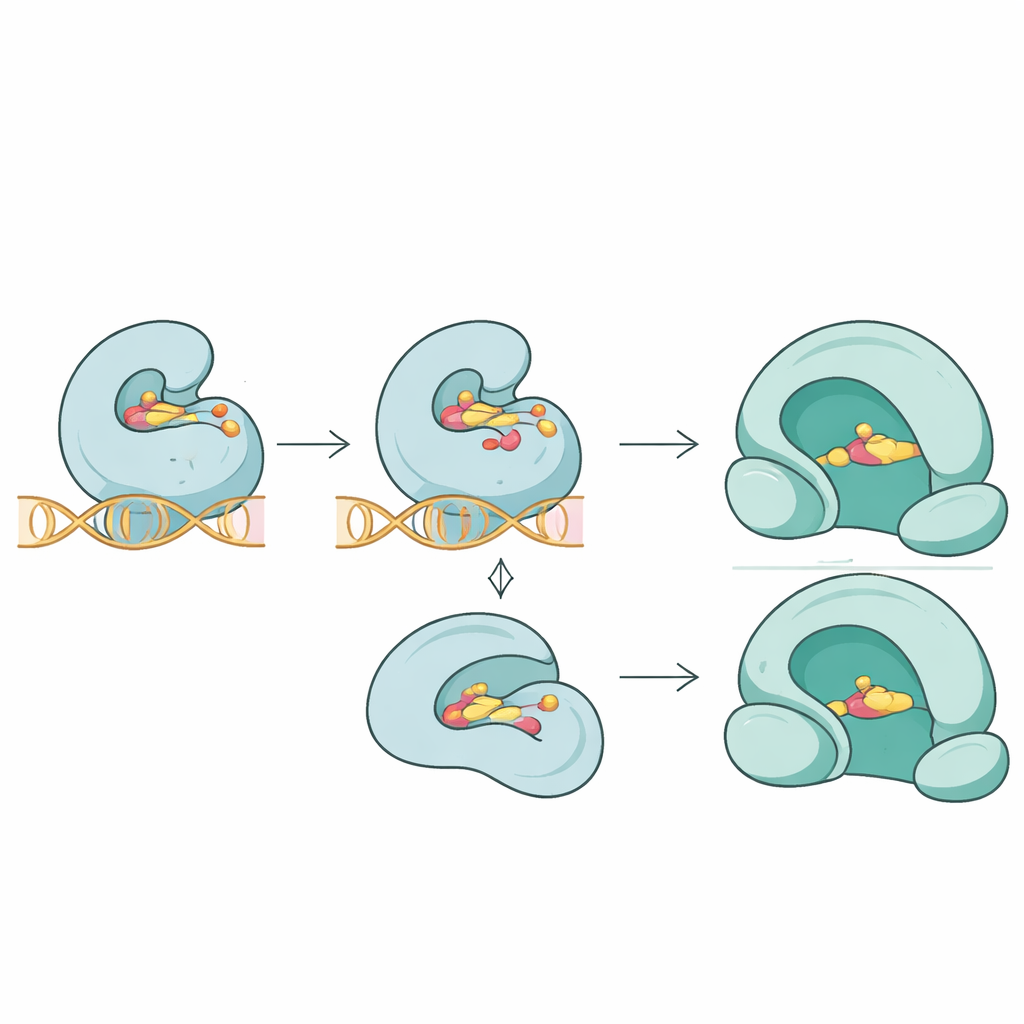
薬剤ごとに異なる混合効果
すべての変異が同じ影響を与えるわけではありませんでした。RNAポリメラーゼRpoBに見られる古典的なリファンピシン耐性変化は、近傍の別の部位を標的とする構造が異なる新しい阻害剤の結合を大きく妨げない場合があり、将来の薬剤設計で既存の耐性パターンを回避できる可能性を示唆します。L22に関するエリスロマイシンのドッキング研究は結果がまちまちで、ある変異は結合を弱め、あるものはほとんど影響せず、1つは結合をわずかに改善する予測さえ示しました。これらの結果は、耐性が単純な白黒の問題ではなく、各変異がタンパク質安定性、柔軟性、薬剤結合をそれぞれ異なる方向に押し、実際の治療への影響は生きた細菌内でそれらがどのように組み合わさるかに依存することを強調します。
患者と監視体制にとっての意味
非専門家向けにまとめると、スーダンのような地域にいる細菌は、よく知られた経路とあまり知られていない経路の両方で耐性を進化させている、というのが主要なメッセージです。既知の経路は国際的なプログラムで追跡されている古典的変異を含みますが、本研究は地域に偏在する多くの追加変異がより微妙な形で抗生物質の効力を弱め得ることを示しています。これらの変化を詳細なタンパク質構造にマッピングすることで、著者らは実験で検証すべき変異の短いリストを提示し、地域の診断パネルに考慮すべき候補を提供しています。実務的には、賢い計算モデリングが限られた実験能力しか持たない国々でも新興耐性をよりよく監視し、最終的にはより確実な治療選択を支援し、細菌の進化より一歩先を行く薬剤設計に寄与し得ると彼らは主張しています。
引用: Sage, E.E., Ibrahim, S.A.E., Firdaus-Raih, M. et al. Structural modeling and docking analysis of canonical and novel resistance-associated missense mutations in Sudanese Escherichia coli. Sci Rep 16, 8995 (2026). https://doi.org/10.1038/s41598-026-39491-7
キーワード: 抗菌薬耐性, Escherichia coli, ミスセンス変異, 構造的バイオインフォマティクス, スーダン