Clear Sky Science · ja
深層学習と物理ベースのモデリングを統合して高精度の抗体-抗原インターフェース予測を実現
将来の医薬にとってなぜ重要か
抗体は免疫系や多くの現代医薬品における誘導ミサイルのような存在です。より優れた抗体を設計するためには、抗体が標的分子(抗原)をどのように把持するかを正確に知る必要があります。これらの構造を実験的に決定するには時間と費用がかかります。本研究は、深層学習と古典的な物理モデルを組み合わせることで、抗体と抗原が接触する箇所の計算予測精度を大幅に向上させられることを示し、抗体設計やスクリーニングの促進につながる可能性を示しています。
「握手ゾーン」を見つける
抗体は先端の小さな柔軟なループ(結合領域)を使って標的を認識し、これらが集まって接触パッチを形成します。これらのループは曲がったりねじれたりし、抗原側の対応領域も深いポケットを作るのではなく広がって浅い場合が多いです。その柔軟性と微妙さが、二つの形状がどのように合わさるかを決めるドッキング問題を計算機にとって非常に困難にしています。従来のドッキングプログラムは、二つのタンパク質の多くの相対的配置を試し、静電気的引力や水の置換などの物理法則に基づいてスコアを付けますが、生物学的な手がかりがないと誤った組み合わせに落ち着きやすいことがあります。
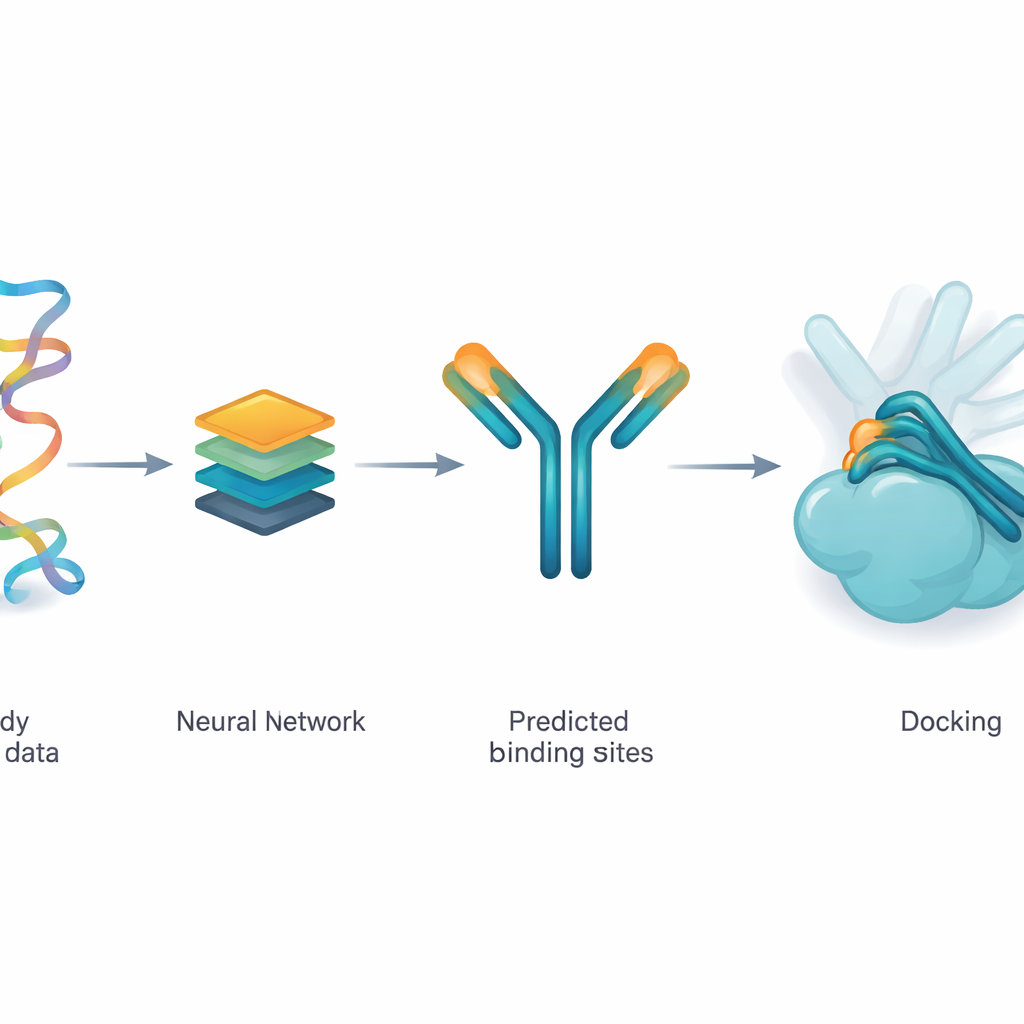
接触しそうなスポットを示唆するネットワークを教える
著者らはParaDeepと呼ばれる深層学習モデルを用いて、抗体のどのアミノ酸が抗原に触れる可能性が高いかを推定します。ParaDeepは抗体の完全な3次元構造を必要とせず、配列(構成要素の順序)のみを入力として用います。重鎖と軽鎖の配列を読み込み、化学的・位置的特徴を符号化し、アテンション機構を用いて結合候補になりやすい残基を強調します。各部位には確率スコアが与えられ、閾値を超えたものが予測接触領域として扱われ、抗体構造上にマッピングされます。
物理エンジンを置き換えるのではなく導く
深層学習で抗体–抗原複合体を一から生成するのではなく、チームはParaDeepの予測した接触残基を既存の物理ベースのドッキングエンジンPyDockWEBに渡します。このドッキングプログラムは、抗体と抗原が出会う可能性のある何千もの配置をサンプリングし、エネルギー関数で評価します。新しいフレームワークでは、予測された接触残基がソフトな拘束条件として働き、サンプリング中の多くの方向がそれらの残基を抗原表面の近くに誘導するようバイアスをかけます。重要なのは、基盤となる物理的スコアリングや剛体扱いは変わらず、処理が透明で比較的軽量に実行できる点です。
予測はどれだけ改善するのか
研究者らは、キュレーションされたデータベースから選んだ50件の既知の抗体–抗原複合体でハイブリッド手法を検証しました。各ケースについて、従来の「ブラインド」ドッキングとParaDeepの拘束で導かれたドッキングを比較しました。局所的なインターフェース精度(予測接触領域が実際にどれだけ一致するか)、全体の形状類似度、およびドッキングモデルを評価する広く用いられる総合品質スコアを測定しました。このセット全体で、ガイド付き手法は結合部位の誤差を大幅に減らし、全体構造を真の複合体に近づけ、多くの予測を明らかに誤ったものから中〜高品質のカテゴリへ移行させました。ガイド付きモデルのほぼ半数が高品質の範囲に入り、ブラインドドッキングの約4分の1に対して大きな改善が見られました。
何がマッチングを容易にするか
どの複合体がより恩恵を受けたかの理由も解析されました。単により多くの接触残基を予測することが成功を保証するわけではなく、重要なのは拘束を置く適切な領域であって数ではないことが分かりました。より親水的で柔軟なコイル領域を多く含むインターフェースは、PyDockWEBが重視する静電気的要素と相性が良く、大きな形状変化を伴わずに整列しやすいため、より良くドッキングする傾向がありました。研究者らが実験構造から直接抽出した「オラクル」的な接触情報を用いて失敗例のいくつかを再試行したところ、多くが改善し、接触パッチの正確な局在化が重要な要素であることが裏付けられました—ただし、大きな形状調整が必要な場合は剛体ドッキングに限界が残ります。
今後の意味
日常的な表現を使えば、本研究は物理ベースのドッキングプログラムに「抗体がどこを掴みやすいか」についての賢いヒントを与えることで、その狙いを大幅に改善できることを示していますが、処理を不透明なブラックボックスに変えるわけではありません。ParaDeep–PyDockWEBの統合パイプラインは、より高度な柔軟性を持つ手法や生成的手法に取って代わるものではありませんが、配列レベルの深層学習信号を用いて、なじみのある解釈可能なドッキングツールを実用的に導く方法を提供します。抗体探索やエンジニアリングで配列ライブラリがますます大規模になる中で、このようなハイブリッドアプローチは、望ましい標的と構造的に整合する候補を速やかにふるいにかけ、配列から実用的な抗体へ至る道をより迅速かつ情報に富んだものにする可能性があります。
引用: Kodchakorn, K., Udomwong, P., Pamonsupornwichit, T. et al. Integrating deep learning with physics based modeling enables high precision antibody antigen interface prediction. Sci Rep 16, 8134 (2026). https://doi.org/10.1038/s41598-026-39466-8
キーワード: 抗体ドッキング, 深層学習, パラトープ予測, タンパク質間相互作用, 抗体設計