Clear Sky Science · ja
抗原特異的T細胞活性化のためにCD32aシグナル食作用を利用したTHP-1-CAR単球の最適化
免疫系に新しい機能を教え込む
現代の細胞療法はすでに免疫細胞をがんに対して再プログラムしているが、ほとんどはT細胞に依存しており、固形腫瘍という過酷な環境では十分に機能しないことがある。本研究は代わりにもう一つの強力な防御者――“食べる”ことを専門とするマクロファージに注目し、これらをどのように書き換えれば有害な細胞やウイルスをより効率的に取り込み、かつ持続的で標的特異的な攻撃のためにT細胞を呼び込めるかを問う。研究は、COVID-19のような感染症や治療困難な固形腫瘍の両方に応用可能な、より優れたキメラ抗原受容体(CAR)マクロファージを構築するための設計指針を明らかにした。
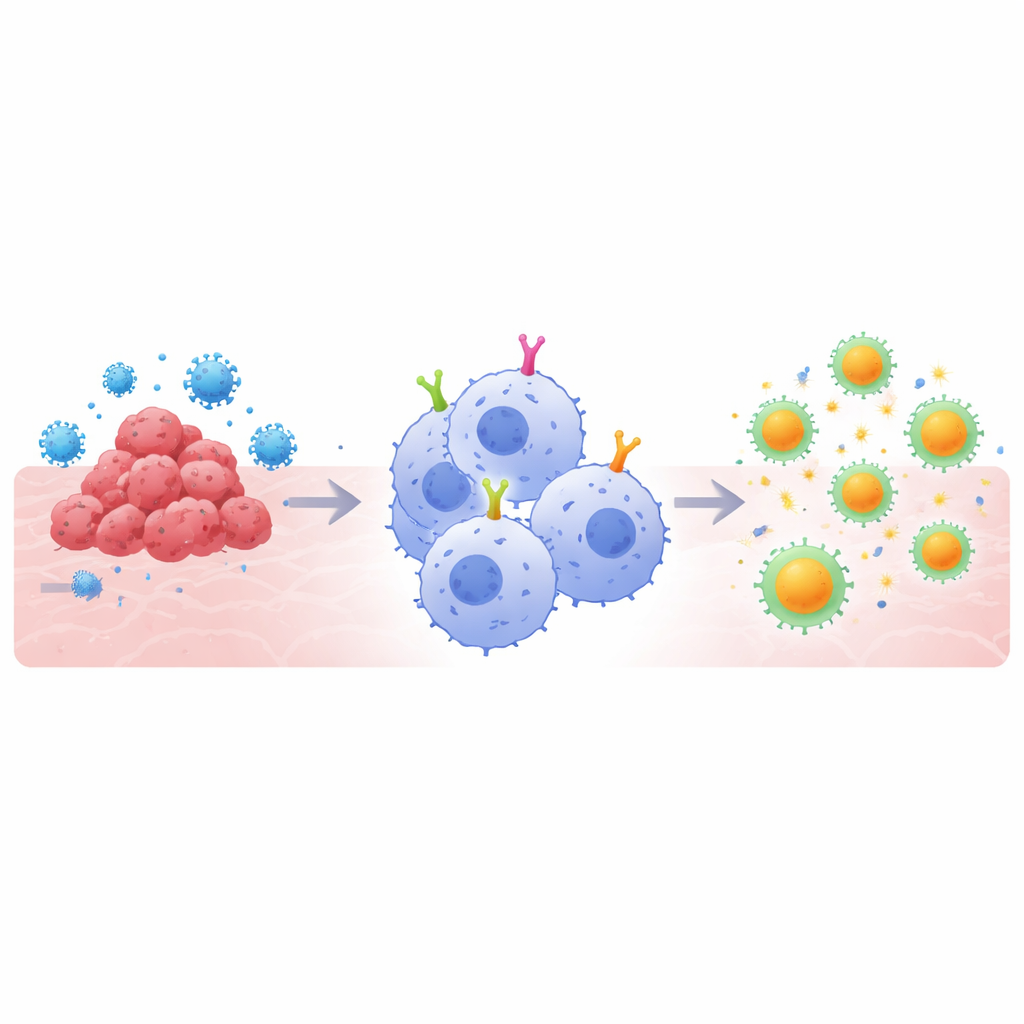
なぜ“スーパー食者”が重要なのか
CARベースの治療は、腫瘍タンパク質やウイルススパイクなど選択した標的を認識するカスタムの表面受容体で免疫細胞を武装させることで機能する。T細胞版は特定の血液がんの治療を一変させたが、固形腫瘍や一部の感染症に対しては障壁がある。マクロファージは別の角度を提供する:本来、脅威を取り込み、断片化してT細胞に提示することで「自然免疫」と「獲得免疫」をつなぐ役割を果たす。しかし、多くのCAR設計はもともとT細胞向けに作られており、マクロファージには最適化されていない。著者らは、マクロファージの強みを最大限に引き出すには、標的が結合した後に細胞に何をさせるかを指示するCARの内部シグナル部分をこれらの“食べる細胞”に合わせて調整する必要があると考えた。
最適な内部配線を探る
研究チームは、ヒト単球系の細胞株(THP‑1)に導入したCARの内部シグナルドメインを体系的に比較した。THP‑1はマクロファージへ分化可能であるため適したモデルである。彼らは通常、食作用や炎症を駆動する受容体に由来するドメインに注目した:CD3ζ(従来のT細胞モジュール)、CD32a(抗体でコーティングされた標的を結合する受容体)、補体受容体の主要成分であるCR3のCD11bとCD18、そして微生物危険を感知するTLR4である。SARS‑CoV‑2スパイクタンパクで被覆したビーズや擬似ウイルスを用い、各CARデザインが標的の取り込み、炎症性分子の産生、そしてウイルスに既に曝露したヒトの記憶CD8 T細胞をその後どの程度活性化するかを測定した。最も有望なデザインをメソセリンと標的化するCARに移し、同じ原則が腫瘍の文脈でも成り立つかどうかを検証した。
より優れた食べ手と信号増幅装置の構築
明確な傾向が現れた:CD32aに基づくCARは、通常のCD3ζドメインを用いたものより一貫して強く早い食作用を促進した。これはCD3ζが従来の活性化モチーフを多く持っているにもかかわらず起きた。言い換えれば、信号とマクロファージの機構との“適合性”が、単なる信号強度よりも重要だった。CD32aの上にCR3由来の断片(CD11bまたはCD18)を追加しても多くの条件で取り込み能がさらに増すことはなかったが、TNF‑αやIL‑1βといった主要な炎症性サイトカインのレベルは上昇した。TLR4を含む組み合わせは炎症シグナルやT細胞刺激能に関連する表面マーカーCD86をさらに増強したが、その代償として細胞表面のCAR量が減少し、やや取り込みが低下するというトレードオフも伴った。
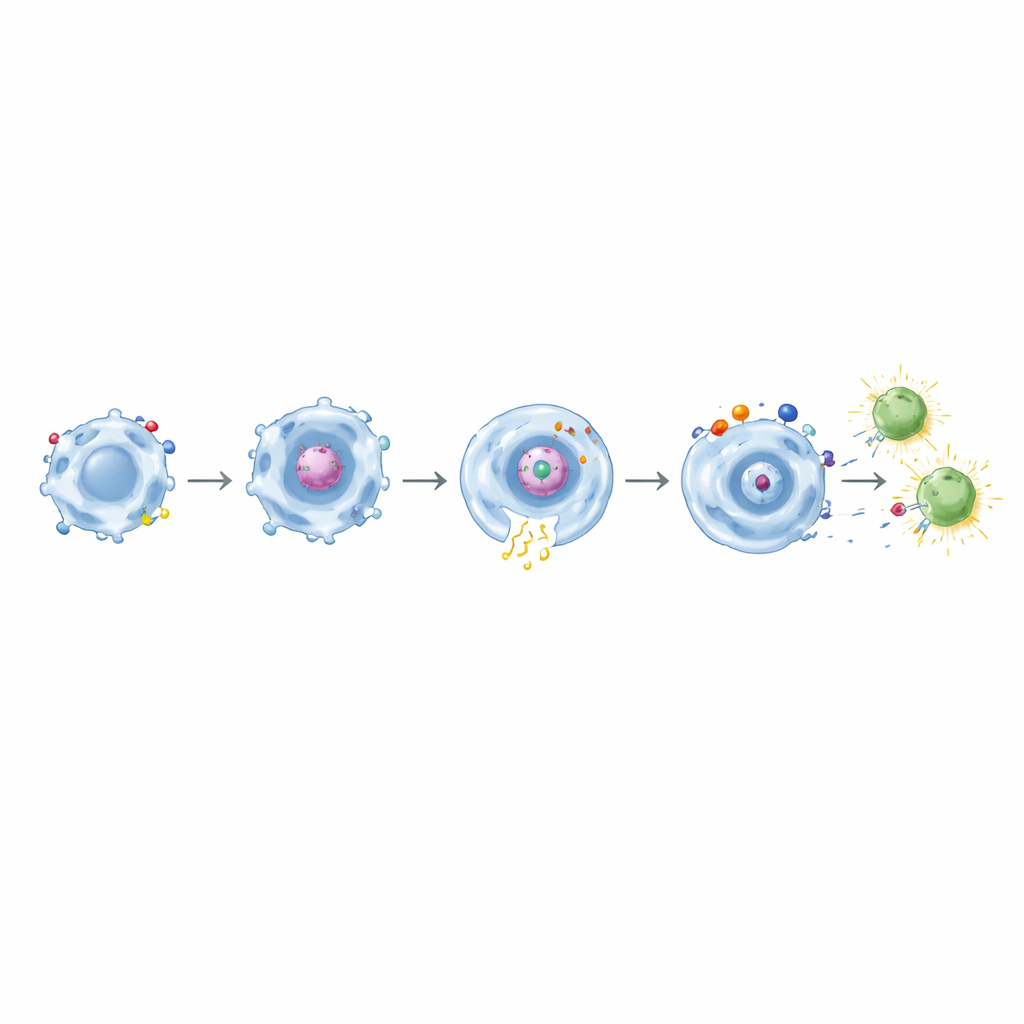
食べることからT細胞を教育するまで
重要なことに、CD32aベースのCARを持つマクロファージがスパイクタンパクを取り込んだ後、以前にCOVID‑19ワクチン接種を受けた人々の記憶CD8 T細胞を活性化できた。これらのT細胞は早期活性化マーカーを発現し、インターフェロン‑γやTNF‑αなどのエフェクター分子を産生した。CD32aをCD11b、CD18、またはTLR4と組み合わせた二重ドメインCARではその効果がさらに強化された。メソセリンを標的とする類似設計を改変腫瘍細胞に対して試したところ、標的依存的な精密な食作用と高まった炎症シグナルの組み合わせが再び示された。これらの中では、CD32a+TLR4の組み合わせが「組織の警報」として最も効果的で、サイトカイン分泌とCD86を強力に増強しつつ、特異的な腫瘍取り込みも維持していた。
将来の治療にとっての意味
素人目には、本研究はマクロファージのエンジニアリングが一律の問題ではないことを示している。内部シグナルモジュールを入れ替え、組み合わせることで、病変細胞の効率的な清掃に特化した細胞や、腫瘍の免疫抑制的環境を再形成してT細胞を動員する免疫増幅器のように振る舞う細胞を設計できる。CD32aベースのCARはそのような設計の堅実な基盤として浮上し、マクロファージにおいて従来のT細胞モジュールを上回り、ウイルスおよび腫瘍の標的で一貫して機能した。これらの結果は培養系モデルに基づくものであり、一次ヒト細胞や動物での検証が必要だが、迅速な取り込みと精密なT細胞活性化を結びつけることで固形腫瘍や持続感染によりよく対処しうる次世代CARマクロファージ療法の設計図を提供している。
引用: Hong, J., Lee, S., Kim, Y. et al. Optimization of THP-1-CAR monocytes utilizing CD32a signaling phagocytosis for antigen-specific T cell activation. Sci Rep 16, 8175 (2026). https://doi.org/10.1038/s41598-026-39406-6
キーワード: CARマクロファージ, CD32aシグナル, 食作用, 固形腫瘍免疫療法, T細胞活性化