Clear Sky Science · ja
放射線生物学的シミュレーションのための細胞核間相の高分子物理モデル
なぜDNAの「住まい」の形が重要なのか
放射線は医療において両刃の剣です:がん細胞を死滅させ得る一方で、健康な組織を損なうこともあります。そのリスクと利点の核心にあるのが、細胞核内にぎっしりと詰め込まれたDNAです。本論文は、核内のこの「DNA都市」を物理に基づく詳細な3次元モデルで表現することで、放射線が染色体をどのように切断し誤修復させるかを予測し、がん治療や宇宙放射線リスク評価の改善に寄与できる可能性を示します。
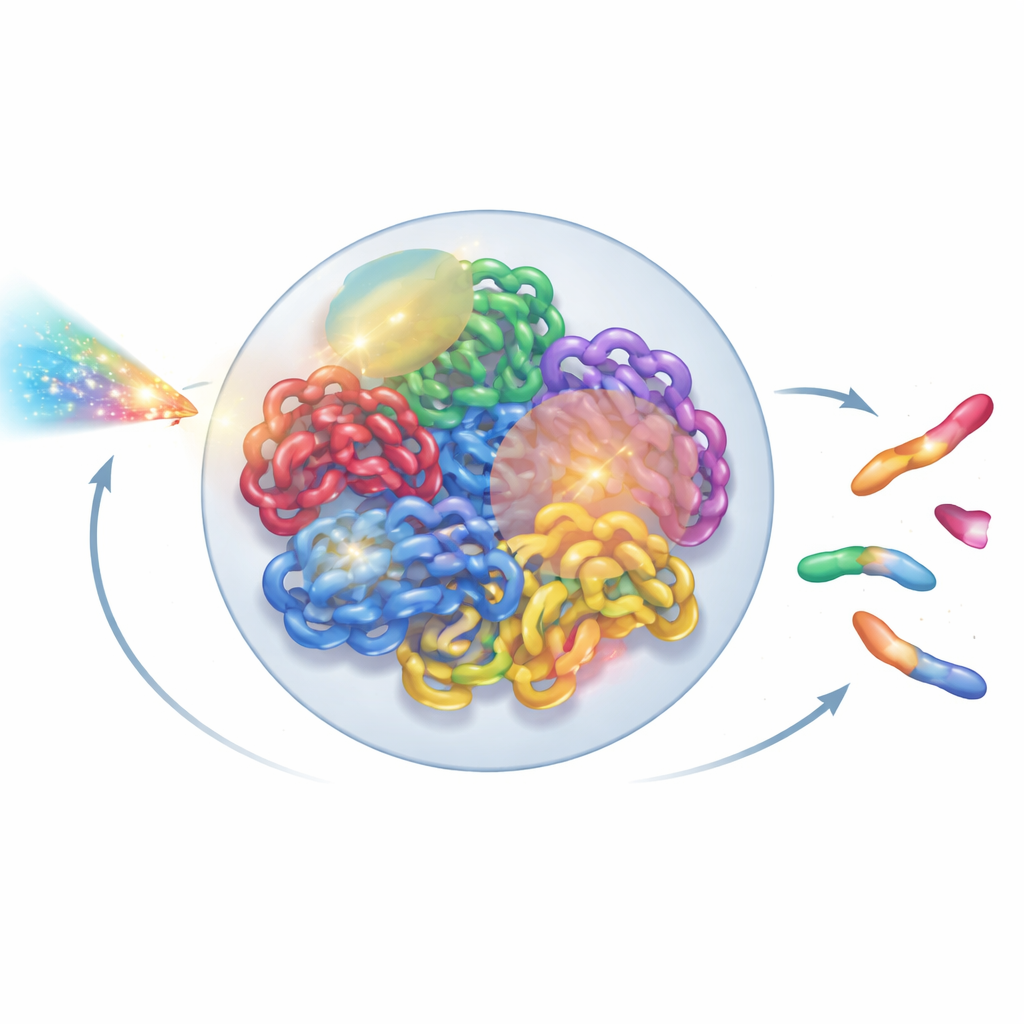
ゲノムを生きた構造としてとらえる
ヒトの各細胞の中には2メートルにも及ぶDNAが、数マイクロメートルしかない小さな核に折りたたまれて収まっています。この折りたたみはランダムではなく、各染色体は独自の領域を占め、さらに近隣群やループ状のドメインに区分されます。超解像顕微鏡やHi-C接触マップといった新しい実験手法は、この精緻な3次元配列を驚くべき詳細で明らかにしました。それでも多くの放射線モデルはDNAを単純化された線の絡み合いか理想化されたループとして扱い、この高次の組織化を見落としています。著者らは、生物学が明らかにした実際のクロマチン構造を尊重しつつ、一般的な研究室の計算機で実行できるだけの高速さを保った全核モデルの構築を目指しました。
高分子物理で仮想的な核を構築する
チームは染色体を可撓性の鎖としてモデル化し、プラスチックや軟材料を理解するために用いられる高分子物理の考え方を取り入れました。膨大な計算コストを抑えるために、問題を3つの緩和段階に分けました。まず、クロマチンドメインと呼ばれる大きな構成要素を核内に配置し、相互反発、軸方向の伸長、より広いサブコンパートメントへの集積を許容しました。次に各ドメイン内を拡大してより細かいクロマチン繊維を配置し、結合タンパク質で保持されるループ領域も再現しました。最後にすべての繊維を核境界内で再び自由に相互作用させ、現実的な最終構成に近づけました。こうした分割処理と階層的探索や並列計算の工夫により、従来実用的でなかった4か月という実行時間を、64コアのワークステーションで核あたり約3時間に短縮しました。
放射線トラックからDNA切断と修復へ
仮想核が構築されると、著者らはGeant4-DNAシミュレーションで生成した詳しい放射線トラックを重ね合わせました。各イオン化イベントについて、どのクロマチンドメイン、繊維セグメント、そして最終的にどのヌクレオチドが最も近いかを探すために階層的探索を用い、100億にも及ぶヌクレオチド位置をメモリに保持することを避けました。代わりに再利用可能なクロマチンのテンプレートを保持し、座標変換をオンザフライで適用しました。DNAバックボーン中のイオン化は一本鎖切断として扱われ、近接した反対鎖上の切断は二本鎖切断になりました。細胞の修復機構を模すために、著者らは距離に基づく再結合ルールを導入しました:近くにある自由なDNA末端ほど再結合しやすいとします。再結合の判断は逐次的に行われ、すべての末端が対を成すか未修復のまま残るまで続けられ、正しい修復と誤再結合の両方を再現しました。
ネットワーク論理で壊れた染色体を分類する
この仮想修復の後、核内には再構成された染色体と残された断片が混在していました。何が起きたかを分類するために、著者らは修復済みゲノムを無向グラフに変換しました:染色体区画を辺に、両端や切断点をノードに置き換えます。標準的な連結成分アルゴリズムを用いることで、新しくできた各染色体様オブジェクトを自動的に取り出し、セントロメア(細胞分裂での付着点)やテロメア(自然の末端)の数といった主要な特徴を数えられました。これにより二本のセントロメアを持つ二重中心体や環状染色体、欠失などを同定しました。そして、ヒト皮膚細胞をガンマ線やアルファ粒子に曝した古典的な実験とシミュレーションを比較し、総染色体異常数が測定値の約20%以内で再現されることを示し、従来モデルよりも大幅に改善していることを示しました。
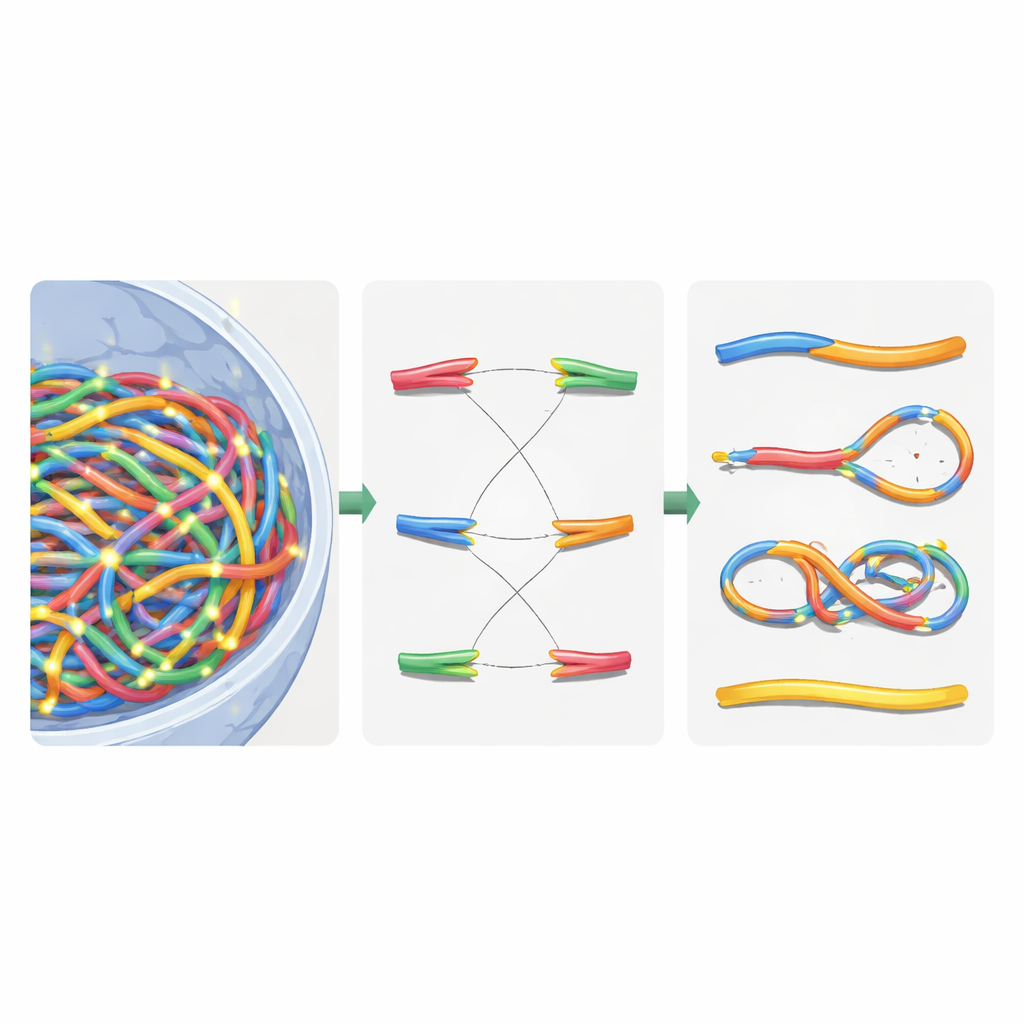
患者と宇宙飛行士にとっての意味
簡潔に言えば、本研究はDNAが核内の「どこ」にあり「どう」折りたたまれているかが、放射線損傷がどのように蓄積して危険な染色体変化につながるかに強く影響することを示しています。現実的な3次元ゲノムアーキテクチャ、効率的な物理ベースのシミュレーション、そして壊れた染色体のグラフベースの解析を組み合わせることで、構造生物学と放射線生物学の間に強力な橋を提供します。著者らは、詳細な修復時間の導入や全ゲノム配列データの活用といった将来の改良により、このアプローチががん治療で用いられる高エネルギー粒子や深宇宙で遭遇する放射線の生物学的影響をさらに正確に予測できるようになると論じています。最終的には、細胞内のDNAの「住まい」をより良くモデル化することが、安全で効果的な放射線治療の実現や長期的な放射線リスクの理解を深める助けになるかもしれません。
引用: Zhao, M., Huang, G., Xu, Z. et al. A polymer physics model of the interphase cell nucleus for radiobiological simulations. Sci Rep 16, 7913 (2026). https://doi.org/10.1038/s41598-026-39234-8
キーワード: 放射線によるDNA損傷, クロマチンの3次元構造, 染色体異常, 高分子物理モデリング, 粒子線治療