Clear Sky Science · ja
AIBP欠損マウスにおける動脈硬化の増加とマクロファージ泡沫細胞におけるインフラマラフトの発現。
動脈の詰まりは単なる脂肪の蓄積以上のもの
動脈硬化――血管がゆっくりと詰まり硬くなる過程――は心臓発作や脳卒中の主要な原因です。血管内に脂肪が溜まるだけと単純に捉えがちですが、実際はより複雑です。血管壁内の免疫細胞は炎症を鎮める役割を果たすこともあれば、炎症を助長することもあります。本研究は、ある状況下でこれらの細胞が脂肪を貯める“掃除屋”から、プラークをより危険な段階へと進める発火装置のような存在に変わる理由を探ります。
脂肪を貯め込む免疫細胞
形成中の動脈プラーク内では、マクロファージと呼ばれる白血球の一種が大量のコレステロールを取り込み、いわゆる泡沫(ほうまつ)細胞になります――油滴で膨らんだ不健康な細胞です。これまでのマウス研究では、こうした泡沫細胞は一見不健康に見えるにもかかわらず、意外に炎症性は低く、むしろ周囲のやせたマクロファージの方が炎症性シグナルを多く発していることが示唆されていました。本研究は、細胞表面からコレステロールを除去し特定の膜上“ホットスポット”を抑える働きをするAIBPというタンパク質が欠けると何が起きるかを問いかけます。
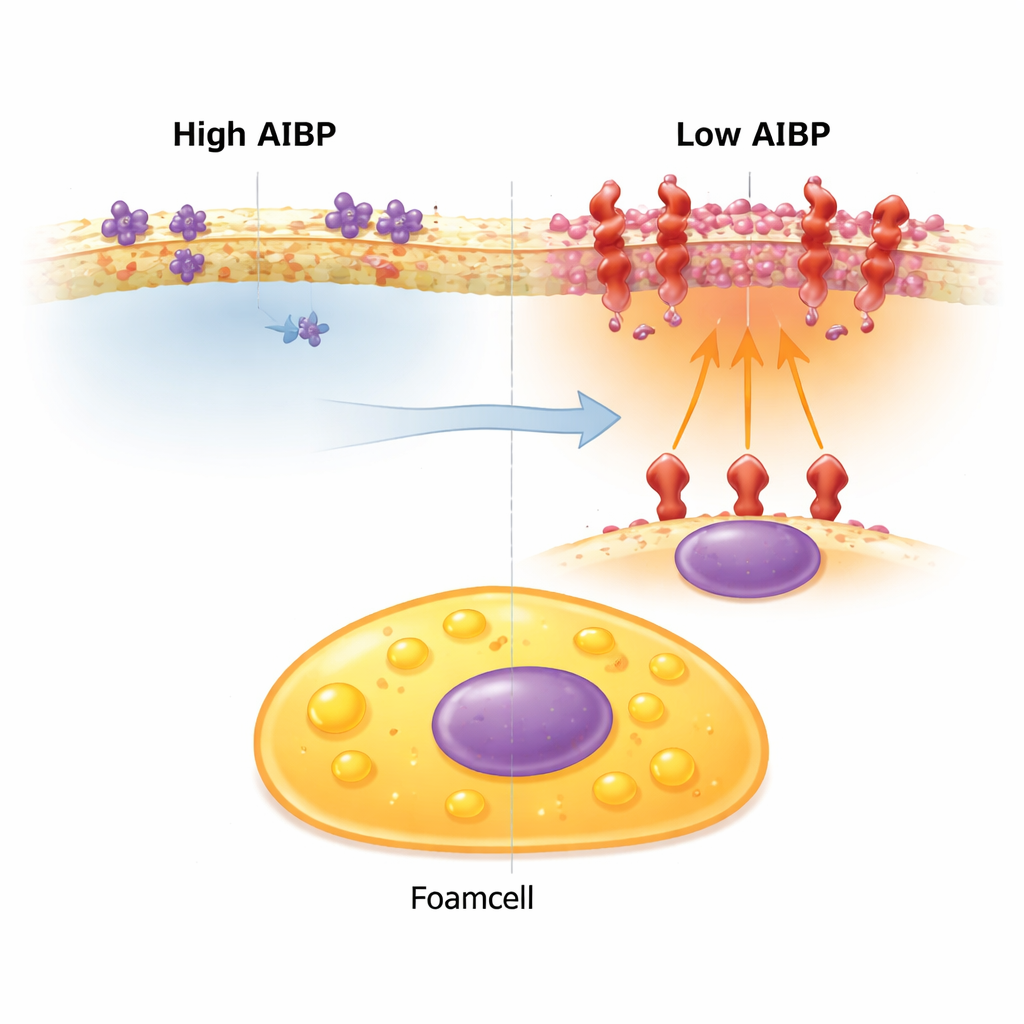
アラーム信号を増幅する膜のホットスポット
細胞表面は均一ではありません。コレステロールや特定の脂質は小さなプラットフォームに集まり、危険を感知する受容体がそこに寄り集まります。これらのプラットフォームが拡大し炎症受容体を取り込むと、著者らはそれらを「インフラマラフト(inflammarafts)」と呼びます。その一つであるTLR4は脅威を検出するのに役立ちますが、過剰に活性化されると慢性的な炎症を引き起こし得ます。高コレステロールに傾きやすい通常のマウスでは、非泡沫性マクロファージの方がこうしたインフラマラフトを多く持ち、泡沫細胞は比較的少ない――このことが泡沫細胞が炎症性に乏しいと見なされてきた理由の一つです。
脂肪を抱えた細胞が炎症性を帯びるとき
研究チームは、AIBPと主要なコレステロール除去受容体の両方を欠く(動脈疾患になりやすい)マウスと、受容体だけを欠く対照マウスを比較しました。高脂肪食を16週間与えたところ、AIBP欠損マウスではより多くの泡沫細胞を含むプラークが形成され、それぞれがより多くの中性脂肪を詰め込んでいました。重要なのは、これらの泡沫細胞がTLR4のペアやコレステロールに富む膜パッチ――インフラマラフトの特徴――を高いレベルで示し、プラーク内で従来の穏やかな脂肪貯蔵型細胞ではなく主要な炎症性細胞となっていた点です。培養実験でも、酸化コレステロールで泡沫化させたAIBP欠損マクロファージは、炎症、組織分解、血管のリモデリングに関連する遺伝子をオンにし、酸化ストレスやミトコンドリアのストレスが増加していました。
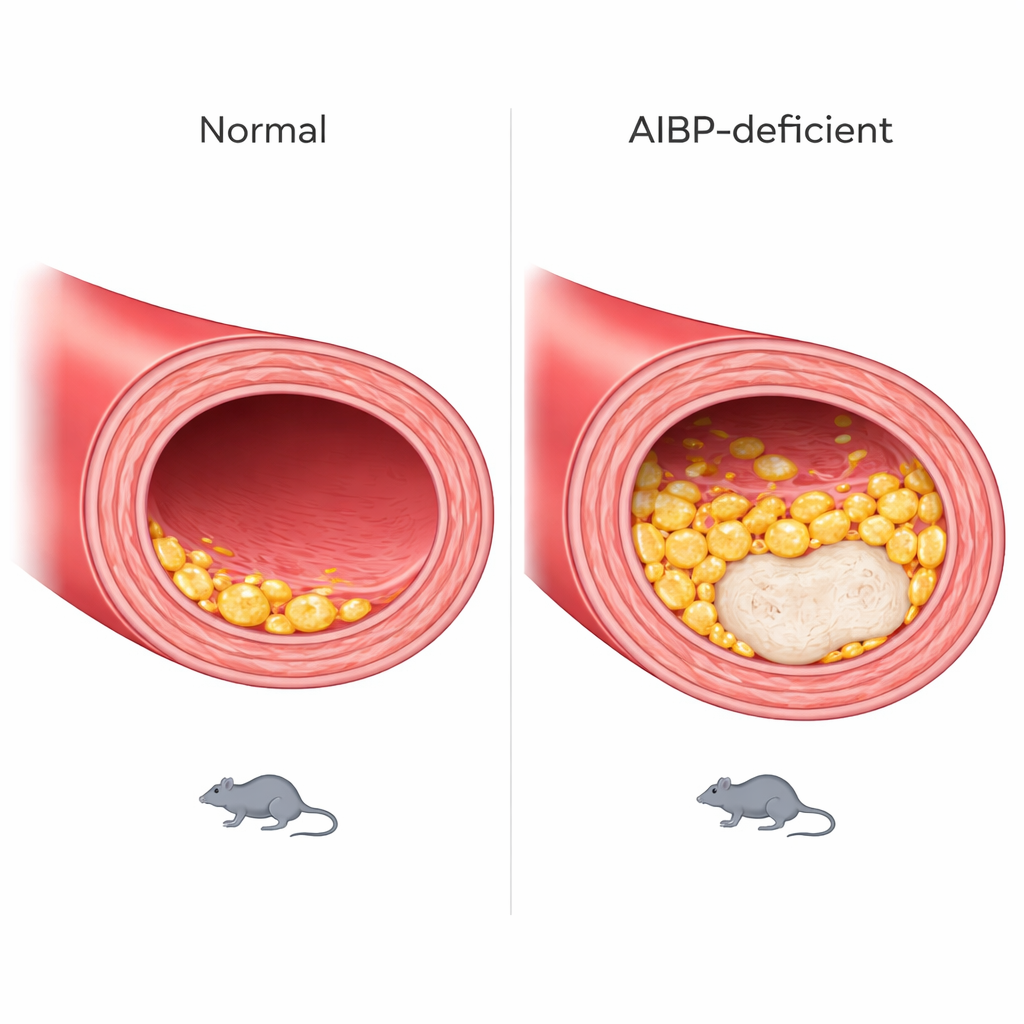
血管壁で成長し不安定になるプラーク
これらの細胞レベルの変化は、動脈の病変悪化という形で反映されました。心臓の大動脈の断面を見ると、AIBP欠損マウスではより大きなプラークが形成され、特に壊死コア――プラーク内の壊死領域で破裂しやすい“脆弱”な病変に関連する部分――が大きくなっていました。雄雌ともに影響が見られましたが、血管のどの部位に最も重篤な損傷が出るかは性差がありました。動物はまた体重がより早く増え、血中中性脂肪値も高くなり、脂質処理全体の乱れを示していました。
将来の治療に向けての示唆
専門外の方に向けた要点は、プラーク内のコレステロールを多く含む細胞が一様ではないということです。AIBPが存在する場合、泡沫細胞は余剰の脂肪を静かに蓄える“倉庫”のように振る舞いがちです。AIBPが欠けると、同じ細胞が表面を再構成してインフラマラフトを作り、大きな炎症性シグナルを発するようになり、プラークを危険な進行段階へと押し進めます。本研究はマウスで行われたものですが、AIBPとこれら膜ホットスポットの制御が、プラークが不安定化して生命を脅かす事態になるのを防ぐための将来の治療ターゲットになり得ることを示しています。
引用: Li, S., Nazarenkov, N., Alekseeva, E. et al. Increased atherosclerosis and expression of inflammarafts in macrophage foam cells in AIBP-deficient mice.. Sci Rep 16, 7645 (2026). https://doi.org/10.1038/s41598-026-39113-2
キーワード: 動脈硬化, マクロファージ泡沫細胞, 炎症, コレステロール代謝, AIBP