Clear Sky Science · ja
重度タイプ2高発現喘息エンドタイプ向けの吸入可能な小分子IL-33/ST2拮抗薬のインシリコ同定
呼吸への影響 — なぜ重要か
重度喘息に苦しむ何百万人もの人々にとって、最新の吸入器や高度な注射療法であっても息切れや危険な発作のリスクを完全に取り除けないことがあります。本研究は、既知の錠剤様薬剤を吸入治療として再設計し、肺内の上流にある「警報」信号の一つを遮断できるかを探るものです。研究者らはコンピュータシミュレーションだけを用いて、重度でアレルギー駆動型の喘息に関与する重要な受容体に結合し得る小分子を探索し、実用的な薬を提供するのではなく将来の実験の基礎を築くことを目指しました。
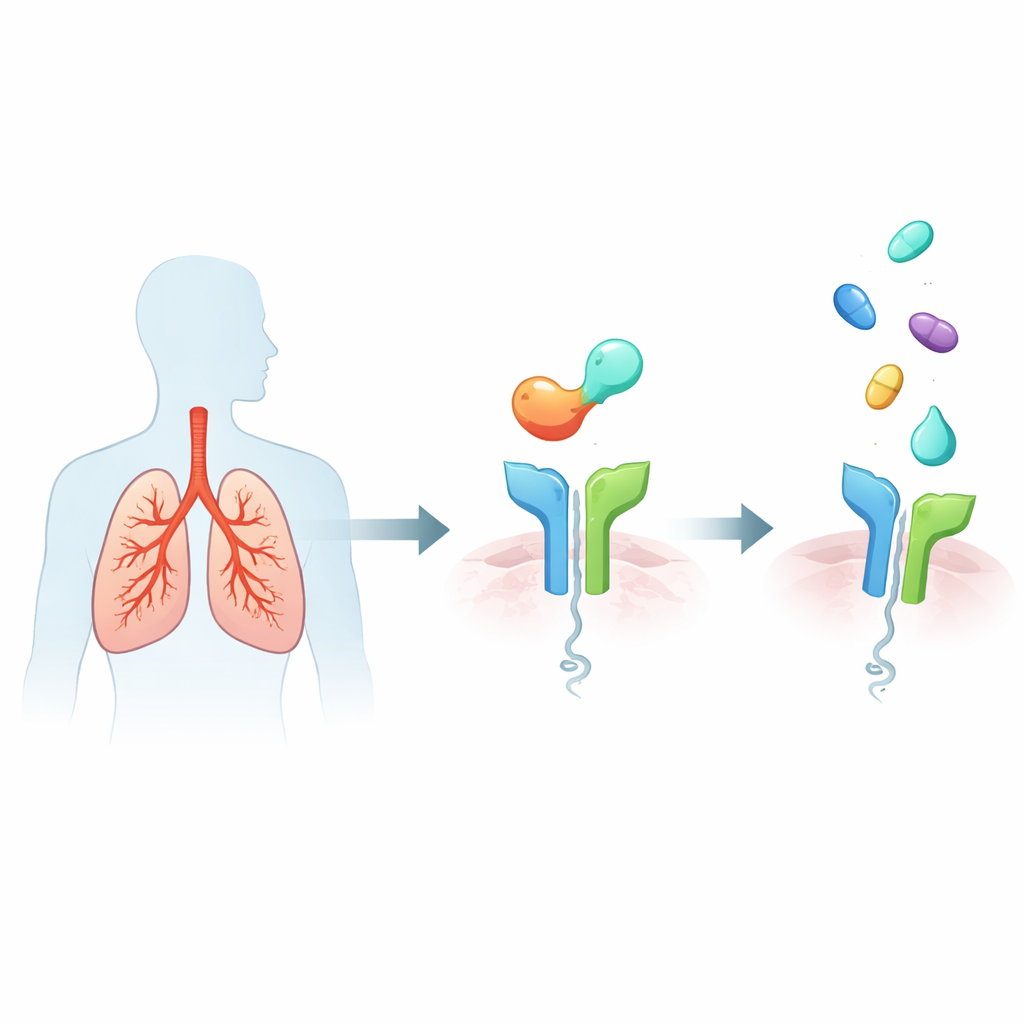
喘息患者の肺内にある警報システム
重度のタイプ2高発現喘息は、粘液や炎症細胞で気道が満たされ、気道が狭窄し、時間とともに肺構造が損なわれる過剰な免疫反応を特徴とします。主要な誘因の一つは、気道上皮細胞がストレスを受けた際に放出するIL-33というタンパク質です。IL-33はさまざまな免疫細胞上のST2という受容体に結合し、強力なメッセンジャー分子の放出を引き起こして、喘鳴、増悪、長期的な気道再構築といった喘息の特徴を推進します。IL-33/ST2活性が高いほど症状が悪化し発作が頻発することが関連しているため、ST2は魅力的な上流ターゲットとして注目されています。ST2を遮断すれば、下流にある多くの炎症シグナルを同時に静められる可能性があるからです。
抗体から日常薬へ
重度喘息の現在の治療のいくつかは、血中の炎症性タンパク質を捕まえたりその受容体をブロックしたりする注射型の抗体を用いています。これらは一部の患者に有効ですが、費用が高く注射が必要であり、主に経路の下流のシグナルに焦点を当てています。これに対して、小分子薬は従来の錠剤や吸入薬に近く、大量生産が可能で保管が容易、そして直接肺に届けられる可能性があります。課題は、ST2がIL-33と広いタンパク質–タンパク質インターフェースを介して結合することで、酵素の深いポケットのような明瞭な結合部位よりも小分子で阻害するのが難しい点です。そこで著者らは、ST2–IL-33複合体の高解像度構造データと最新のインシリコツールを用い、既知の抗炎症薬の中にこのインターフェースの一部に思いがけず結合し得るものがないかを検討しました。
受容体表面をコンピュータで探索
研究チームはヒトST2と結合したIL-33の結晶構造を用い、まずIL-33を除去して受容体の結合表面を露出させ、ポケット検出プログラムで小分子が収まるのに最も有望な領域を特定しました。次に、モンテルカストやザフィルルカストといったロイコトリエン受容体拮抗薬、サリドマイド類縁の免疫調節薬、JAK阻害薬など、喘息や関連免疫疾患で臨床的に用いられている10種の小分子と、比較用の既報のST2標的分子を選びました。仮想ドッキングソフトで各化合物をST2表面に数千回配置し、最も適合する姿勢を予測結合強度でスコアリングしました。その結果、ザフィルルカストが最上位の骨格として浮上し、モンテルカストや既知のST2指向性比較分子をやや上回りました。
スクリン上でのリード化合物の調整
予測結合と一般的な薬物様性のバランスが最も有望だったザフィルルカストを基に、著者らはAI支援の設計ツールを用いてこの分子の修飾版を作成しました。目的はST2への結合を維持しつつ、安全性予測を改善することです。再設計された類縁体は、ドッキングスコアが非常に類似しており、インシリコでは毒性が低いと予測されました。詳細な接触マップは、親化合物と修飾化合物の双方が通常IL-33が接触するいくつかのST2アミノ酸に触れていることを示し、機能的に重要なインターフェース領域を占めていることを示唆しました。水と塩の環境での拡張分子動力学シミュレーション(合計0.5マイクロ秒の仮想運動)では、受容体とリガンドの両方が柔軟性を保ち、小分子は表面に固定されるのではなく様々な位置を探索することが示されました。時間経過での相互作用エネルギーの計算は、有意ではあるが動的な結合を示しており、比較的平坦なタンパク質–タンパク質表面を試行錯誤する分子の挙動と整合しました。
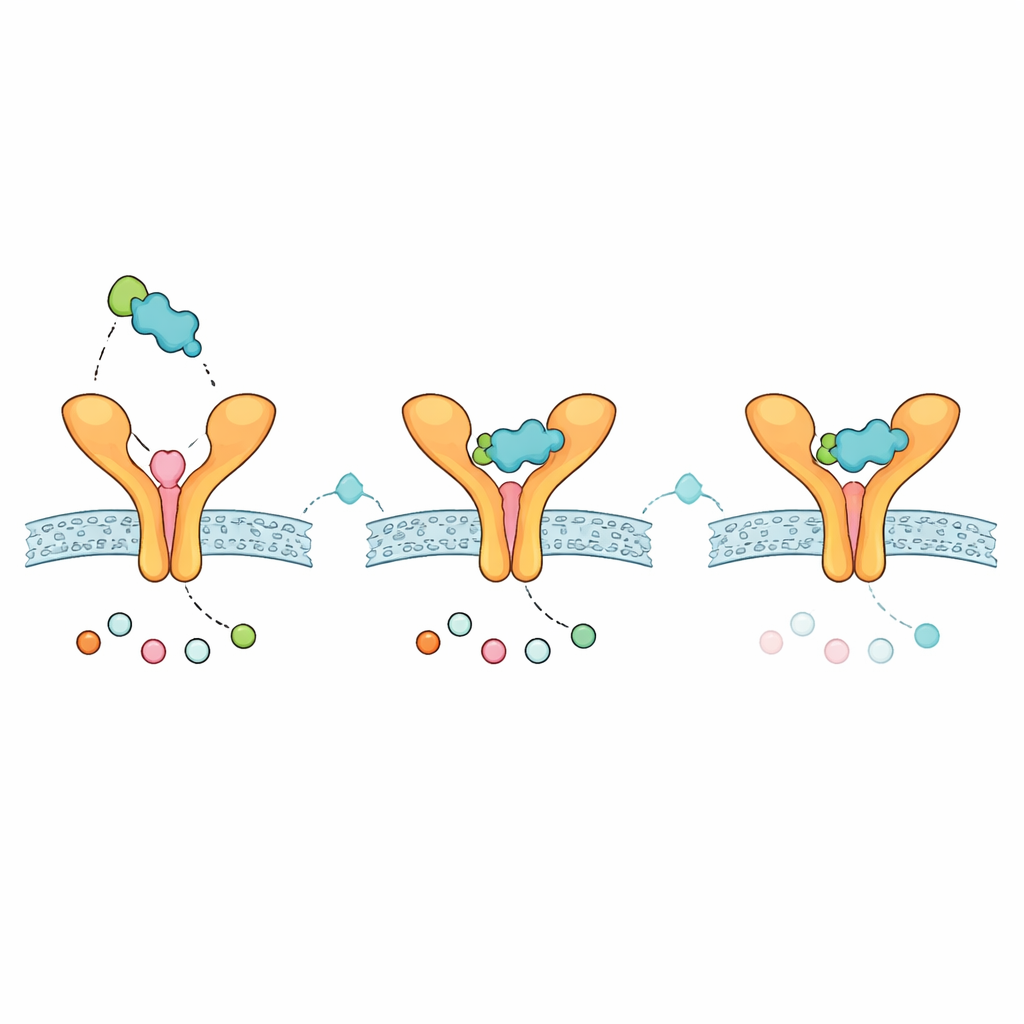
将来の吸入薬の挙動に関する手がかり
修飾ザフィルルカストが薬として妥当かどうかを検討するため、チームは吸収、分布、代謝、排泄、毒性(ADMET)の標準的な計算チェックを実施しました。類縁体は一般的な経口薬らしさのルールを満たし、中程度のサイズと脂溶性を示し、脳への移行が少ないと予測されました。これらは全身性の副作用が限定された肺局所治療として好ましい特徴となり得ます。溶解度の推定はモデルによってばらつきがあり、特に吸入のような非経口投与経路では慎重な製剤化が必要であることを示唆しています。また、この化合物は特定の肝酵素と相互作用する可能性が予測され、他の薬剤と併用する場合の薬物相互作用に注意が必要であることを示しています。
この研究が本当に示すこと
本研究は新たな喘息薬を提供するのではなく、気道細胞表面にあるIL-33/ST2の警報システムを阻害し得る小分子を見つけて改良するための段階的な計算戦略を実証しています。ザフィルルカストとAIで最適化したその類縁体を、ST2インターフェースの重要領域を占めうる実験開始点として示し、広く許容され得る安全性と薬物様特性を予測で示しました。しかし、すべての証拠は仮想的なものであり、これらの分子がIL-33のST2結合を実際に阻害するか、炎症シグナルを抑制するか、患者の呼吸を改善するかを証明するものではありません。それらの答えは生化学試験、細胞実験、動物モデル、最終的には臨床試験が必要です。現時点では、本研究は計算上のロードマップと、研究者が体内の喘息の警報スイッチを実用的な吸入可能な薬剤標的に変えようとする際の候補骨格の短いリストを提供しています。
引用: Sun, G., Liu, Q., Yu, M. et al. In Silico identification of inhalable small-molecule IL-33/ST2 antagonists for severe type-2-high asthma endotypes. Sci Rep 16, 7996 (2026). https://doi.org/10.1038/s41598-026-39027-z
キーワード: 重度喘息, IL-33 ST2経路, 小分子拮抗薬, インシリコ薬物設計, 吸入治療薬