Clear Sky Science · ja
A2-パンコルチンがBcl-xLおよびWAVE1と相互作用してミトコンドリア–小胞体接触部位(MERCs)を促進し、ミトコンドリア内カルシウム上昇を悪化させて新生児脳卒中における細胞死を媒介する
新生児の脳で小さな接点が重要な理由
脳卒中は成人の病気と考えられがちですが、新生児に発生すると発達中の脳に静かに損傷を与え、 lifelong な問題を引き起こすことがあります。本研究はそのような危機の際に神経細胞の奥深くで何が起きるかを探ります。著者らはパンコルチンと呼ばれるあまり知られていないタンパク質群に着目し、発達期に発現する2つのアイソフォームが危険な“増幅因子”のように働き、主要な細胞構造間の接触を強めて大量のカルシウム流入を促し、若いニューロンを死へと追いやる仕組みを示します。
新生児脳に潜む見えにくい原因
パンコルチンは発達中の脳の形作りを助ける足場(スキャフォールド)のようなタンパク質です。A2-パンコルチンと呼ばれる2つの形は発達初期に多く存在し、脳が成熟するにつれてほとんど消失します。新生児の脳は酸素不足に特に脆弱であるため、研究者らはこれらの発達期タンパク質が新生児脳卒中で皮質への血流が一時的に途絶した際の損傷を悪化させるかどうかを検討しました。培養したマウス皮質ニューロンで、遺伝学的手法によりパンコルチンをすべて低下させてから、脳卒中を模倣する酸素・グルコース欠乏条件にさらしました。パンコルチンを減らしたニューロンは生存率が著しく高く、これらのタンパク質は若い細胞を保護するどころか、ストレス下で損傷へと導くことを示唆しました。
マウスの脳卒中モデルから救われた脳組織へ
この有害な役割が生体内でも起きるかを確認するため、研究チームは発達期のA2-パンコルチンを特異的に欠くマウスを作製しました。生後2週間の若いノックアウトマウスと正常な同腹子は、虚血性脳卒中の標準モデルである大脳動脈の閉塞にさらされました。1日後、両群とも深部脳領域に損傷を示しましたが、A2-パンコルチン欠損マウスの皮質損傷は正常マウスの約半分でした。注目すべきことに、この保護効果は5週齢のマウスでは消失し、成体型のパンコルチンが優勢になると見られました。これらの年齢依存的な結果は、A2-パンコルチンが新生児皮質における主要な細胞死促進因子であり、発達プログラムが脳卒中感受性に結びつくことを示しています。
ニューロン内部の危険な接触領域
細胞内部では、エネルギーを生産するミトコンドリアがカルシウムを蓄える小胞体(ER)に近接して配置されています。両膜が近接する場所、いわゆるミトコンドリア–ER接触部位は、カルシウムが通過する微小なトンネルとして機能します。適度な移動はエネルギー産生を支えますが、過剰になるとミトコンドリアが過負荷になり細胞死を引き起こします。研究者らは、A2-パンコルチンがBcl-xLおよびWAVE1という2つのパートナーと共に、これら接触部位に局在する三者複合体を形成することを見出しました。A2-パンコルチンとこれらのパートナーを過剰発現させると、スプリット蛍光センサーの報告でミトコンドリアとERの接触頻度と密接度が高まることが示されました。GRP75と呼ばれるテザリング蛋白もこの複合体に加わり、接触領域の安定化に寄与していました。
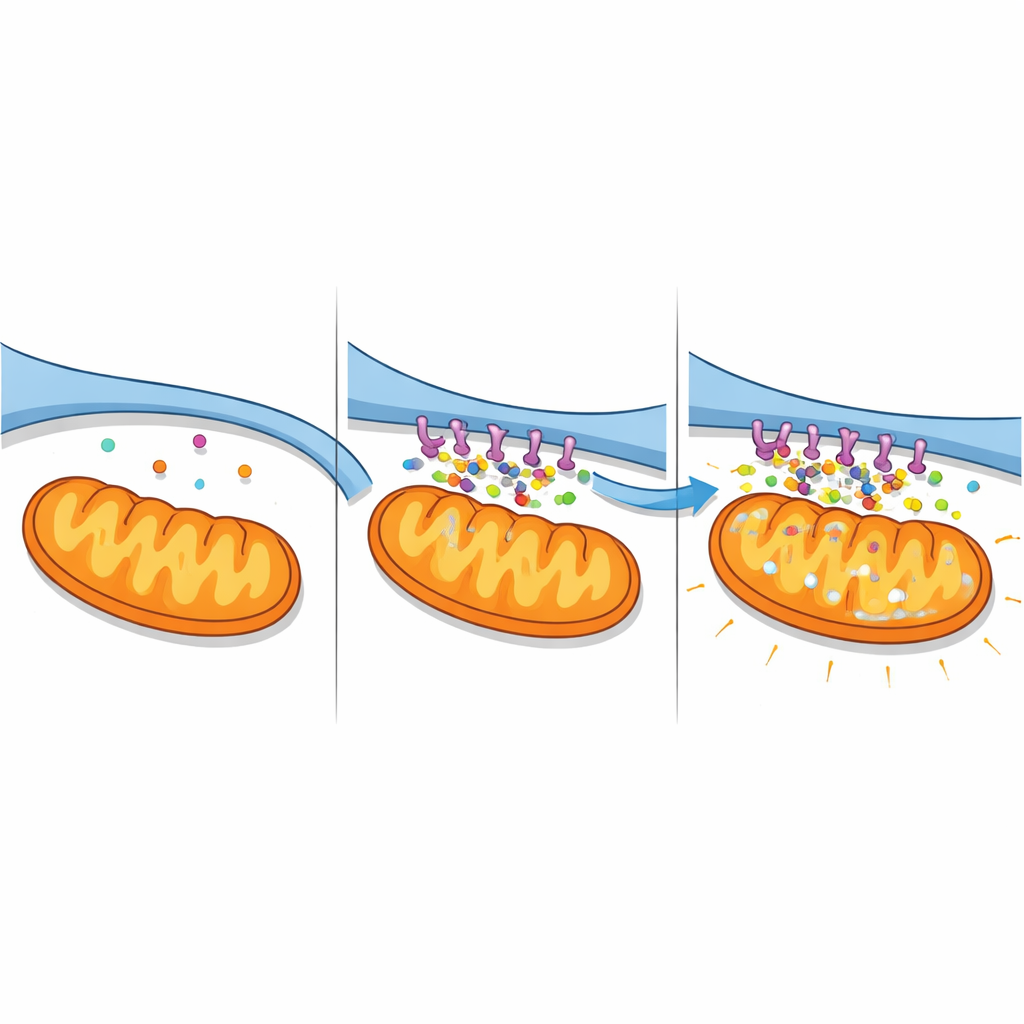
カルシウムの洪水と機関の失敗
強化された接触はカルシウムの恒常性に深刻な影響を及ぼしました。細胞質、ER、ミトコンドリア内のカルシウムを別々に報告する蛍光指標を用いて、著者らは時間経過での変化を観察しました。A2-パンコルチン複合体を発現する細胞では、ミトコンドリア内と周囲の細胞質でカルシウムが持続的に上昇し、ER貯蔵は減少しました。これはERからミトコンドリアへの大規模な移動の特徴です。ER表面の主要なカルシウム放出チャネル(IP3R)を阻害するとこれらの変化は大部分が抑えられ、この複合体が特定のER→ミトコンドリア経路を増幅することが裏付けられました。脳卒中様の酸素・グルコース欠乏にさらされた神経様細胞では、パンコルチンをノックダウンすると逆の効果が生じ、カルシウム過負荷は鈍りER貯蔵はより良く保持されました。これらの発見は、A2-パンコルチンが虚血ストレス下で致命的となるカルシウムの“スーパー・ハイウェイ”を組織化することを明らかにします。
新生児の脳を守るための意味
専門外の方への要点は、本研究が若いニューロンが脳卒中後に生き残るか死ぬかを決める新しい分子スイッチを同定したことです。カルシウムを貯える膜と細胞の発電所であるミトコンドリアの微小な接合部を強化することで、A2-パンコルチンはミトコンドリアに過剰なカルシウムを引き起こし機能不全に導きます。若いマウスからこれらのタンパク質を除くと実験的脳卒中の影響が緩和され、A2-パンコルチン複合体を破壊する薬剤や遺伝子治療、あるいはそれらが強化する接触部位を緩める方法がいつか新生児の脳損傷を軽減する可能性を示唆します。こうした治療法は将来の課題ですが、本研究は発達期タンパク質からカルシウム過負荷、ニューロン喪失へと至る明確で検証可能な経路を描き出しました。
引用: Yang, Q., Wang, CC., Matsuyama, T. et al. A2-pancortins interact with Bcl-xL and WAVE1 to promote mitochondria-ER contact sites (MERCs) and exacerbate mitochondrial calcium elevation to mediate cell death in stroke. Sci Rep 16, 8467 (2026). https://doi.org/10.1038/s41598-026-38928-3
キーワード: 新生児脳卒中, ミトコンドリア–小胞体接触部位, カルシウム過負荷, パンコルチンタンパク質, 神経細胞死