Clear Sky Science · ja
極限環境性Ts2631エンドリシンの熱安定性を決定する残基レベルの要因
将来の抗生物質にとって熱を好むウイルスが重要な理由
抗生物質耐性が進む中、危険な細菌を殺す新しい方法を見つけるために研究者たちは急いでいます。有望なアプローチの一つは細菌に感染するウイルス、バクテリオファージが持つ武器を借用することです。これらのウイルスはエンドリシンと呼ばれる酵素を生産し、細菌の細胞壁に穴を開けます。ここで取り上げる研究は、アイスランドの温泉に生息するウイルス由来の非常に耐熱性の高いエンドリシンTs2631に注目しています。このタンパク質が沸点近くの温度でも極めて安定でいられる理由を個々の構成要素(残基)レベルで明らかにすることで、医療やバイオテクノロジー向けにより丈夫で寿命の長い抗菌酵素を設計する手がかりを得ようとしています。 
沸騰する温泉で鍛えられたウイルスの道具
Ts2631は耐熱性細菌Thermus scotoductusに感染するバクテリオファージ由来で、この細菌は60 °Cを大きく上回る水温でも生育します。Ts2631酵素は細菌細胞を取り囲む強固なメッシュであるペプチドグリカンの特定の結合を切断します。Ts2631が際立っているのはその極端な熱安定性で、溶液条件にもよりますが約100–105 °Cまで折りたたまれた構造を保ちます。これはほとんどのタンパク質が崩れる温度をはるかに上回ります。著者らは、Ts2631を温和な温度域のウイルス由来で最もよく研究されている近縁のT7リゾイムと比較して、Ts2631が厳しい環境下でも形を保つために自然が使った構造的トリックを探りました。
短いループと異なる残基の組み合わせ
タンパク質は20種類のアミノ酸がつながって折りたたまれた鎖です。研究者らがTs2631とT7リゾイムの3次元構造を重ね合わせると、全体のアーキテクチャは非常によく似ており、どちらもコンパクトなヘリックスとシートのコアを持っていました。鍵となる違いはそれらをつなぐ柔軟なループ領域にありました。Ts2631ではこれらのループが短く柔軟性が低いのに対し、T7リゾイムはループが長くより自由度が高いのです。さらにTs2631は耐熱性に関連することが多い特定のアミノ酸をより多く含んでいました:剛直なプロリン、チロシンやトリプトファンのような芳香族残基、そして正に帯電するアルギニン。一方で高温で脆弱になりやすいセリン、アスパラギン酸、グルタミン酸は少なめでした。この傾向はT7リゾイムとの比較だけでなく、Ts2631を数十万のウイルス性タンパク質や数百万の細菌性タンパク質と比較しても一貫して見られました。
単一残基を置換して重要性を試す
相関から因果へ進むために、研究チームはTs2631の55か所の個々のアミノ酸を体系的に置換し、各変異が融解温度(Tm)と細菌細胞壁分解能にどのように影響するかを測定しました。亜鉛を含む活性部位周辺のいくつかの変化は特に有害でした。亜鉛を配位する3つの残基(H30、H131、C139)を変えると、タンパク質のTmは最大で約20 °C低下し、活性は失われました。保存された2つのチロシン(Y60とY69)も安定性に寄与していました。驚くべきことに、システインC80とC90間のジスルフィド結合(システイン間の共有結合)を取り除くと、活性は失われたものの融解温度はむしろ上昇しました。これは、試験管内で極めて安定であることが必ずしも実際の条件で機能が向上することを意味しないことを示しています。 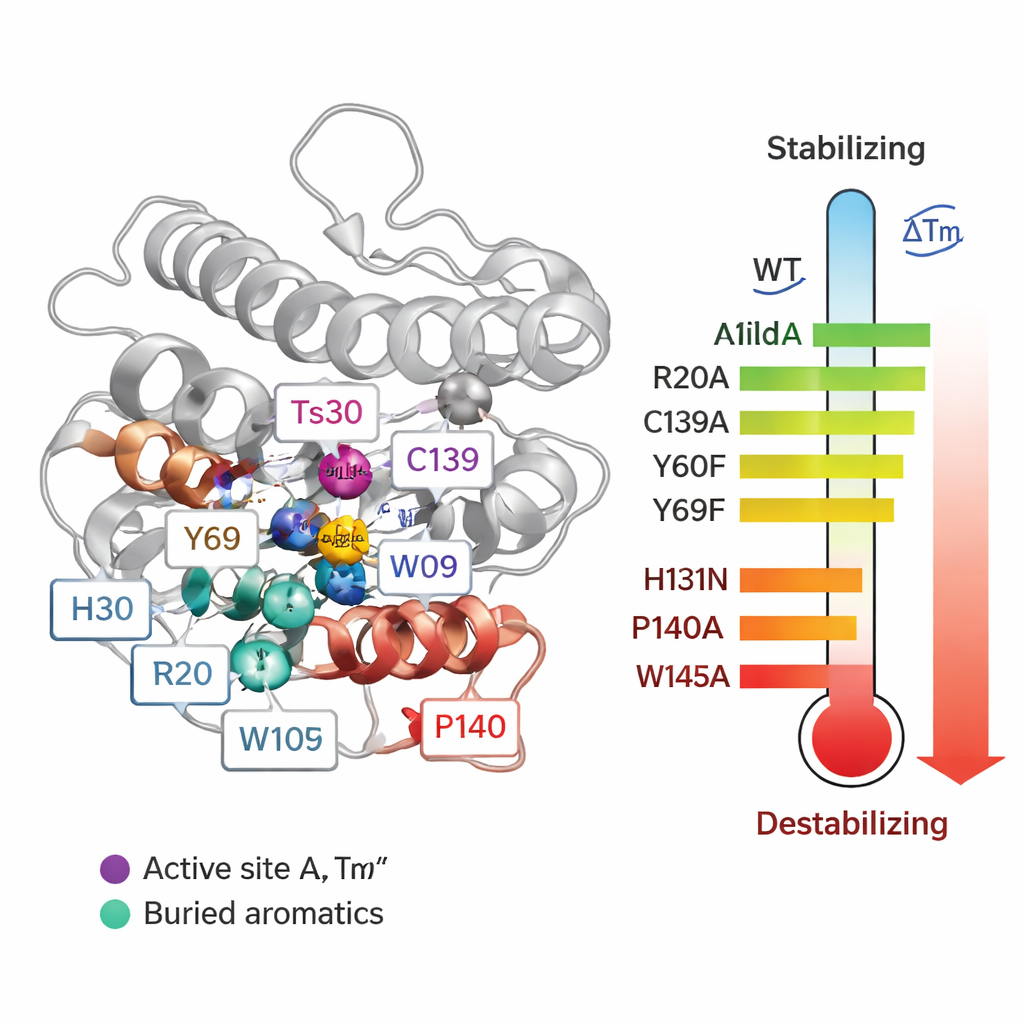
隠れた芳香族の“係留点”と細胞壁への重要な把持
最も顕著な結果はプロリンとトリプトファン残基の変異から得られました。亜鉛結合C139のすぐ隣にある単一のプロリン(P140)を変えると、Tmは21 °C以上低下し、加熱後の活性も弱まりました。これは金属結合に必要な特別な結合幾何が乱されたためです。深く埋め込まれたトリプトファン(W102、W109、特にW145)も重要で、これらをアラニンに置換するとTmは14–24 °C低下し、活性試験での耐熱性が大幅に低くなりました。こうした芳香族残基はタンパク質コアをロックする内部の係留点として働きます。アルギニンの中ではほとんどが安定性に大きな影響を与えませんでしたが、R20はペプチドグリカンの把持に不可欠でした。R20を置換すると酵素の細胞壁結合が弱まり、加熱で活性を失ってしまい、一部の残基は純粋な熱安定性よりも機能に対して重要であることが明らかになりました。
温泉酵素からより強靭な抗菌薬へ
総じて、この研究はTs2631の卓越した耐熱性がタンパク質全体の均一な強化ではなく、少数の適所に配置されたアミノ酸に依存していることを示しています。亜鉛結合残基、活性部位近傍の保存されたプロリン、埋め込まれた芳香族側鎖が安定化コアを形成しており、ジスルフィド結合や塩橋のような古典的な安定化要素がここでは期待ほど重要でない場合もあります。広い分野への示唆としては、中温性(メソフィル)エンドリシンも特定の位置をトリプトファンやプロリンに慎重に置換することで耐久性を高められる可能性があり、抗菌活性を犠牲にせずに実用的なタンパク質ベースの抗生物質をより信頼性高く長持ちさせるための設計図を自然から学べるということです。
引用: Cieminska, K., Kaczorowska, AK., Kozlowski, L.P. et al. Residue-level determinants of the thermal stability of the extremophilic Ts2631 endolysin. Sci Rep 16, 7630 (2026). https://doi.org/10.1038/s41598-026-38786-z
キーワード: 耐熱性エンドリシン, バクテリオファージ酵素, タンパク質の熱安定性, 抗生物質耐性, タンパク質工学