Clear Sky Science · ja
ConvAHKG: 薬物リポジショニングのための二重チャネル畳み込みアプローチを備えた作用ベースのハイブリッド知識グラフ
既存薬の新たな用途を見つける
まったく新しい薬を市場に出すには10年以上かかり、数十億ドルの費用がかかることがあり、多くの候補が途中で脱落します。本研究は賢い近道を探ります。すなわち、データと人工知能を用いて、既に承認されている薬が安全に治療できる可能性のある新しい疾患を発見するという手法です。著者らはConvAHKGと呼ばれるフレームワークを提示しており、さまざまな種類の生物医学情報を一つの連結された地図に編み込み、最新のニューラルネットワークで有望な薬—疾患の組み合わせを見つけ出します。これにより、新しい治療法への道がより速く、より安価になる可能性があります。
薬と疾患の相互作用を豊かに表す地図
この研究の中心には「ハイブリッド知識グラフ」があります。これは薬、疾患、タンパク質、副作用、化学構造、生物学的経路を互いに結ぶ巨大な地図です。単純な有無のリンク(例えば「薬Aは疾患Bを治療する」)だけを記録するのではなく、薬がタンパク質に対してどのように作用するか—活性化、阻害、結合など—や、タンパク質がバイオマーカーとして作用するか、活性が変化するなど、疾患にどう関与するかを記録します。グラフは11,000以上のエンティティと59種類の関係を含み、薬の分類、副作用、タンパク質間接触、化学的部分構造などの詳細情報を備えています。こうした多層の文脈を捉えることで、治療効果や有害反応の背後にある実際の生物学的複雑性をよりよく反映できます。 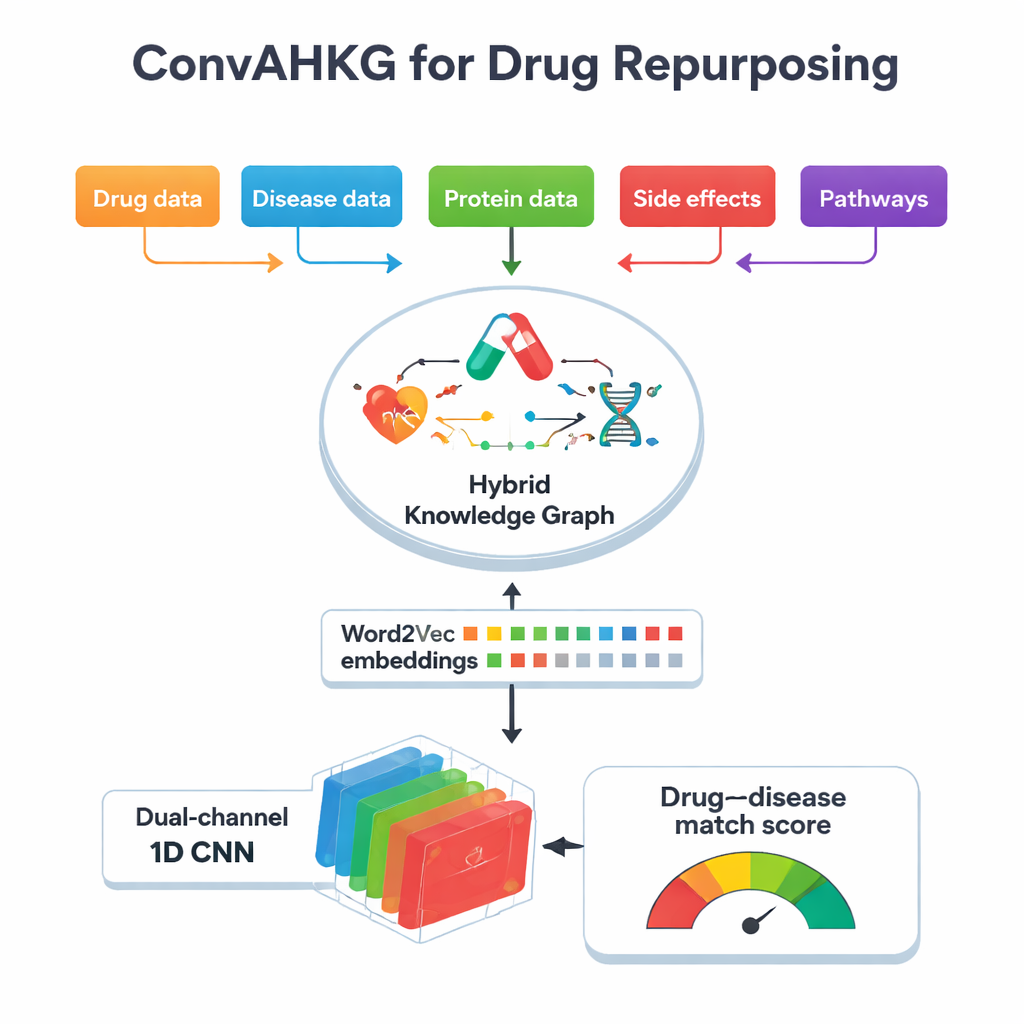
コンピュータに生物学の言語を教える
この複雑な地図を機械学習で利用可能にするために、チームはグラフ内の各接続を単純な三部構成の「文」に変換します:ヘッド(例えば疾患)、関係(例えばバイオマーカー)、テイル(例えばタンパク質)。次に、自然言語処理向けに開発されたWord2Vecという手法を適用して、すべての薬、疾患、タンパク質に数値的な「埋め込み」を学習させます。これらの文でしばしば一緒に現れる項目は、この数学空間で互いに近く配置され、テキスト中で意味が似た単語が近くなるのと同様の効果を生みます。このアプローチは多くのグラフ固有の埋め込み手法よりずっと単純で高速ですが、微妙なパターンも捉えます。いくつかの一般的な知識グラフ埋め込み手法と比較したテストでは、Word2Vecは予測性能で同等かそれ以上を示し、計算時間も大幅に少なかったと報告されています。
治療の可否を判定する二重のニューラル経路
各薬と疾患が数値ベクトルに翻訳された後、ConvAHKGはそれらを二重チャネルの1次元畳み込みニューラルネットワークに入力します。1つのチャネルは薬のベクトルを、もう1つのチャネルは疾患のベクトルを処理し、局所的なパターンやより広いモチーフを検出する連続した畳み込みフィルタを適用します。これはInceptionNetやAlexNetなどの画像認識設計に触発されたものです。この個別処理の後、2つのストリームを結合し、複数の全結合層を通して単一の確率を出力します。それはこの薬–疾患ペアが有効な治療である可能性が高いか、むしろ有害な副作用であるかを示します。既知の正例が負例より遥かに稀であるという事実に対処するため、著者らは見逃した真の治療をより重く罰する重み付き損失関数を導入しており、見つけにくいケースでの性能を改善しています。 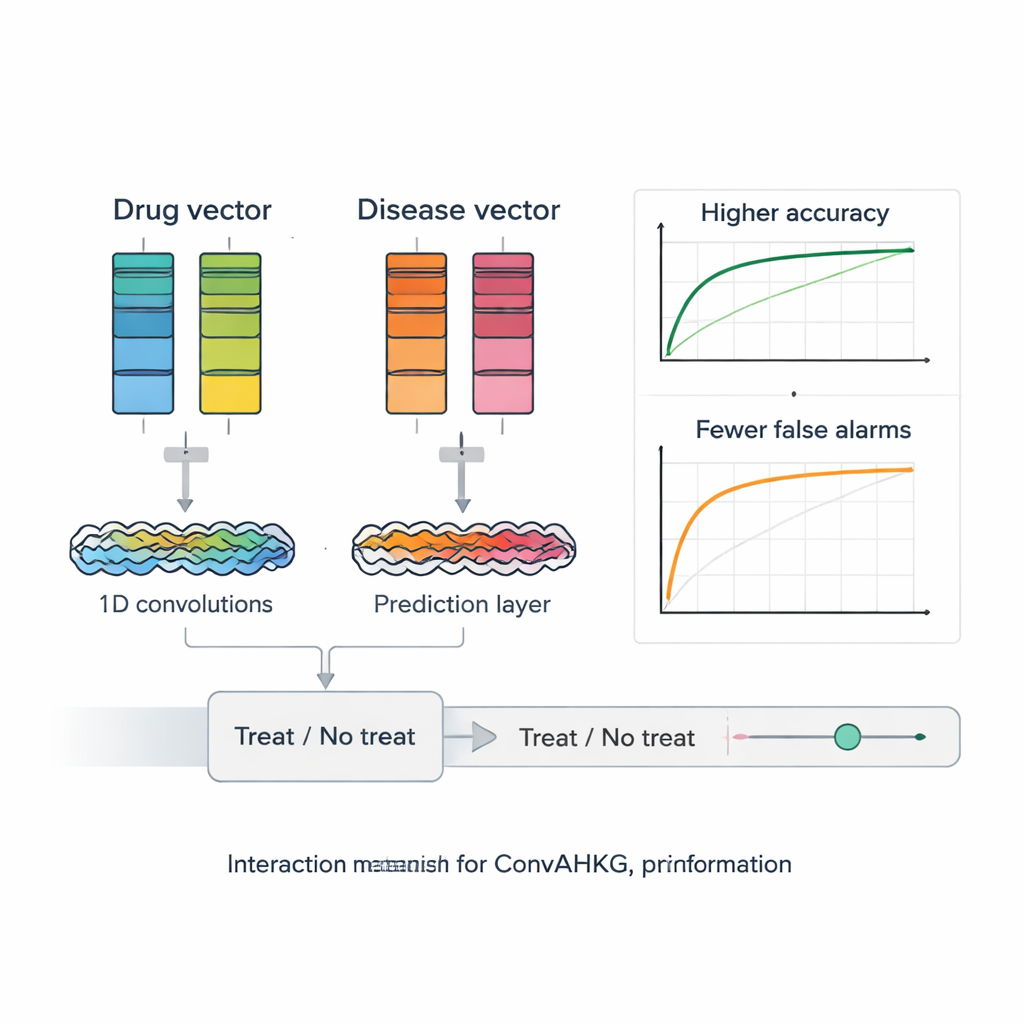
既存手法を上回り、がん候補薬を発見
研究者らはこのフレームワークを、行列分解、グラフニューラルネットワーク、深層オートエンコーダを用いる複数の最先端の薬物リポジショニング手法と厳密に比較検証しました。ConvAHKGはROC曲線下面積で0.9836、精度–再現率曲線下面積で0.9686を達成し、同じベンチマークデータセット上で競合するすべての手法を上回りました。次にモデルを非小細胞肺がん(世界で最も一般的かつ致死性の高い肺がんの形態)に適用したところ、従来この疾患の治療薬としてラベル付けされていなかった複数の薬を指摘しました。その中にはHER2タンパク質を標的とし、肺がんでの臨床的証拠をすでに支持する抗体トラスツズマブや、その他の生物製剤、さらには従来型の抗生物質であるベンジルペニシリンも含まれます。ドッキングシミュレーションは、ベンジルペニシリンがDNAやトポイソメラーゼIIα(これらの腫瘍でしばしば上昇する酵素)に強く結合する可能性を示唆しており、実験室での検証に値する抗がんメカニズムの可能性を示しています。
なぜ患者にとって重要なのか
平たく言えば、ConvAHKGは既存薬と疾患の間で高度に情報化された仲介者のように機能します。詳細な生物学的作用の地図と強力なパターン認識エンジンを用いて、既存の薬が新しい適応で有効である可能性を予測します。安全性が検証された薬を単一目的の道具ではなく再利用可能な構成要素と見なすことで、このフレームワークは特に従来の創薬が遅すぎたり費用がかかりすぎる場合に、肺がんのような疾患に対する治療の発見を加速できる可能性があります。予測は依然として慎重な実験的および臨床的検証を必要としますが、本研究は豊富な生物学的知識と最新のAIを組み合わせることで探索空間を大幅に絞り込み、潜在的に命を救う治療をより速く手に届くものにできることを示しています。
引用: Khodadadi AghGhaleh, M., Abedian, R., Zarghami, R. et al. ConvAHKG: Action-based hybrid knowledge graph with a dual-channel convolutional approach for drug repurposing. Sci Rep 16, 7592 (2026). https://doi.org/10.1038/s41598-026-38656-8
キーワード: 薬物リポジショニング, ナレッジグラフ, 深層学習, 肺がん, 創薬