Clear Sky Science · ja
現場での複合化合物合成とネイティブ質量分析によるガレクチン‑3結合剤の最適化
将来の医薬品にとっての意義
多くの現代医薬品は体内のタンパク質に結合して作用しますが、正確な部位に選択的かつ強く結合する低分子を見つけるのは遅く、コストがかかり、しばしば骨折りな作業です。本研究は、標的タンパク質の存在下で直接こうした分子を迅速に最適化し、非常に感度の高い質量測定法で勝者を読み出す手法を示します。著者らはこの手法をがん増殖に関連するタンパク質ガレクチン‑3に適用し、既存の優れた化合物に匹敵するほど強く結合する有望な薬物様候補を得ましたが、それは予期せぬタンパク質表面のポケットに結合していました。

薬物リード探索の再考
従来の薬物最適化は高価な推測の繰り返しに似ています。化学者は出発化合物を段階的に変更して各バージョンを試験し、標的タンパク質への結合を改善できることを期待します。しかしタンパク質表面は可塑性があり、水分子が介在し、結合そのものがタンパク質の形を変えることがあるため、計算予測は信頼できないことが多い。高解像度構造が得られても、提案された変更が有効である保証はありません。既存の「ターゲット誘導」法はタンパク質に構成要素を選ばせる試みですが、真に最良の結合を示す化合物を推定するには依然として複雑な解析や間接的な指標に頼らざるを得ません。
タンパク質に選ばせ、勝者を秤にかける
研究者らは二つの考えを一つの効率的なワークフローに組み合わせました。まず、共通の糖を基幹に可逆的に結合させる化学反応を用い、1本の試験管内で多数の異なる側鎖をつけた関連化合物の混合物を作成しました。出発物質の比率を慎重に調整することで、生成物は単純な濃度則で支配される平衡状態に落ち着き、反応性の違いによる量の偏りをある程度均すのに役立ちます。次にその混合物をガレクチン‑3に晒し、ネイティブ質量分析で調べました。ネイティブ質量分析はタンパク質―分子ペアを穏やかな(水に近い)条件で保持したまま測定できる質量分析法です。各候補は固有の質量を持つため、器械はラベルや参照標識なしにどの分子が実際にタンパク質に結合しているかを直接検出できます。
混雑した混合物から抜きん出た結合子へ
このセットアップを用いて、研究チームは既知の阻害剤GB1107に着想を得た糖基に様々な側鎖を付けて数十種のガレクチン‑3結合体を作成しました。35種の異なるヒドラジド断片を扱いやすいグループに分け、すべての組み合わせを現場で合成してからガレクチン‑3を加えました。ネイティブ質量分析はタンパク質と共に最も頻繁に検出された化合物を特定し、それらを一次ヒットとして示しました。ガス相での測定に起因する偽陽性を除外するため、化合物が加熱下でタンパク質を安定化させる程度を測る熱安定性テストを追試し、三つの主要候補が残りました。さらに詳細な熱に基づく結合測定により、GalAldBZ20と呼ばれる一つが特に強く、亜マイクロモル領域でガレクチン‑3に結合することが示されました。
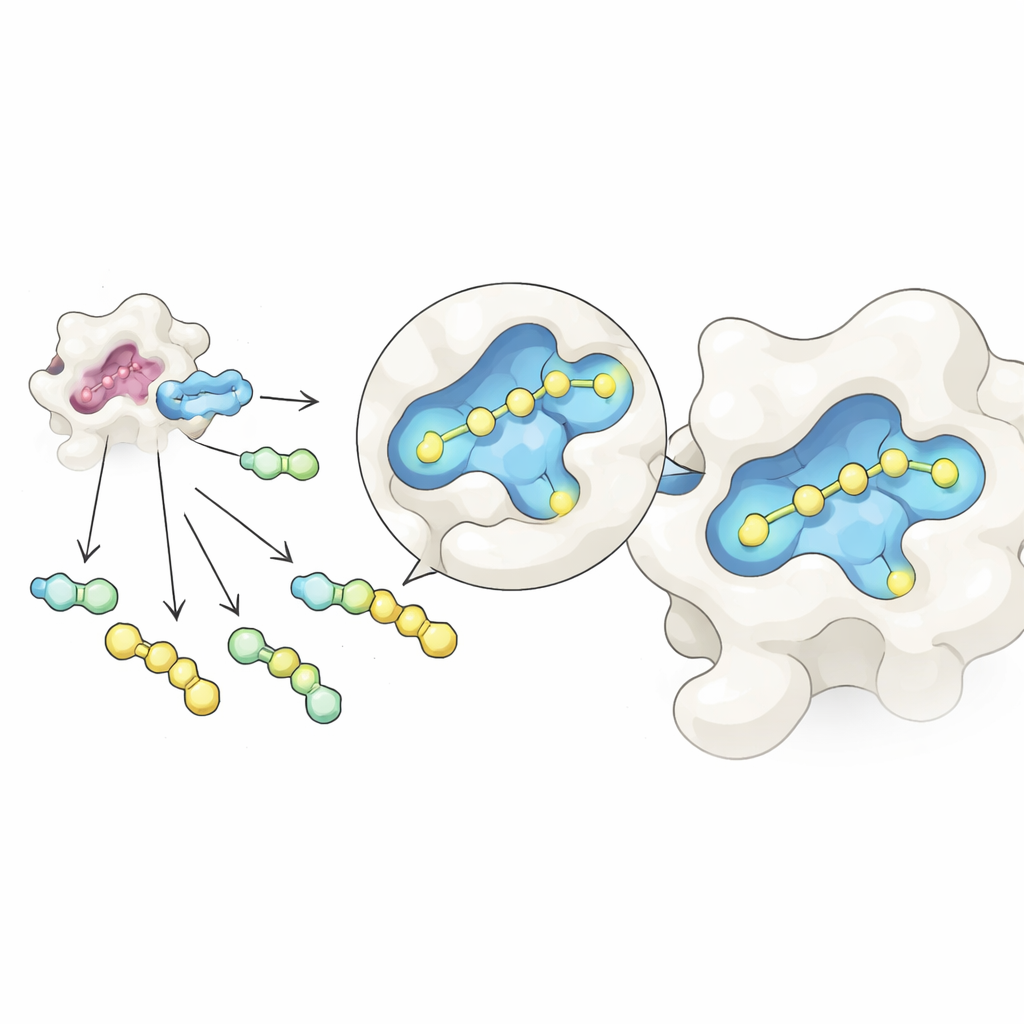
隠れたポケットの発見と強化
次の驚きは、GalAldBZ20がガレクチン‑3表面にどのように位置しているかを調べたときに訪れました。既知の多くの結合子は糖結合部位に近い「アルファ」ポケットを利用しますが、構造解析と計算シミュレーションはGalAldBZ20が代わりに隣接する「ベータ」ポケットを好むことを示しました。X線結晶解析がその可能性を示唆し、溶液中の核磁気共鳴はその近傍で複数の局所的な立体配座を明らかにし、分子動力学シミュレーションは分子上のニトロ基を含む芳香環がベータ部位に収まるというモデルを支持しました。研究者らはこの配座をより確固たるものにできると考え、糖部とニトロ芳香環をつなぐリンカーを再設計して新たな極性相互作用を促し、柔軟性を低減させました。
巧妙なスクリーニングを強力な候補へ
この知見に基づき、チームは同じ糖とニトロ芳香環を維持しつつ接続子を変えたより剛直な追試化合物の小さなセットを合成しました。そのうち一つ、N‑ガラクトシド(化合物5)が際立ちました。これは元のヒットより約10倍強くガレクチン‑3に結合し、GB1107に匹敵する結合強度に達しながら、依然としてベータポケットを好みました。超高解像度の結晶構造では、そのベータポケットに収まるニトロ芳香環の明瞭な電子密度が観察され、複数の水素結合や重要なアミノ酸とのカチオン‑π相互作用に支えられていました。ニトロ基を除去するか簡単なメチル基に置換すると結合は著しく弱まり、その重要性が明らかになりました。ガレクチン‑1のような類縁タンパク質はこのベータポケットを欠くため、新規化合物は最終的により高い選択性を示す可能性があり、これは薬剤設計で望まれる特性です。
将来の創薬にとっての意義
わかりやすく言えば、この研究は多くの関連化合物を混ぜ合わせ、疾患に関係するタンパク質に「選ばせ」、そのタンパク質–分子ペアを直接秤にかけてどれが最もよく付着するかを見ることができると示しています。ガレクチン‑3に適用した例では、この戦略は予期せぬポケットでの結合を発見しそれを強化することに成功し、既存の優れた阻害剤に匹敵する化合物を生み出し、新たながん治療薬のリードとなり得ます。より広く見れば、現場での化学合成とネイティブ質量分析の組み合わせは、複数の結合部位を持つタンパク質に対するリード化合物の洗練化に汎用的な近道を提供し、創薬初期段階の時間、資材、労力を節約する可能性があります。
引用: Hoshi, K., Konuma, T., Taguchi, R. et al. Optimization of galectin-3 binding agents by in situ multiple compound synthesis and native mass spectrometry. Sci Rep 16, 8453 (2026). https://doi.org/10.1038/s41598-026-38570-z
キーワード: ガレクチン‑3阻害剤, ネイティブ質量分析, フラグメントベース薬物探索, ターゲット誘導合成, がん治療候補化合物