Clear Sky Science · ja
非ヒドロキシマート型[1,2,4]トリアゾロ[4,3-a]キノリン化合物によるHDAC8の標的阻害
小児がんに向けた新たな希望
神経芽細胞腫は神経細胞由来の攻撃的な小児がんで、転移すると治療が難しくなることが多い。本研究は、HDAC8と呼ばれる重要な細胞内スイッチをオフにすることで、神経芽細胞腫細胞の増殖を抑えるか死滅させる新たな方法を探るものだ。研究者たちはこのスイッチに非常に選択的に作用する新しい薬様分子群を構築することで、腫瘍に対してより効果的で、全身に対しては副作用の少ない治療の実現を目指している。
がんの中心にある分子スイッチ
細胞内では遺伝子が常にオン・オフされている。重要な制御機構の一つは、DNAに関わるタンパク質に付くアセチル基と呼ばれる小さな化学タグに依存している。ヒストン脱アセチル化酵素(HDAC)と呼ばれる酵素はこれらのタグを除去し、DNAの梱包を締めて通常は遺伝子活性を抑える。HDAC8はこの酵素ファミリーの一員で、神経芽細胞腫を含むいくつかのがんと関連している。HDAC8が過剰に活性化するとがん細胞はより容易に増殖・生存・転移できるようになり、したがって新規薬剤の魅力的な標的となる。
従来のHDAC薬の限界
いくつかのHDAC阻害薬は既に血液がんの治療薬として承認されているが、これらは多くのHDAC種類を一度に抑える傾向がある。これらの大半は酵素の活性部位にある金属イオンを捉えるためにヒドロキシマートという化学基を用いる。確かに有効だが、この基は金属に非常に強く結合するため副作用を引き起こしやすく、異なるHDACを精密に区別する能力を制限してしまう。その結果、患者に毒性が現れ、がん細胞だけでなく正常細胞も損なわれる可能性がある。こうした理由から、がんに対する利点を維持しつつ望ましくないダメージを減らす代替的な化学設計が模索されてきた。
ターゲット型阻害剤の新規クラスの設計
本研究では、研究チームはトリアゾロキノリン骨格を中心に据え、柔軟なリンカーを介してHDAC8の活性部位にある亜鉛原子と結合し得るα-アミノアミド領域を持つ21種の新規化合物を設計・合成した。コンピュータ支援設計を用い、この構造がHDAC8特有の狭い“酢酸放出チャネル”に適合すると考えられ、高い選択性を実現しやすいと判断した。詳細なドッキング解析と分子動力学シミュレーションにより、特に9mおよび9rと呼ばれる複数の新規分子がHDAC8ポケット内で安定かつ持続的な相互作用を形成し、既知の参照阻害剤と同等かそれ以上の結合の強さを示すことが示された。重要なのは、生化学的検査により最良の化合物が他のHDACファミリーメンバーにはほとんど影響を与えずにHDAC8を強力に阻害することが確認された点である。
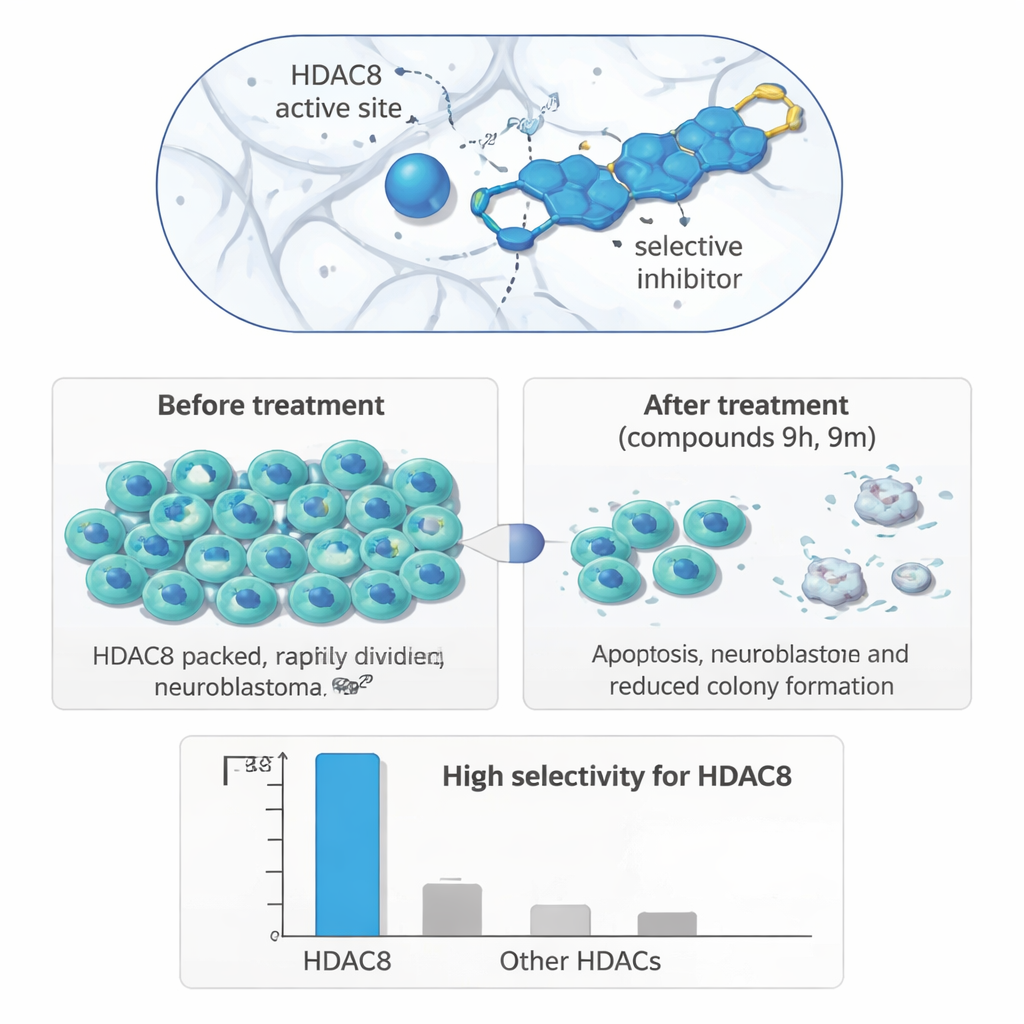
試験管から腫瘍細胞へ
この精密な酵素標的化が有用な生物学的効果に結びつくかを評価するため、研究者たちはヒト細胞株パネルで化合物を試験した。神経芽細胞腫細胞(IMR-32)では、9hと9mの2分子が際立っており、マイクロモル濃度で細胞増殖を抑制し、乳がんや大腸がん細胞、非がん性の腎細胞よりも神経芽細胞腫でより強い効果を示した。長期のコロニー形成実験では、処理された神経芽細胞腫細胞は薬剤暴露後の再増殖能力を大幅に失った。傷治癒アッセイ(細胞層のひっかき傷をどれだけ早く閉じるかを追跡する)では、両化合物が神経芽細胞腫細胞の移動を遅らせ、転移能の低下を示唆した。
化合物ががん細胞をどのように死滅させるかを探る
フローサイトメトリー実験により、9hおよび9mは神経芽細胞腫細胞でプログラム細胞死(アポトーシス)を誘導し、DNA損傷や死と関連する細胞周期の段階(Sub-G1)に細胞が蓄積することが明らかになった。これらの効果が本当にHDAC8阻害に由来するかを確認するため、研究チームは姉妹染色体の保持に関与する既知のHDAC8標的タンパク質であるSMC3のアセチル化状態を測定した。HDAC8が阻害されるとアセチル化SMC3が蓄積する。9hまたは9mで処理した後、アセチル化SMC3のレベルは急増したが、全SMC3タンパク質量は変化しなかった—これはこれらの化合物が生細胞内で直接HDAC8に作用し、染色体制御における通常の機能を撹乱している強い証拠である。
将来の治療に何を意味するか
化学、計算モデリング、酵素試験、細胞ベース実験を総合すると、新たに開発されたトリアゾロキノリン化合物は強力で非常に選択的なHDAC8阻害剤であり、他のHDAC酵素をほとんど触らずに神経芽細胞腫細胞の増殖と拡散を抑えられるという一貫した絵が浮かぶ。従来のヒドロキシマート基を回避しているため、HDAC8を治療標的として利用する際により安全な道を提供する可能性がある。動物実験や最終的な臨床試験などまだ多くの作業が残っているが、本研究は小児神経芽細胞腫やおそらくHDAC8が関与する他の疾患に対するより精密な薬剤開発の堅固な基盤を築くものだ。
引用: Bandaru, N.V.M.R., Fathima, A., Sengar, S. et al. Targeted HDAC8 inhibition with non-hydroxamate [1,2,4]triazolo[4,3-a] quinoline compounds. Sci Rep 16, 7472 (2026). https://doi.org/10.1038/s41598-026-38490-y
キーワード: HDAC8阻害剤, 神経芽細胞腫, エピジェネティック療法, トリアゾロキノリン, 標的化がん薬