Clear Sky Science · ja
ヒトiPSC由来ニューロンにおけるGluN2A依存性電流とカルシウムシグナル
なぜ試験管内で育てた小さな脳細胞が重要なのか
研究者たちは、自らの脳がどのように形成されるかを調べ、発達障害、てんかん、アルツハイマー病などで何がうまくいかなくなるのかを探るために、試験管で育てたヒトの脳細胞をますます利用するようになっています。本研究は単純だが重要な問いを投げかけます:こうして作られたニューロンは、本物のヒト脳と本当に似た形で成熟し配線されるのか。特にグルタミン酸という重要な化学信号をどのように扱うかという点で。本研究の答えは、より現実的な“ミニ脳”モデルの構築方法を示し、脳の健康や疾患を調べる新たな手がかりを提供します。
再プログラムされた細胞からニューロンを作る
研究者たちはヒト誘導多能性幹(iPS)細胞から出発しました――通常の細胞を「再プログラム」して幹細胞状態に戻したものです。そこから神経前駆細胞へと誘導し、最終的にニューロンと支持細胞であるアストロサイトのネットワークを形成させ、人間の皮質発生を模倣しました。彼らは二つの広く使われる培養条件を比較しました。一つはBrainPhys培地と呼ばれ、活動的で電気的応答性の高いニューロンを促進し、アストロサイトをより多く生みやすいよう設計されています。もう一方は従来の神経維持用培地で、アストロサイトが少ないニューロンを優勢にします。60日間にわたり外観、遺伝子発現、細胞タイプの変化を追跡したところ、BrainPhys培養はより精巧なニューロン形態を発達させ、ニューロン対アストロサイト比がヒト脳に近い結果を示しました。
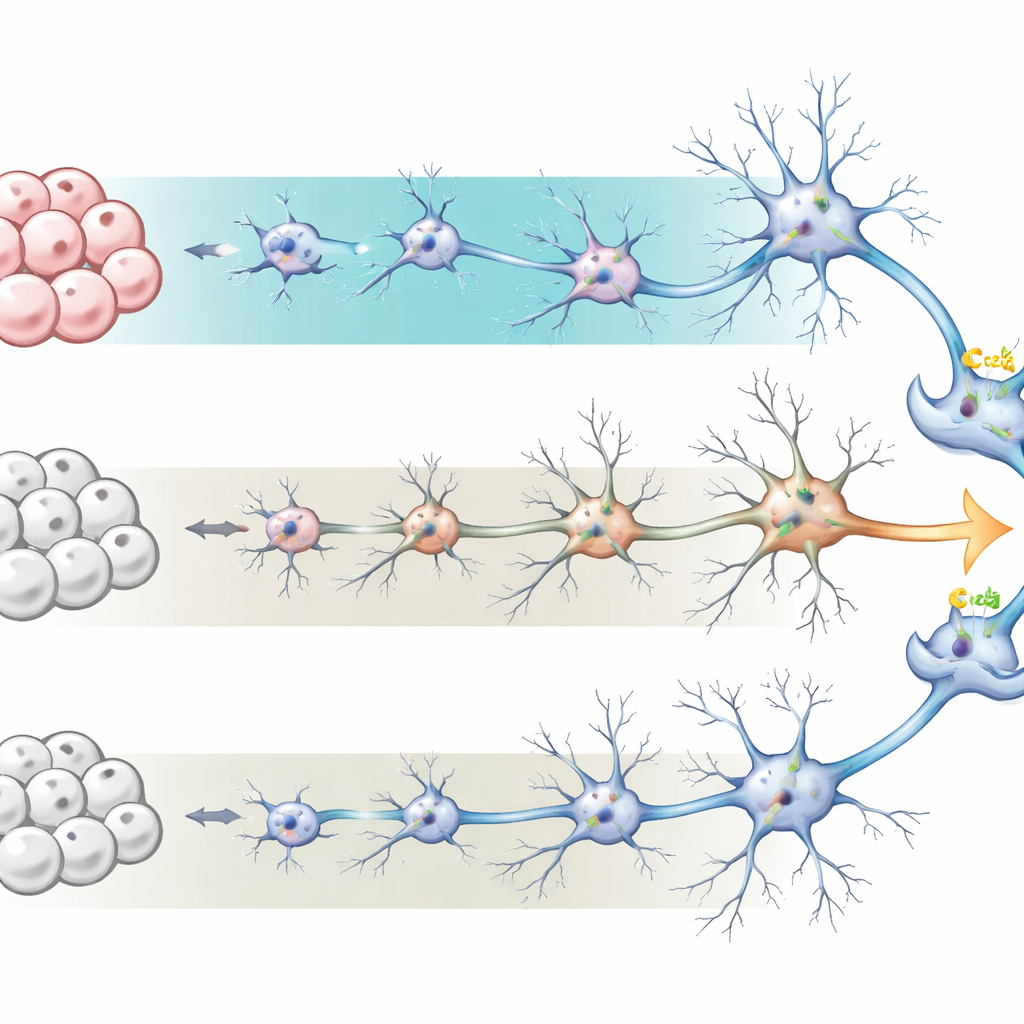
細胞が成熟している兆候
ニューロンがどれだけ「成熟」しているかを見るために、チームは60日目にRNAシーケンシングで全体的な遺伝子発現を測定しました。BrainPhysで育てられた細胞は、標準培地と比べてほぼ2,000遺伝子が有意に発現変動を示し、多くはニューロン分化、シナプス形成、電気活動に関連していました。アストロサイト機能や炎症に関連する遺伝子も高く、アストロサイト集団の増加を反映しています。これらのパターンは、BrainPhys培養がより進んだ発達段階を再現しており、ニューロン間の通信点が洗練され、支持環境が生体組織に近づいていることを示唆します。
化学的コミュニケーションの重要なスイッチ
脳の成熟の特徴の一つは、NMDA受容体の構成の変化です。NMDA受容体はグルタミン酸に応答して開く分子ゲートで、学習関連の結合を形成するのに寄与します。発達初期にはGluN2Bというサブユニットが優勢ですが、後期にはGluN2Aが台頭して受容体の開く時間や強さを変えます。顕微鏡観察により、時間経過とともにより多くのNMDA受容体がシナプス、つまりニューロンの接触点に移動することが示され、とくにBrainPhys培養でその傾向が強まりました。対象を絞った遺伝子解析では“早期型”のGluN2Bの低下と“後期型”GluN2Aの上昇が明らかになり、ニューロンがこの古典的な発達スイッチを経ていることが示されました。
細胞内の電流とカルシウムを追う
これらの分子変化が機能的に重要であることは実験でも確認されました。細い電極を用いて、NMDAというNMDA受容体を選択的に活性化する薬剤で誘発される電流を記録しました。両方の培養条件のニューロンは強い電流を示しましたが、GluN2Aサブユニットを遮断すると電流は約半分に減少し、GluN2Aが信号伝達で主要な役割を担っていることが示されました。続いて蛍光色素でカルシウム(細胞内の重要なメッセンジャー)を追跡しました。NMDAに曝露すると、BrainPhysで育てたニューロンのはるかに大きな割合が強いカルシウムの急上昇を示し、シグナルの大きさも大きかった。遺伝子解析はその理由を示唆します:BrainPhys培養はカルシウムチャネルや放出経路の複数成分を上方制御しており、NMDA受容体の活性化を広範で協調したカルシウムシグナルへと変換する装備が整っているのです。
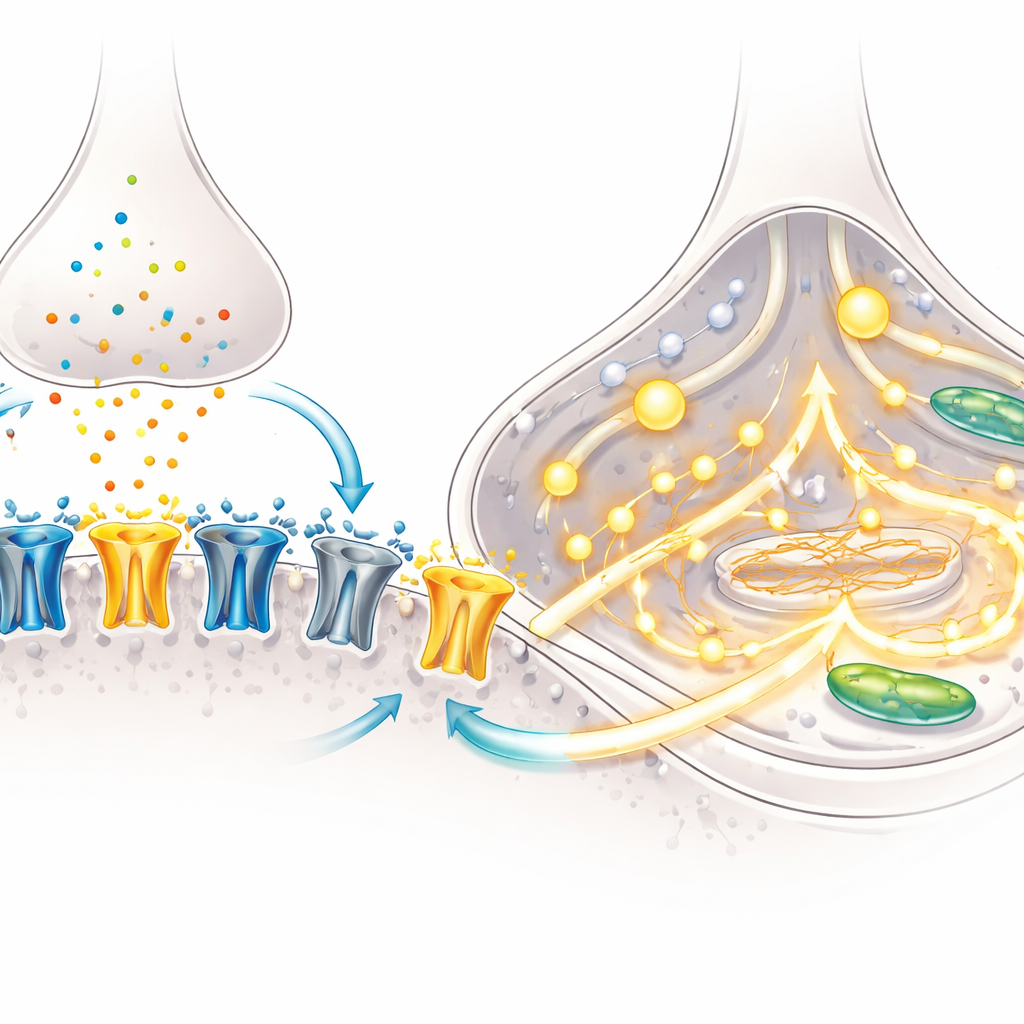
脳疾患研究への示唆
総じて、これらの発見はヒト幹細胞由来ニューロンがわずか2か月で機能的に成熟した状態に達し得ることを示しています。特に活動的なネットワークと現実的なニューロン・アストロサイトの混合を促す条件下で顕著です。この状態では“成人様”のGluN2AサブユニットがNMDA受容体電流を支配し、カルシウムシグナルに強く寄与しており、発達中のヒト脳に見られる様相とよく一致します。一般の読者にとっての要点は、研究者がヒトの興奮性ニューロンがどのように成熟し、配線され、グルタミン酸に応答するかをより忠実に再現する実験室モデルを手に入れたことです。これにより、微妙な遺伝的変化や疾患プロセスがこれらの精緻なスイッチをどのように乱すかを調べることが可能になり、てんかんからアルツハイマー病までの病態への洞察を開き、将来の治療法の設計・検証を導く手がかりとなります。
引用: Escamilla, S., Avilés-Granados, C., Peralta, F.A. et al. GluN2A-mediated currents and calcium signal in human iPSC-derived neurons. Sci Rep 16, 9736 (2026). https://doi.org/10.1038/s41598-026-38482-y
キーワード: NMDA受容体, 幹細胞ニューロン, 脳の発達, カルシウムシグナル伝達, シナプス成熟