Clear Sky Science · ja
二重G9a阻害剤かつヒスタミンH3受容体拮抗薬A-366はBTBR T + tf/Jマウスの反復行動と社会行動を改善し神経炎症を軽減する
このマウス研究が自閉症にとって重要な理由
自閉スペクトラム症(ASD)と暮らす家族は、しばしば一度にごく一部の症状しか和らげられない治療の寄せ集めに直面します。本研究はA-366と呼ばれる新しい実験化合物を検討しており、これは本来非常に異なる二つの生物学的系に同時に作用するよう設計されました。広く用いられる自閉様行動のマウスモデルで、A-366は反復行動を減らし、社会的相互作用を改善し、脳の炎症を鎮めました。これは、単一の薬剤でASDの複数の中核的特徴に同時に対処できる可能性を示唆します。
多面的な状態
ASDは単一の原因を持つ一つの病気ではありません。社交的コミュニケーションの困難、反復行動、しばしば不安や注意問題などの他の課題を伴います。これらの外面的な兆候の背後には、脳内の化学や遺伝子制御の変化が複雑に絡んでいます。現在の薬剤は、例えば抗精神病薬アリピプラゾールのように主にドーパミンやセロトニンといった脳内伝達系を標的とし、刺激性などの付随症状に限定して承認されています。一方で、脳細胞内でDNAがどのように折りたたまれ化学的に標識されるか(エピジェネティクス)や、脳内の免疫・炎症反応の活動もASDで変化することが明らかになっています。これらの多層的な要因は、単一のターゲットに順番に取り組むアプローチが狭すぎる可能性を示唆します。
遺伝子スイッチと脳の伝達系の両方を狙う
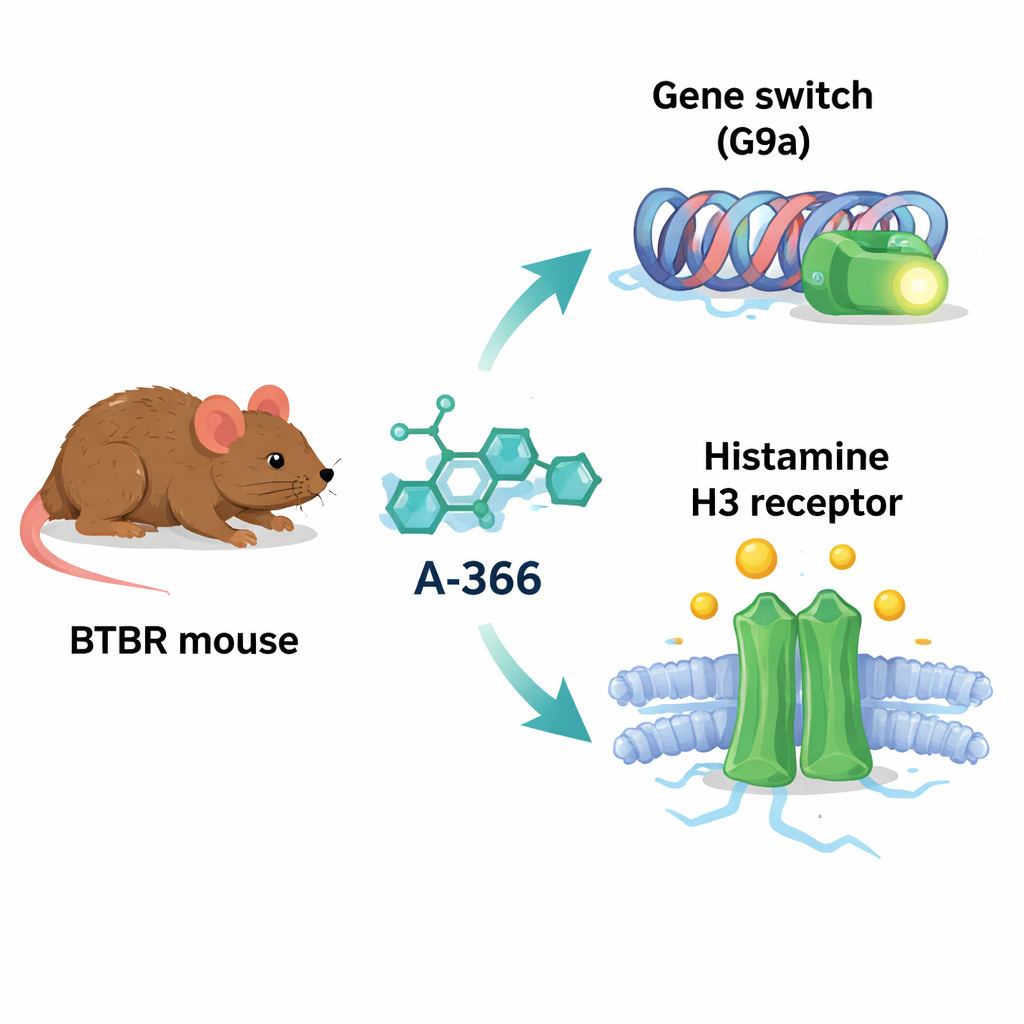
A-366は当初、G9aと呼ばれるタンパク質を阻害するために開発されました。G9aはヒストンタンパク質に化学的標識を付与して遺伝子の発現を抑える傾向がある酵素です。いくつかの脳疾患でG9aの活性やその標識が増加しており、学習や記憶、適切な神経回路に重要な遺伝子が沈黙される可能性があります。興味深いことに、A-366の化学的形状はヒスタミンH3受容体を阻害する薬剤と類似しており、H3受容体はヒスタミンや他の伝達物質の放出を制御するスイッチで、注意、覚醒、社会行動に関連しています。この重なりから著者らは、A-366が「二重作用薬」として働くかもしれないと考えました:G9a阻害によって有害な遺伝子サイレンシングを緩める一方で、H3受容体の遮断によりヒスタミンシグナルを高めるというものです。
自閉様マウスでのA-366の試験
研究チームはBTBR T+tf/Jマウスを用いました。この系統は自然に社交性が低く、強い反復的な毛づくろいや掘削行動、そして高まった脳の炎症を示し、ASDの主要な側面を反映します。雄のBTBRマウスにA-366を3週間、3段階の用量で毎日注射し、その行動を標準的なC57マウスおよびピトリシスタント(標準的なH3受容体拮抗薬)またはアリピプラゾールで処理したBTBRマウスと比較しました。複数の課題において、A-366は用量依存的に掘削、破片化、自己毛づくろいといった反復行動を減少させ、Y字迷路による空間作業記憶の成績を改善しました。三室社会性試験では、A-366は空のケージより他のマウスと過ごすことを好むというマウスの嗜好を回復させただけでなく、最高用量では社会性スコアを標準マウスのレベルまで引き上げ、ピトリシスタントやアリピプラゾールの効果を上回りました。
炎症の鎮静とターゲットの確認
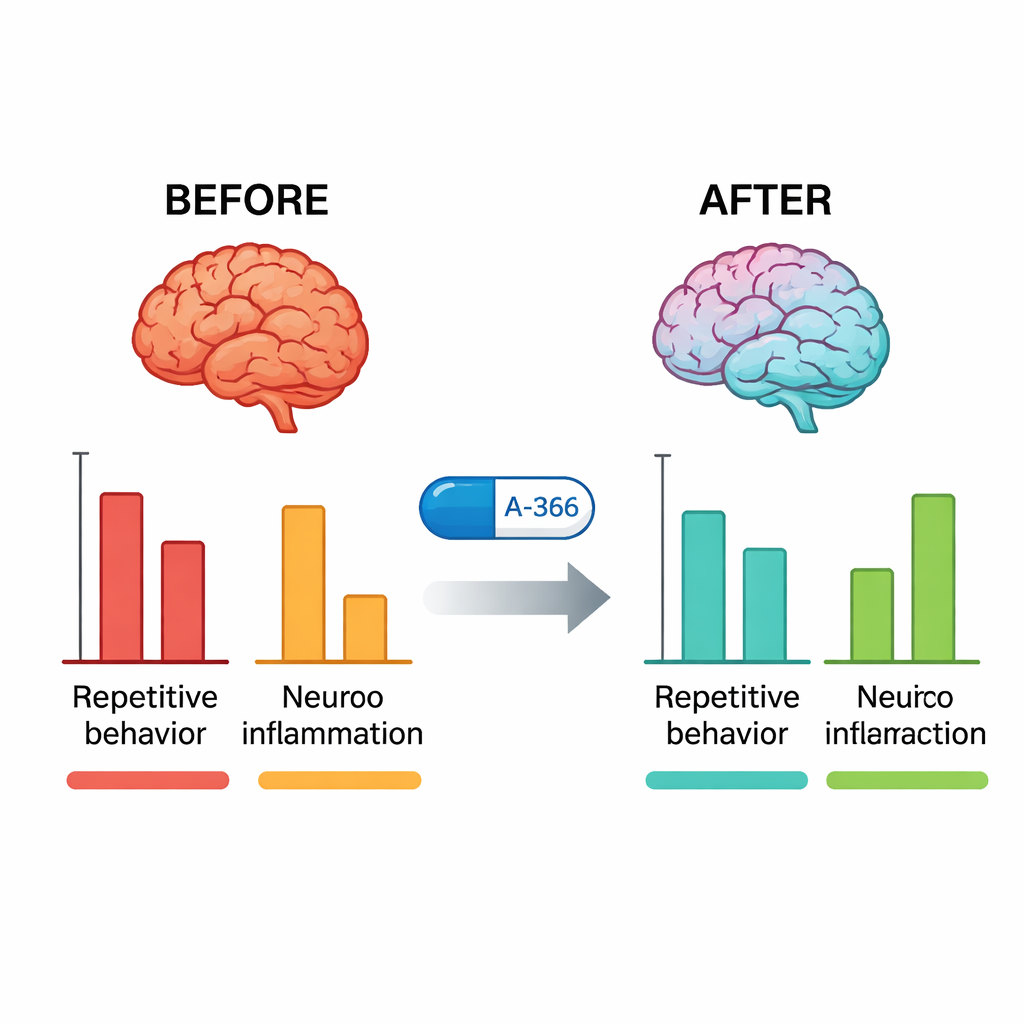
行動試験の後、研究者らはマウスの脳を調べました。未処理のBTBRマウスでは海馬と小脳におけるG9a活性が標準マウスより著しく高かった。A-366での治療はこの活性を急速に正常に近づけるほど低下させたのに対し、ピトリシスタント単独ではそうならず、A-366が実際にエピジェネティック標的に作用していることを確認しました。同時に、主要な炎症性分子であるTNF-α、IL-6、IL-1βはBTBRマウスで大幅に上昇しており、これらはA-366によって有意に低下し、アリピプラゾールよりも強い低下を示しました。さらに、研究者らがA-366にH3受容体を活性化する薬(RAMH)を併用すると、行動および抗炎症の利点は部分的にしか逆転せず、G9a活性の低下は残りました。このパターンは、G9a阻害による安定したエピジェネティックな緩和とH3受容体遮断を介したヒスタミン依存の寄与が組み合わさった作用機序を支持します。
将来の治療にとっての意味
専門外の読者には、本結果は「ソフトウェア」と「メッセージ伝達系」の両方に同時に作用する薬を設計できる可能性を示唆します。この自閉様行動のマウスモデルでは、A-366は有害な遺伝子の抑制を緩めつつヒスタミンシグナルを調整することで、反復行動を和らげ、社会的関与を改善し、慢性の脳炎症の兆候を減少させました。A-366自体は他の疾患向けに開発されたものであり、ヒトでの使用には最適化と広範な安全性試験が必要です。それでも、ASDの複雑な生物学に取り組むために、単一経路への対処だけでは限られた効果しか得られてこなかった状況に対する新しい多標的薬の設計図を提供します。
引用: Hajar, M., Jayaprakash, P., Stark, H. et al. The dual G9a inhibitor and histamine H3 receptor antagonist A-366 improves repetitive and social behaviors and attenuates neuroinflammation in BTBR T + tf/J mice. Sci Rep 16, 7105 (2026). https://doi.org/10.1038/s41598-026-38481-z
キーワード: 自閉スペクトラム症, エピジェネティック療法, ヒスタミンH3受容体, 神経炎症, マウスモデル