Clear Sky Science · ja
ヒト胚性幹細胞からのTCRγδ+T細胞の生成
免疫系を武装する新たな方法
がん治療はますます体自身の免疫系を動員して腫瘍を攻撃する方向へ進んでいます。中でも有望なのがγδ(ガンマ・デルタ)T細胞と呼ばれる免疫細胞で、患者の組織型を正確に認識する必要がなくがん細胞を殺せるため、「既製品(オフ・ザ・シェルフ)」療法の候補として注目されています。しかし成人の血中ではこれらの細胞は稀で、大量に増やすのは困難です。本研究はヒト胚性幹細胞からラボでγδ T細胞を育てる手法を示しており、より入手しやすいがん免疫療法への道を開く可能性があります。
白紙の細胞をがんと戦う兵士へ変える
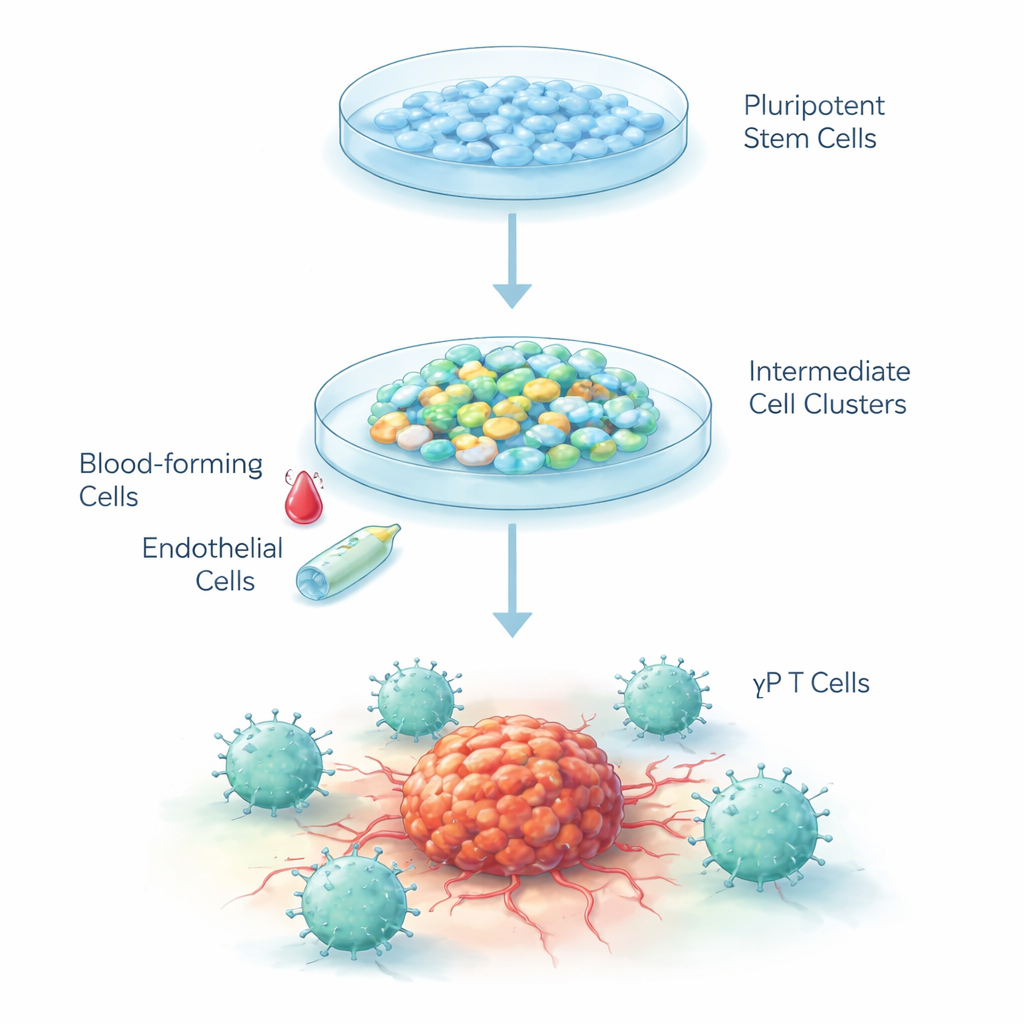
ヒト胚性幹細胞は原理的に体内のほぼ任意の組織に分化し得る「白紙」の細胞です。研究者らは、血液と免疫系が胚で初めて形成される際に辿る経路を模倣する、段階的なレシピを設計しました。三段階のプロセスを用い、まず幹細胞を血管様の初期細胞へ導き、次に未熟な造血前駆細胞へ、最後にγδ型T細胞へと誘導しました。細胞は三次元クラスターとして、発生中の胚を模した低酸素条件の特殊な液体培養で育てられ、成熟に伴って通常の酸素濃度に戻しました。
免疫細胞の製造ラインを構築する
第1段階では化学シグナルで幹細胞を血液や血管の元となる中胚葉へと促しました。6日以内に各クラスターの約40%が“造血内皮細胞”のマーカーを示し、これは血液を生み出す過渡的な細胞型です。第2段階では増殖因子を変えることでこれらの内皮様細胞が遊走性の造血前駆細胞へとスイッチしました。浮遊する細胞の99%超が主要な初期造血マーカーを持ち、約90%が別の造血マーカーを発現しており、免疫系へ進む強い潜在能力を持つ非常に純度の高い集団が得られました。
γδ T細胞への到達
最終段階では、胸腺に通常ある手がかりを模すNotch活性化タンパク質など、T細胞分化を促すシグナルを供給しました。25日後には細胞の40%超が特徴的な表面受容体と、一般的なT細胞に見られるCD4およびCD8のタグを欠く「ダブルネガティブ」プロファイルによりγδ T細胞へ成熟していました。重要な点として、従来型のαβ T細胞はほとんど生成されず、このプロトコルがγδ系への分化を強く促すことが示されました。時間経過に伴う遺伝子解析は、細胞が血液およびT細胞の形成過程を体内で辿るのと非常に近い順序で遺伝子群をオン・オフしていることを明らかにしました。
培養した細胞を試験する
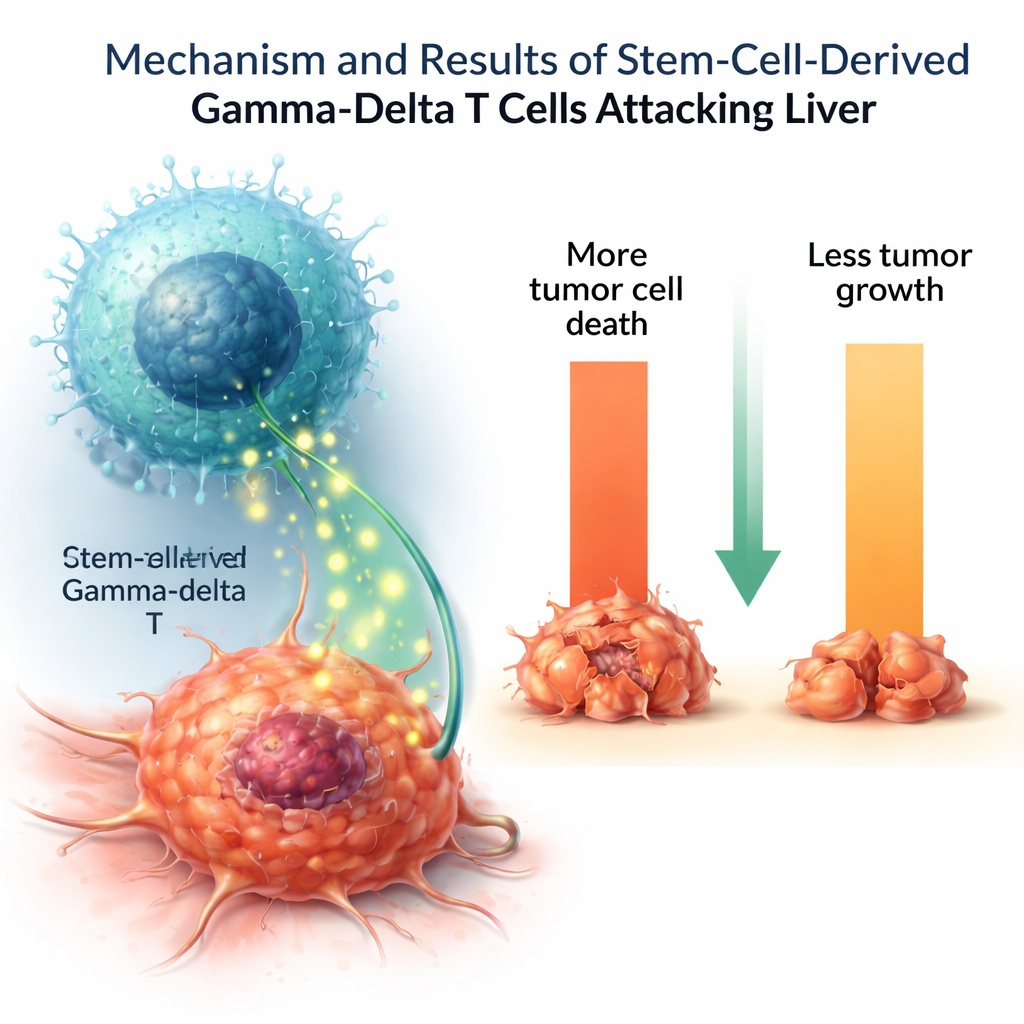
これらのラボ製細胞が実際にがんと戦えるかを確かめるため、研究者らは複数のヒト腫瘍細胞株に暴露させました。γδ T細胞は肝がん細胞のかなりの割合を殺し増殖を抑えた一方で、健常対照細胞にはほとんど影響を与えませんでした。刺激に応じて腫瘍壊死因子やインターロイキン‑2など、免疫反応を調整・増幅する重要なシグナル分子を分泌しました。一方で一部の殺傷分子は自然由来のγδ T細胞より低いレベルで検出され、培養で作られた細胞が完全に成熟していないか、あるいは特定の機能サブタイプを表している可能性が示唆されます。
将来のがん治療にとっての意味
動物由来のフィーダー細胞を使わずに、皿の中で初期造血の簡略版を再現することで、研究者らは1か月未満で大量のγδ T細胞を生産しました。これは従来法より速く簡便です。最終的な細胞混合物の精製、スケールアップ、臨床適合の血清フリー条件への適用などまだ取り組むべき課題はありますが、このアプローチは標準化された再生可能なγδ T細胞の供給源を目指す道を示しています。さらなる安全性と有効性の検証が進めば、これらの細胞は肝腫瘍などのがんに対する次世代の既製免疫療法の広く利用可能な構成要素となる可能性があります。
引用: Zhang, X., Chen, C., Fu, Y. et al. Generation of TCRγδ + T cells from human embryonic stem cells. Sci Rep 16, 6762 (2026). https://doi.org/10.1038/s41598-026-37941-w
キーワード: γδ T細胞, がん免疫療法, ヒト胚性幹細胞, 細胞分化, 肝がん