Clear Sky Science · ja
AT-101はmiR-21-5p/FDX1軸を標的として舌扁平上皮癌細胞の増殖と浸潤を抑制する
この舌癌研究が重要な理由
舌癌は発話、食事、嚥下といった日常生活の機能に重大な影響を及ぼし、現在の治療はこれら機能を損なう一方で病勢を完全には抑えられないことが多い。本研究は植物由来化合物であるAT-101を調べ、実験室モデルで舌扁平上皮癌の増殖と転移を遅らせる仕組みを明らかにしている。腫瘍細胞内の小さな遺伝子制御スイッチを解読することで、研究者たちはこの難治性癌に対するより標的化された治療法の可能性を示している。
現在の舌癌治療の問題点
舌扁平上皮癌は口腔癌の中でも頻度が高く攻撃的なタイプの一つだ。舌は発話や咀嚼に必須であるため、外科医は腫瘍を十分に切除することと機能を温存することを天秤にかけなければならず、それでも局所再発やリンパ節転移に直面する患者が少なくない。標準化学療法は毒性があり、腫瘍が抵抗性を獲得すると効果を失うことがある。こうした限界から、舌癌細胞が増殖し、移動し、周囲組織へ浸潤するための分子機構により精密に作用する薬剤の探索が進んでいる。
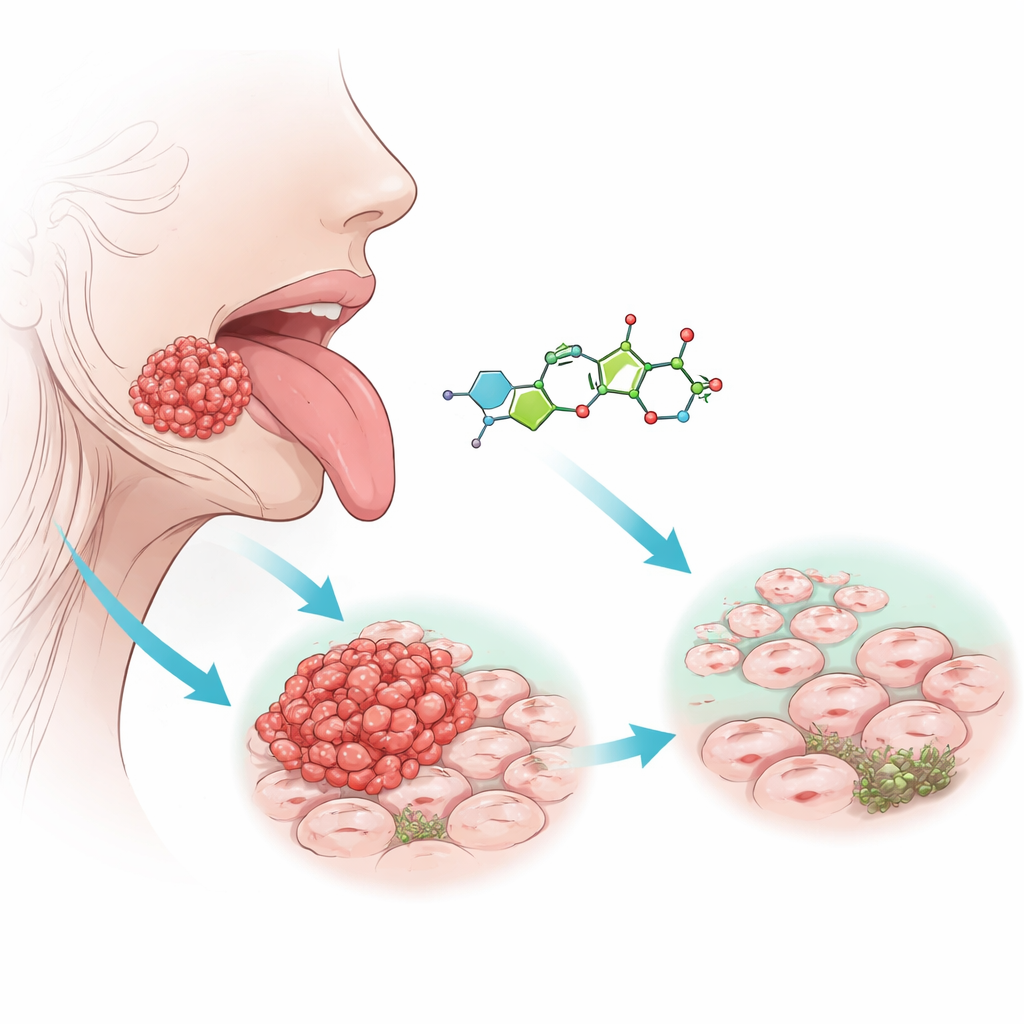
小さなRNAスイッチと防御的タンパク質
研究チームは、遺伝子発現の調節を行う小さな分子であるマイクロRNAに注目した。これらは遺伝子活動の調光スイッチのように働く。中でもmiR-21-5pは多くの癌でアクセルの役割を果たし、細胞の増殖やアポトーシス回避を促進すると知られている。複数の公開遺伝子データベースと舌癌細胞株および患者サンプルを用いた実験により、舌腫瘍ではmiR-21-5pの発現が著しく増加し、一方でFDX1というタンパク質は著しく減少していることが判明した。FDX1はミトコンドリア内での健全な細胞代謝を維持するのに関与し、癌的振る舞いに対するブレーキとして作用するように見える。細胞が作るmiR-21-5pが多いほどFDX1は少なくなり、両者が密接に結びついた制御軸を形成していることが示された。
細胞と腫瘍でのオン・オフ関係の立証
培養された舌癌細胞でmiR-21-5pを増強すると細胞はより速く増殖し、移動性や浸潤能が高まった。逆に抑えるとその効果は逆転した。研究者たちはmiR-21-5pがFDX1をコードする遺伝情報に直接結合してその産生を抑えることを示した。FDX1自体を減少させると、細胞は高miR-21-5pと同様の攻撃的な挙動を示し、FDX1を戻すと増殖が鈍り移動や人工膜を介した浸潤が減少した。ヒト舌癌細胞を移植したマウスでは、FDX1を増強すると細胞死が増え腫瘍が小さくなり、逆にFDX1をサイレンシングすると腫瘍は大きくより活発になることから、その保護的役割が強調された。
綿花由来化合物が軸を書き換える
AT-101は綿花に由来する天然物ゴシポールの精製形態で、以前から癌細胞を自己破壊に導く能力が研究されてきた。著者らはAT-101が舌癌細胞においてmiR-21-5pのレベルを低下させ、同時にFDX1を回復させることを見出した。用量を慎重に選ぶと、AT-101は癌細胞の増殖、遊走、浸潤を強力に抑えたが、正常な口腔細胞に対する影響ははるかに穏やかだった。miR-21-5pを人工的に増加させるとAT-101による増殖抑制効果が部分的に救済され、逆にmiR-21-5pを阻害すると薬剤の効果は増強された。対照的にFDX1を除去するとAT-101の有益効果は弱まり、AT-101が主にmiR-21-5pの抑制からFDX1を解放することで作用することが示唆された。
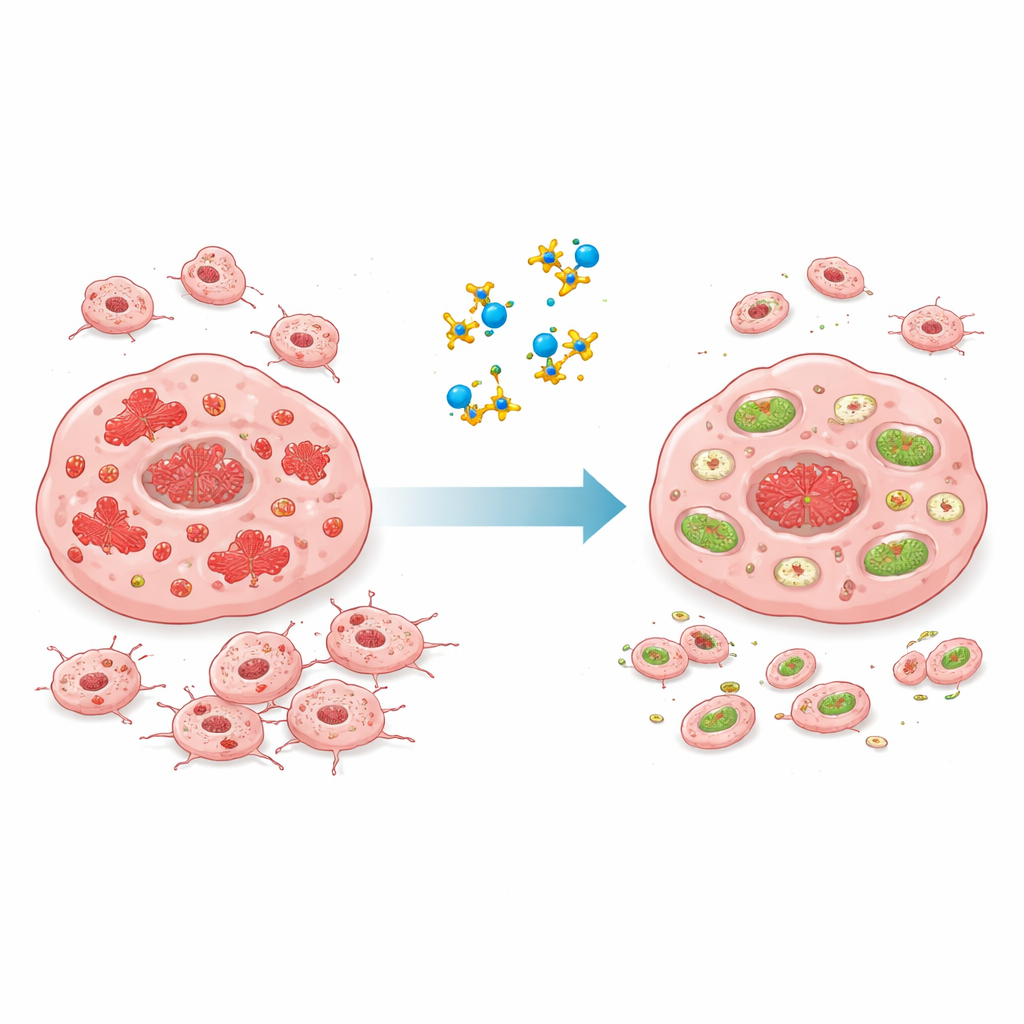
将来の治療への示唆
専門外の読者にとっての要点は、研究者たちが因果の連鎖をたどったことだ。過剰に活性化したマイクロRNA(miR-21-5p)が防御的タンパク質(FDX1)を沈黙させることで舌癌細胞の増殖と転移が進み、天然化合物AT-101はこの連鎖を断ちFDX1の保護的な働きを回復させる。これらの発見はまだ実験室および動物研究段階にあるが、AT-101をモデルとした薬剤や同じRNA–タンパク質回路を標的にする併用療法が、外科手術や広域化学療法に頼るだけでなく、より精密で副作用の少ない舌癌治療をもたらす可能性を示している。本研究は、癌の内部スイッチをはずすことを目指した将来の治療設計のための明確な分子ロードマップを提供している。
引用: Fu, S., Cui, Qy., Tuo, Xy. et al. AT-101 inhibits the proliferation and invasion of tongue squamous carcinoma cells by targeting the miR-21-5p/FDX1 axis. Sci Rep 16, 10361 (2026). https://doi.org/10.1038/s41598-026-37710-9
キーワード: 舌癌, マイクロRNA, 標的療法, 天然化合物, 細胞代謝