Clear Sky Science · ja
APOL1の細胞膜プールは急速なタンパク質分解に抵抗する
腎臓タンパク質の「消える」挙動が重要な理由
近年アフリカ系の祖先を持つ人々の重篤な腎疾患の多くが、単一遺伝子APOL1の2つの変異に結び付けられています。それでも、なぜこの遺伝子が多くの保因者には害を与えずに腎細胞を傷つけるのか、正確な仕組みは未解明のままです。本研究は一見単純だが重要な問いを投げかけます:細胞内でAPOL1タンパク質が作られた後、どれくらいの期間残り、どこで最も安定しているのか?答えは驚くべき二面性を示します—APOL1は細胞内では急速に分解される一方で、細胞外側の膜に埋め込まれると頑強に安定する。これは将来の治療を導く手がかりになり得ます。
二面性を持つリスク遺伝子
APOL1遺伝子は特定の寄生虫から人間を守る働きがあり、この進化上の利点が、リスク変異(G1およびG2)がアフリカ系集団に多い理由と考えられます。しかし残念なことに、これらの変異を二コピー受け継いだ人々はAPOL1関連腎疾患と総称される腎障害のリスクが大幅に高まります。以前の研究は、炎症などに応じてAPOL1量が増えると、特に糸球体のろ過を担う繊細な細胞であるポドサイトに対してタンパク質が毒性を示すことを示してきました。とはいえ、ほとんどの研究はAPOL1がどのようにオンになるかに着目しており、細胞がそれをどうオフにするか、例えばどのように分解するかについてはあまり知られていませんでした。
細胞内で壊れやすいタンパク質を追跡する
APOL1の安定性を調べるため、研究者らはヒト細胞株を遺伝子操作してAPOL1とその最も近い親族であるAPOL2の蛍光タグ付きバージョンを発現させました。これにより、ウエスタンブロット、顕微鏡観察、フローサイトメトリーを使って、各タンパク質が異なる条件下でどれだけ蓄積・消失するかを追跡できました。彼らは細胞の主要なタンパク質分解装置であるプロテアソームを阻害し、別に新規タンパク質合成を阻止しました。プロテアソームを阻害するとAPOL1レベルは急速に上昇し、通常は高速で分解されていることが示されました。新規合成を止めるとAPOL1レベルは急落しました。対照的にAPOL2はどちらの処理でもほとんど変化せず、はるかに安定なタンパク質であることが明らかになりました。重要なのは、APOL1の高いターンオーバーは正常型(G0)でもリスク型(G1およびG2)でも同様であり、膜内での配置が異なるいくつかの自然発生型APOL1でも同じであったことです。
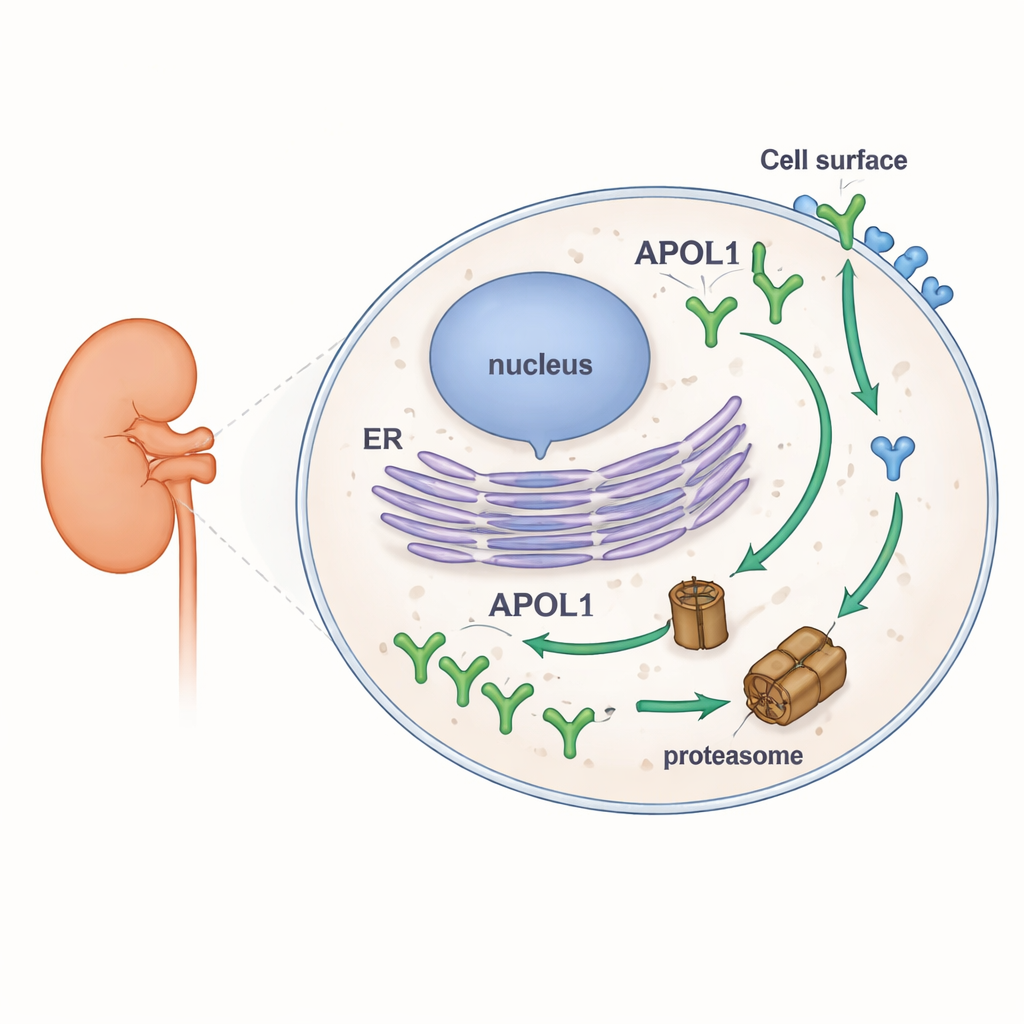
配列の手がかりと二つの居場所の物語
タンパク質構造を掘り下げると、研究チームは計算ツールを用いてAPOL1とAPOL2に存在する柔軟で構造を持たないセグメント(内在性無秩序領域)をスキャンしました。こうした領域はしばしばプロテアソームに対する“食べてください”シグナルとして働きます。APOL1にはAPOL2にはほとんど見られない2つの強い候補領域が同定されました。APOL1の独特な前端がその脆弱性に寄与しているかを調べるため、彼らはハイブリッドを作成しました:最初の59アミノ酸を欠く短縮型APOL1と、そのAPOL1断片を持つAPOL2キメラです。APOL1のN末端部分をAPOL2に付加するとAPOL2はより速く分解されるようになり、一方で短縮APOL1は依然として不安定なままでした。これはAPOL1の複数の部位が急速な分解を促していることを示唆します。これらの結果は、APOL1の異常な柔軟領域が高速ターンオーバーに結びつくことを示す一方で、この挙動が必ずしも疾患を引き起こす変異に特有のものではないことを示しています。
細胞表面で頑強なタンパク質
最も注目すべき発見は、細胞内にあるAPOL1と細胞表面にあるAPOL1を区別したときに現れました。外側に露出する部分だけを認識する抗体を用いて、表面レベルを全体レベルと分けて測定しました。細胞内のAPOL1は予想どおりに振る舞い、プロテアソームが阻害されると蓄積し、新規合成が止まると急速に消失しました。しかし表面のAPOL1はどちらの条件でもほとんど動じませんでした。一度APOL1分子が細胞膜に到達すると、急速な分解に対して非常に抵抗性を示したのです。さらに、リスク変異は総APOL1量を減らす傾向にあるものの、表面レベルは正常型と似ていました。これは、リスク型と正常型のAPOL1が細胞内では同程度にクリアランスされるが、イオンチャネルを形成して毒性を引き起こすと考えられる膜埋め込みプールはすべてのバリアントで保存されていることを示唆します。
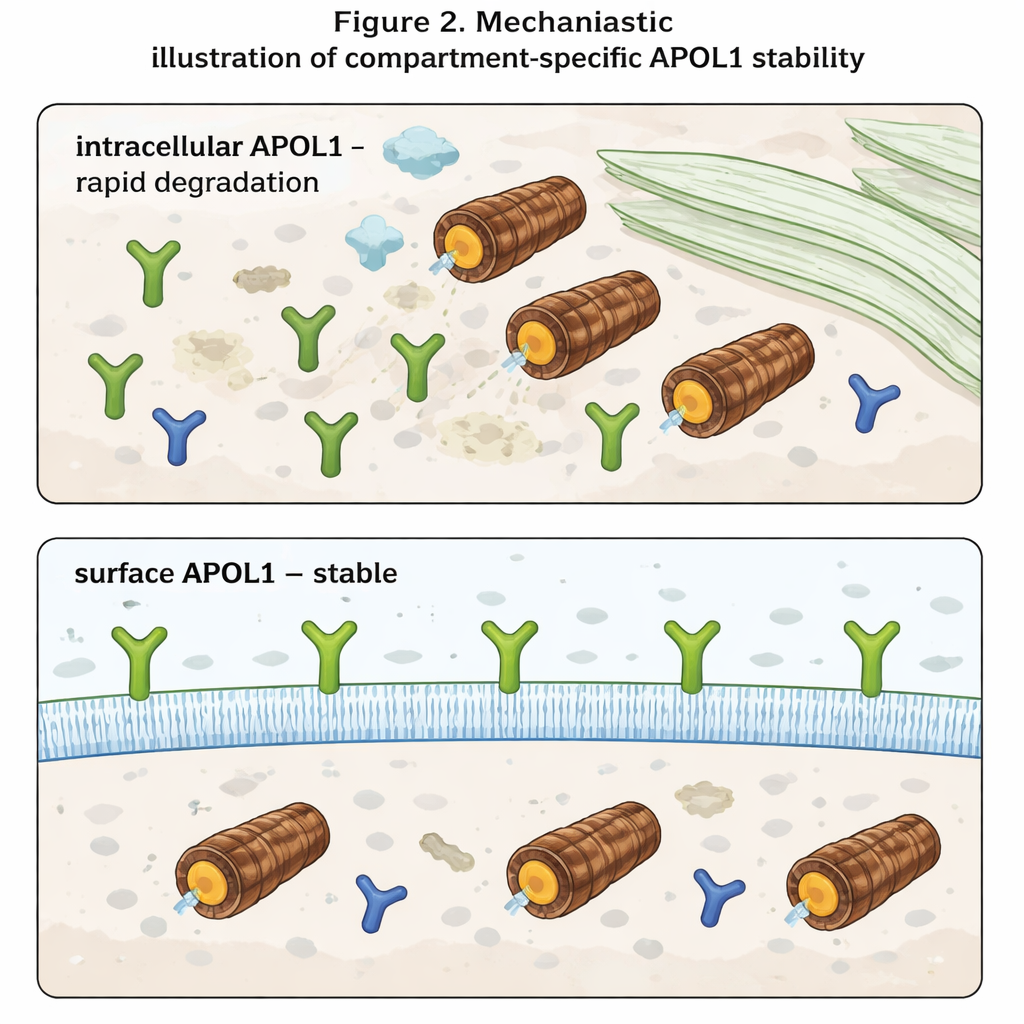
今後の治療への示唆
専門外の読者への要点は、APOL1は居場所によって非常に異なる振る舞いをするということです。細胞内では短命なタンパク質で、素早く認識され分解されます。細胞表面では長寿命で比較的保護され、細胞の分解機構が変化してもそうした性質は維持されます。疾患は表面のAPOL1チャネルがナトリウムやカリウムのようなイオンのバランスを乱すときに生じるように見えるため、治療は総APOL1量よりもどれだけが細胞膜へ到達し持続するかに注目する必要があるかもしれません。APOL1の細胞表面への輸送を減らすか、表面プールだけを選択的に不安定化する戦略は、遺伝子の有益な免疫機能を完全に阻害することなく腎障害を和らげる可能性があります。
引用: Höffken, V., Alvermann, L., Niggemeier, D. et al. APOL1 plasma membrane pools resist rapid protein degradation. Sci Rep 16, 6718 (2026). https://doi.org/10.1038/s41598-026-37647-z
キーワード: APOL1, 腎臓病, タンパク質分解, 細胞膜, プロテアソーム