Clear Sky Science · ja
ヒトヒストン脱アセチル化酵素5の触媒ドメインのin vitro特性解析
DNAの梱包にある小さなスイッチが重要な理由
すべての細胞内で、私たちのDNAはスプールのように働くタンパク質に巻き付いており、何メートルにも及ぶ遺伝情報を微小な空間に収めています。ある遺伝子がオンかオフかは、多くの場合これらのスプールタンパク質上の小さな化学タグによって左右されます。本研究はHDAC5と呼ばれる特定のタンパク質“スイッチ”に焦点を当てます。HDAC5は心疾患、脳障害、がんなどと関連しており、その分子レベルでの動作を理解することで、副作用を抑えたより精密な薬の開発につながることが期待されます。
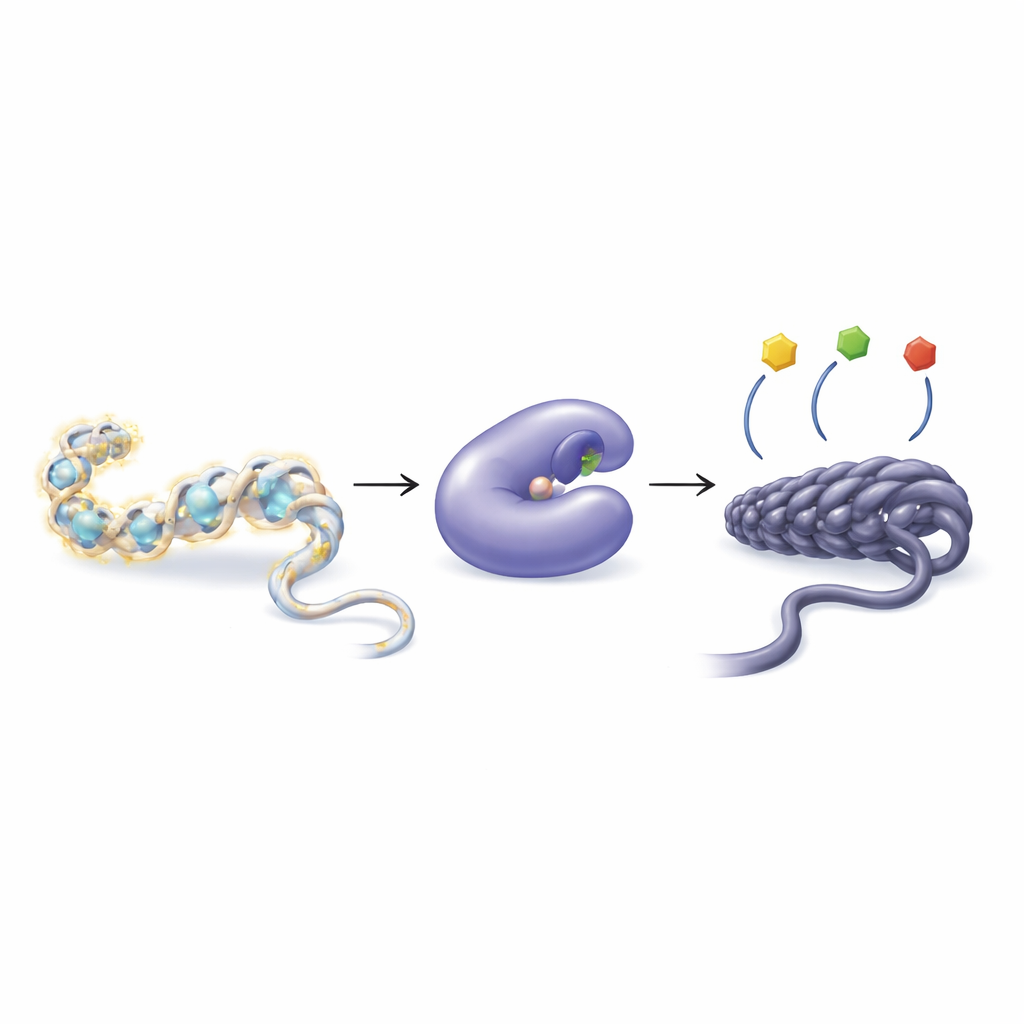
細胞が小さな化学タグで遺伝子を調節する仕組み
DNAは自由に浮いているのではなく、ヒストンと呼ばれるタンパク質に巻き付いてクロマチンという構造を形成します。細胞はヒストンの末端にアセチル基のような小さな化学基を付けたり外したりして、クロマチンをゆるくしたり締めたりします。ゆるい梱包は一般に遺伝子の読みやすさを高め、締まった梱包は遺伝子の沈黙化を招きます。このバランスを管理する酵素群は、ヒストンアセチルトランスフェラーゼ(アセチル基を付加する)とヒストン脱アセチル化酵素(HDAC、アセチル基を除去する)です。この均衡が崩れると、がん、心疾患、筋萎縮、免疫疾患など幅広い疾患に寄与し得ます。
HDAC5が有望だが扱いが難しい薬物標的である理由
HDACは複数のクラスに分かれる大きな酵素ファミリーを形成しています。現在臨床で使われている多くの薬は複数のHDAC型を一度に阻害するため、重要な正常機能まで妨げられ強い副作用を引き起こしがちです。クラスIIaのHDAC(HDAC5を含む)は、脳、心臓、骨格筋など特定の組織で豊富に発現し、他のタンパク質と連携して重要な遺伝子ネットワークを制御する点で際立っています。HDAC5はしばしば架け橋として働き、強力に活性を持つパートナー酵素(HDAC3)を特定の遺伝子へ誘導してクロマチンを締め、遺伝子を抑制します。こうした局所的な役割ゆえにHDAC5は選択的薬剤の魅力的な標的と考えられますが、その触媒コアの高解像度構造がなく詳細な生化学データが不足していたため、合理的な薬剤設計が難しい状況でした。
試験管内でHDAC5を再構築する
このギャップに取り組むため、研究者たちはヒトHDAC5の触媒コア、すなわち化学反応を担う部分のみを細菌で発現・精製し、溶液中で安定した単量体として存在することを確認しました。次に、異なる塩濃度や酸性度での活性を評価しました。HDAC5の活性は広い塩濃度範囲で堅調に維持され、やや塩基性の条件で活性のピークを示し、これは多くの細胞内環境と類似していました。特殊な蛍光検査基質を用いると、野生型のHDAC5はクラスIIa酵素を調べる際に一般的に用いられる特定の一種類の基質のみを認識することが分かりました。関連するHDACに関する先行研究に基づき、重要な部位の一つのアミノ酸(ヒスチジン)をチロシンに置換しました。驚くべきことに、この小さな変化により変異体のHDAC5は双方の種類の検査用基質を効率よく処理できるようになり、触媒部位の単一残基が酵素の基質選択性をどのように決めているかが明らかになりました。
2つの新しい薬剤候補の評価と比較
次に研究チームは、NT160とFFK24として知られる2つの実験的なHDAC5阻害化合物を検討しました。これらの化合物は、古いヒドロキサマート系薬に見られるいくつかの毒性や選択性の問題を回避する新しい亜鉛結合基を利用しています。各阻害剤がHDAC5の反応をどの程度遅らせるかを精密な反応系で測定したところ、極めて低いナノモル領域の阻害定数が得られ、両化合物とも酵素に強く結合することが示されました。NT160は一貫してFFK24より約10倍強く結合しました。その理由を探るため、研究者らはHDAC5触媒コアのAlphaFold予測構造を用いたコンピュータドッキングを行いました。両阻害剤は金属イオンに接触する活性ポケットの深部に入り込む共通の頭部領域を持っていましたが、NT160の尾部はポケット内の特定のアミノ酸と追加の安定化相互作用を形成していました。これらの追加の相互作用が、より高い効力を説明していると考えられます。
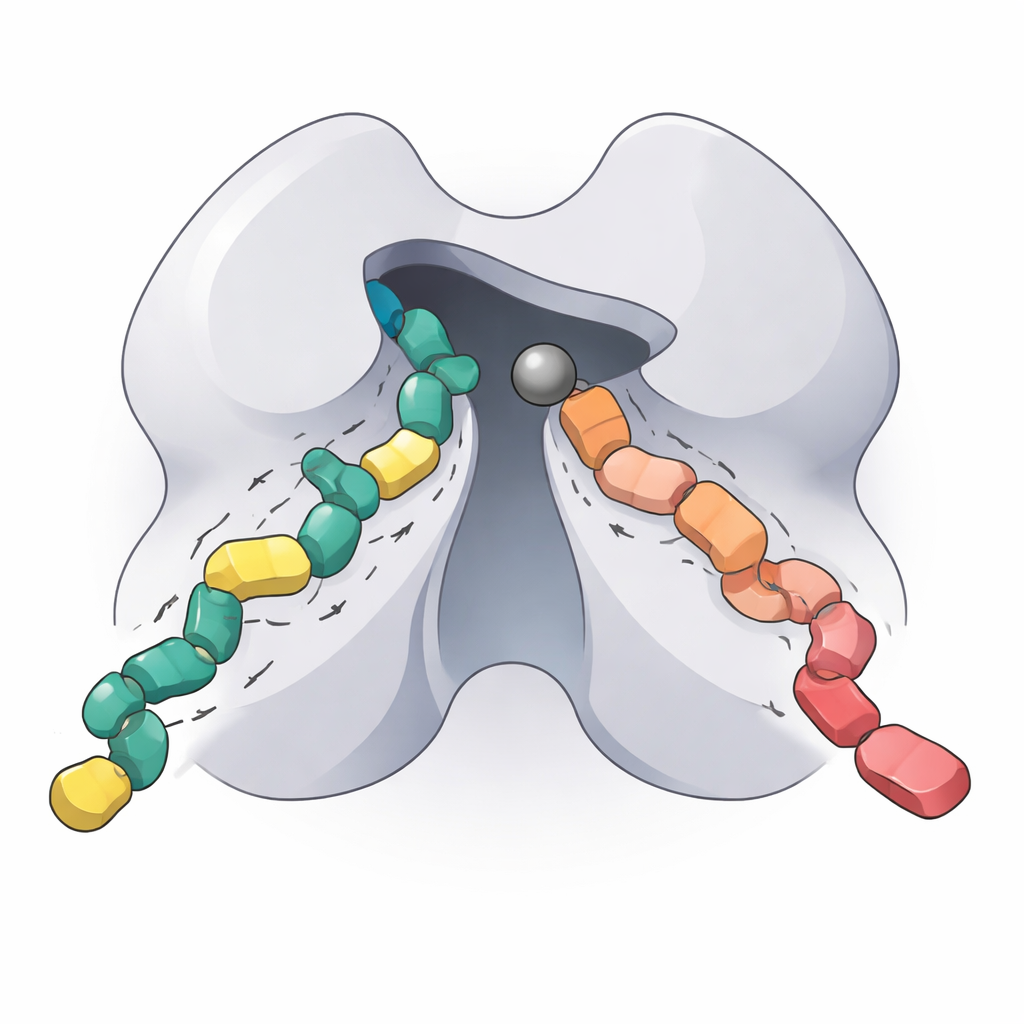
将来の標的治療にとっての意義
本研究はHDAC5の作動コアを再構築し、最適な作動条件をマッピングし、単一アミノ酸の変化が挙動をどのように変えるかを解析し、2つの次世代阻害剤がどのように結合するかを定量化することで、これまで十分に特徴付けられていなかった重要な酵素の詳細な生化学的“フィンガープリント”を提供します。専門外の読者への要点は、HDAC5が特定の遺伝子のオン・オフを制御するのを助け、そのスイッチを精密に調節することが心疾患、神経変性、がん、免疫疾患の治療に有用であり得るということです。ここで得られた新たな知見とツールは、必要な場所で作用しつつ体の他の部位での不要な影響を最小限に抑えるHDAC5およびクラスIIa選択的薬剤の設計を助けるはずです。
引用: Mammen, C., Hornung, F.M., Anzenhofer, C. et al. In vitro characterization of the catalytic domain of human histone deacetylase 5. Sci Rep 16, 7935 (2026). https://doi.org/10.1038/s41598-026-37633-5
キーワード: ヒストン脱アセチル化酵素5, エピジェネティック制御, HDAC阻害剤, 標的化がん治療, クロマチン構造