Clear Sky Science · ja
コピー数増幅がIFI30過剰発現と協調的免疫活性化を駆動し、胃腺癌における新規診断・治療ターゲットを同定する
なぜ胃のタンパク質が重要なのか
胃がんは世界で最も致命的ながんの一つであり、その多くは発見が遅く治療が難しいことが主な理由です。本研究は、免疫系が脅威を認識するのを助ける細胞に存在するあまり知られていないタンパク質IFI30に着目します。胃腫瘍でのIFI30の変化とそれが体の防御に与える影響をたどることで、研究者らはより早期の診断や、より効果的で個別化された治療の選択に役立つ強力な手がかりになり得ることを示唆します。
胃腫瘍に潜むシグナル
研究チームはまず基本的な問いを立てました:IFI30は健康な胃組織とがん組織で発現量が異なるのか。何千ものサンプルからの遺伝子発現を統合した大規模な公開データセットを用いると、IFI30は胃腺癌(胃がんで最も一般的な型)で正常な胃粘膜に比べて一貫して高発現していることが明らかになりました。この傾向は複数の独立した患者群およびRNAとタンパク質の両レベルで確認されました。IFI30単独で腫瘍組織と正常組織を識別できるかを評価したところ、その診断能(AUC)は0.92と顕著で、単一マーカーとしては優れた性能です。顕微鏡画像はまた、IFI30が抗原が免疫認識のために処理される細胞内のリサイクル系(エンドソーム/リソソーム系)に局在することを示しました。
IFI30を上げるDNAの変化
次に研究者らは、なぜIFI30がこれらの腫瘍で高くなるのかを調べました。The Cancer Genome Atlasのがんゲノムをスキャンしたところ、IFI30遺伝子のコピー数増幅(コピー数の過剰)がその過剰発現の主な駆動因子であることが判明しました。IFI30が増幅した腫瘍は全体的なゲノム不安定性が高く、TP53やPIK3CAなどよく知られたがん変異を伴うことが多かった。IFI30のコピー数が増えるに従ってRNAレベルも上昇しており、構造的なDNA変化とこのタンパク質の産生増加との直接的な関連を示唆しています。これによりIFI30は単なる傍観者ではなく、より攻撃的な腫瘍生物学の一部であることが浮かび上がります。
腫瘍周囲の免疫クロストーク
IFI30は免疫細胞が抗原をT細胞に「指名手配ポスター」として提示する過程に関与するため、研究チームはそれが腫瘍微小環境のどこに位置するかを詳しく調べました。単一細胞シーケンス(個々の細胞の遺伝子発現を読み取る方法)により、IFI30は樹状細胞、マクロファージ、CD8陽性T細胞といった抗腫瘍免疫を開始・維持する主要な細胞に特に豊富であることが示されました。ネットワーク解析は、IFI30豊富な免疫細胞と周囲の腫瘍細胞や支持細胞との間に密なコミュニケーションがあることを明らかにしました。IFI30高発現腫瘍は、抗原提示、炎症シグナル、免疫細胞を引き寄せ組織化する通信分子に関連する経路の強い活性化を示しました。同時に、これらの腫瘍は細胞周期の促進、組織再構築、低酸素適応など浸潤やストレスの特徴も示しており、IFI30が腫瘍内での攻撃と防御の交差点に関与していることを浮き彫りにしています。
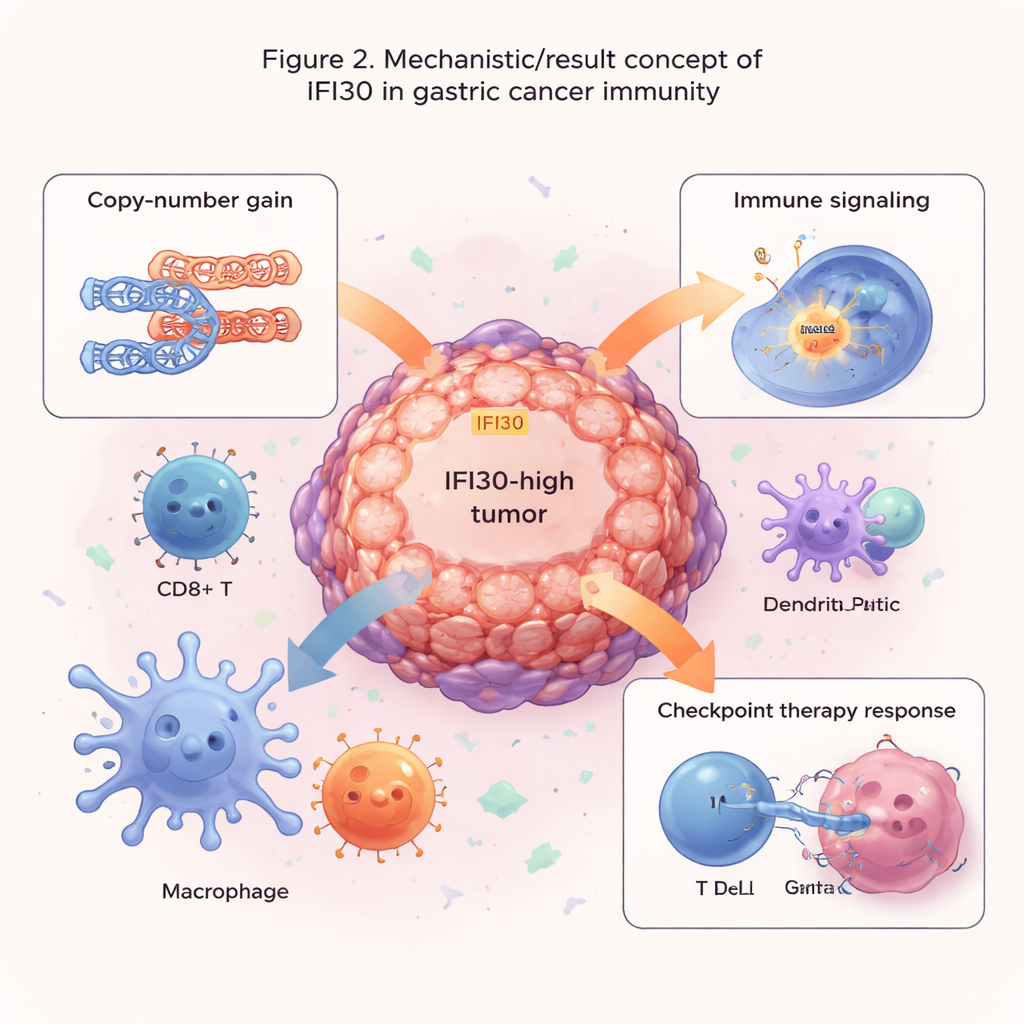
薬剤選択と免疫療法の手がかり
著者らは次に、IFI30が治療への反応を予測するのに役立つかどうかを検討しました。IFI30の発現と大規模な薬剤反応データセットを組み合わせると、IFI30高発現腫瘍は細胞分裂を標的とする薬や一般的な増殖経路(MAPK)を阻害する薬に抵抗性を示す傾向がある一方で、EGFRやPI3K/AKTシグナルを遮断する薬には感受性が高いように見えました。注目すべきは、IFI30のレベルがPD-L1と密接に連動していたことで、PD-L1は現在のチェックポイント阻害薬が標的とする主要なT細胞抑制因子です。いくつかの免疫療法研究を通して、腫瘍でIFI30発現が高い患者は低い患者よりもチェックポイント阻害に反応する可能性が高いことが示されました。IFI30に基づくスコアは腫瘍変異負荷やPD-L1単独といった既存の指標より優れており、とくにマイクロサテライト不安定性(MSI)が高い腫瘍群で豊富に見られました。MSI高は既に免疫療法に比較的良く反応することが知られているサブグループです。
基礎研究から新たな標的へ
IFI30が単なるマーカーなのか腫瘍増殖を促進する因子でもあるのかを検証するため、研究チームは遺伝学的手法で胃がん細胞株のIFI30レベルを下げました。IFI30をノックダウンするとがん細胞の増殖が遅くなり、腫瘍増殖の維持に直接関与していることが示されました。総合すると、IFI30は免疫活動の指標であると同時に悪性挙動に寄与する因子でもあることが示唆されます。患者にとっては、将来的にIFI30の簡便な測定が胃がんの検出をより確実にし、特定の分子標的薬や免疫療法が有効な患者を予測し、あるいはIFI30の腫瘍促進作用を直接的または間接的に阻害する新たな治療法の開発に道を開く可能性があります。
引用: Liu, Q., Yuan, W., Zhaowang, R. et al. Copy-number amplification drives IFI30 overexpression and coordinated immune activation, identifying a novel diagnostic and therapeutic target in gastric adenocarcinoma. Sci Rep 16, 6945 (2026). https://doi.org/10.1038/s41598-026-37574-z
キーワード: 胃がん, IFI30, バイオマーカー, 腫瘍免疫, 免疫療法